Clear Sky Science · nl
Deglycosylering veroorzaakt een nieuwe distale conformatie in de mannose-receptor CD206
Waarom suikerlaagjes op immuunsensoren ertoe doen
Onze immuuncellen vertrouwen op moleculaire "antennes" om bedreigingen zoals microben en kankercellen te detecteren. Een van deze antennes, de mannose-receptor CD206, helpt immuuncellen suiker-gedecoreerde moleculen te grijpen en kan zich zelfs richten op tumoren. Zoals veel eiwitten is CD206 zelf bedekt met korte suikerketens. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote implicaties: wat gebeurt er met de vorm en functie van CD206 wanneer die suikers worden verwijderd?
Een flexibele arm die suikerachtige signalen leest
CD206 bevindt zich aan het oppervlak van bepaalde immuuncellen, vooral macrofagen die weefsels en tumoren patrouilleren. Het heeft een lange, gewrichtachtige structuur die vanaf het celmembraan uitsteekt en eindigt in meerdere "lectine"-segmenten die suikers op passerende moleculen herkennen. CD206 kan ook worden afgesplitst en in de bloedbaan vrijkomen, waarbij de concentratie samenhangt met inflammatoire en fibrotische aandoeningen, waardoor het een potentiële ziekte-indicator is. Het eiwit is sterk geglycosyleerd met N-gebonden suikerketens; eerder werk toonde al aan dat deze suikers kunnen beïnvloeden hoe effectief verschillende segmenten van de receptor suikers herkennen. Veel van deze suikerlokaties liggen ver van de belangrijkste bindingspocketen, wat suggereert dat ze meer als afstandsregelaars dan als simpele blokkeringen kunnen fungeren.
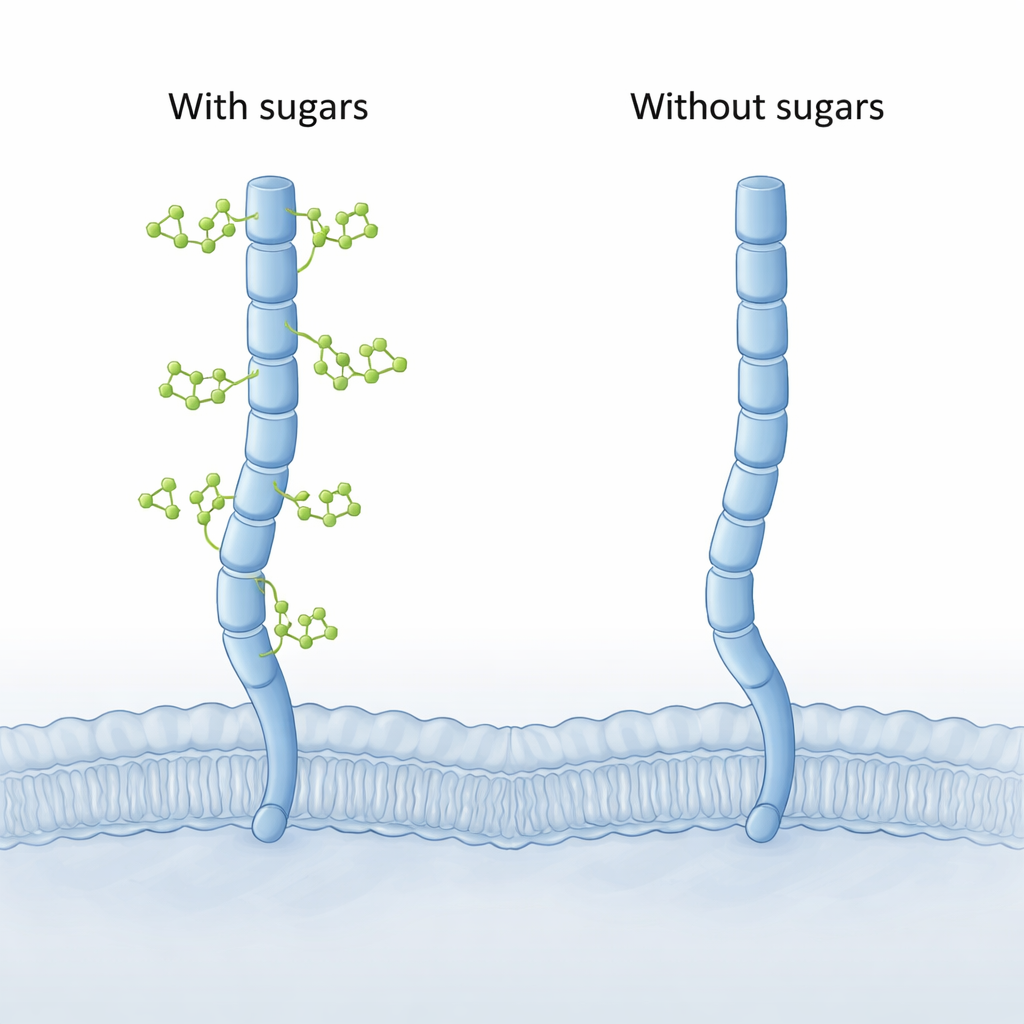
Computermodellen onthullen een verborgen buiging
Aangezien de volledige 3D-structuur van CD206 nog niet experimenteel is vastgelegd, wendden de auteurs zich tot moderne computationele hulpmiddelen. Ze gebruikten eerst AlphaFold om volledige modellen van de receptor te bouwen en voerden vervolgens lange, gedetailleerde moleculaire dynamica-simulaties uit van CD206 met en zonder de gebonden suikers. Beide versies gedroegen zich als een uitgestrekte moleculaire arm, maar de "suikervrije" vorm toonde een opvallende nieuwe beweging aan het uiterste uiteinde. De laatste twee lectine-segmenten (CTLD7 en CTLD8 genoemd) konden naar binnen zwaaien en een concave, naar binnen gekromde punt vormen — een vorm die nooit werd gezien in de geglycosyleerde versie, die meer naar buiten gekromd (convex) bleef.
Hoe een kleine verandering de beweging hervormt
Om dit verschil te begrijpen analyseerde het team de dominante bewegingen in hun simulaties. Ze ontdekten dat de belangrijkste beweging die de twee vormen onderscheidt die buiging van het distale uiteinde was, en dat die alleen optrad wanneer suikers ontbraken. Het verwijderen van suikers maakte de receptor over het algemeen flexibeler, vooral in de afstandelijke lectine-segmenten en in iets mindere mate nabij het N-terminale uiteinde. Correlatiekaarten van hoe verschillende delen van het eiwit samen bewegen toonden aan dat zonder suikers de laatste twee lectine-segmenten meer gecoördineerd bewegen en sterker gekoppeld zijn aan andere regio's. In wezen zitten de suikers niet alleen aan het oppervlak; ze helpen te regelen hoe de hele arm buigt en hoe communicatie langs de lengte plaatsvindt.
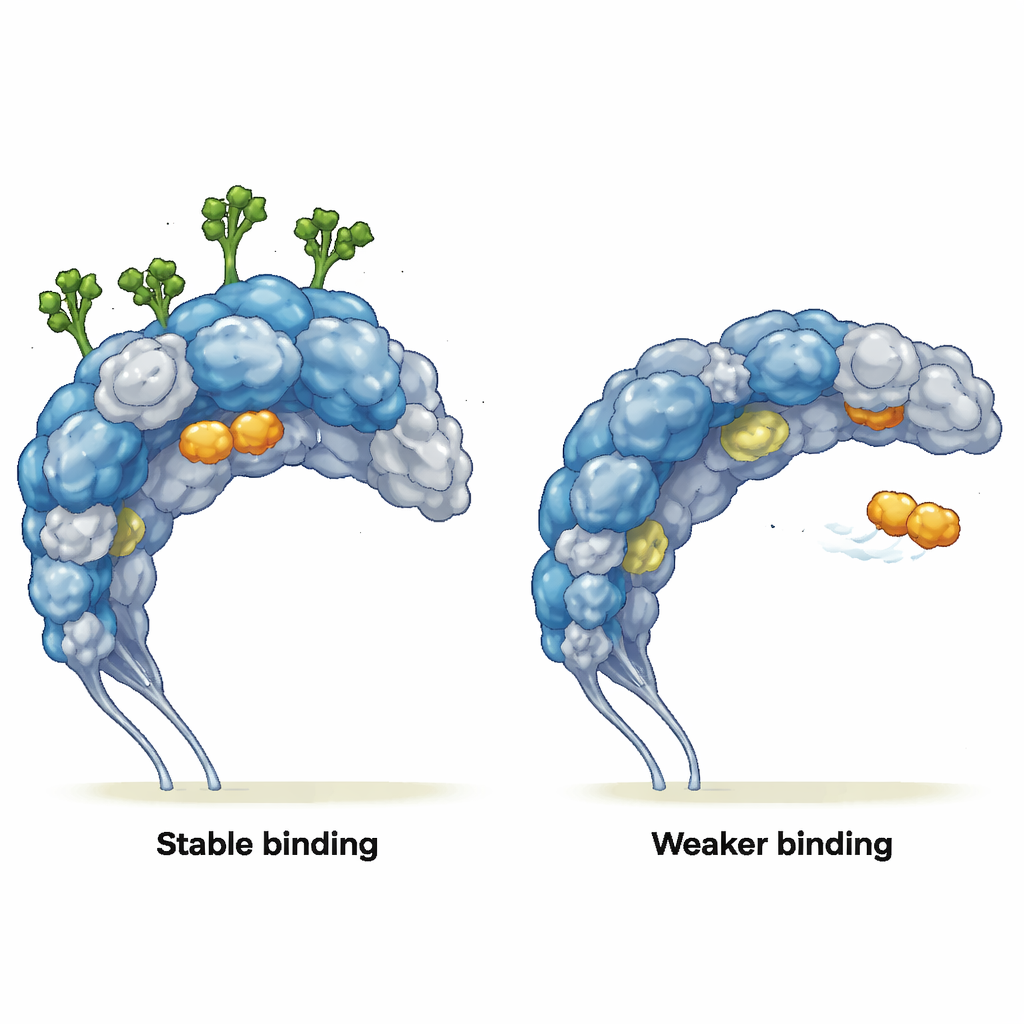
De manier waarop partners binden verandert
De auteurs onderzochten vervolgens hoe deze gewijzigde beweging echte bindingspartners beïnvloedt. Ze simuleerden interacties met twee liganden: een eenvoudige mannose-achtige suiker (MMA), die in een goed gedefinieerde pocket past, en een tumor-gericht peptide genaamd mUNO, dat zich richt op CD206-positieve tumor-geassocieerde macrofagen. Wanneer suikers aanwezig waren, bleef MMA stevig in zijn bindingspocket gedurende de volledige simulatie en behield het sleutelcontacten, ook al veranderde de nabije eiwitstructuur nauwelijks. Zonder suikers ontsnapte MMA uit de pocket, schoof over het eiwitoppervlak en vormde slechts korte, oppervlakkige contacten. Voor mUNO toonde de geglycosyleerde receptor meerdere stabiele bindingsposes met frequente, langdurige contacten. In de gedeglycosyleerde receptor was de binding van mUNO zwakker en verspreid, en het peptide begon ook regio's te verkennen die normaal door suikerketens worden geblokkeerd, waardoor nieuwe, eerder verborgen interactieplaatsen zichtbaar werden.
Wat dit betekent voor ziekte en therapie
Samen laten deze resultaten zien dat de suikers die aan CD206 zitten fungeren als afstandsregelaars van zijn vorm en kleefkracht. Door bepaalde buigingen te beperken en te organiseren hoe segmenten samen bewegen, helpt glycosylering de receptor sommige liganden steviger vast te houden en andere naar voorkeursbindplaatsen te sturen, terwijl delen van het oppervlak ook worden afgeschermd. Bij ziekten zoals kanker, waar de algemene suikermotieven op eiwitten vaak veranderd zijn, kan CD206 andere vormen en bindgedragingen aannemen, wat verandert hoe immuuncellen hun omgeving waarnemen. Inzicht in deze suikergemedieerde "conformationele schakelaar" verheldert niet alleen hoe CD206 werkt, maar suggereert ook nieuwe manieren om geneesmiddelen of beeldvormingsmiddelen te ontwerpen die gebruikmaken van het veranderende landschap van de receptor in tumoren en andere pathologische omstandigheden.
Bronvermelding: Alvarez, G., Di Lella, S., Pickholz, M. et al. Deglycosylation induces a novel distal conformation in the mannose receptor CD206. Sci Rep 16, 5239 (2026). https://doi.org/10.1038/s41598-026-35240-y
Trefwoorden: mannose-receptor, eiwit-glycosylering, immuunherkenning, tumor-geassocieerde macrofagen, moleculaire dynamica