Clear Sky Science · nl
Classificatie van rectale neoplasie met kunstmatige intelligentie door endoscopische fluorescentie‑perfusieanalyse
Waarom dit belangrijk is voor patiënten en artsen
Bij mensen met grote rectale poliepen is een van de grootste vragen of de groei onschuldig is of al in kanker verandert. Tegenwoordig kunnen artsen dit vaak pas zeker weten nadat ze de hele laesie hebben verwijderd, wat kan leiden tot grotere operaties dan nodig of tot vertraging in de behandeling. Deze studie onderzoekt of een slimme beeldtechniek, gecombineerd met kunstmatige intelligentie, tijdens de ingreep verborgen kanker kan opsporen door te observeren hoe bloed door het weefsel stroomt.
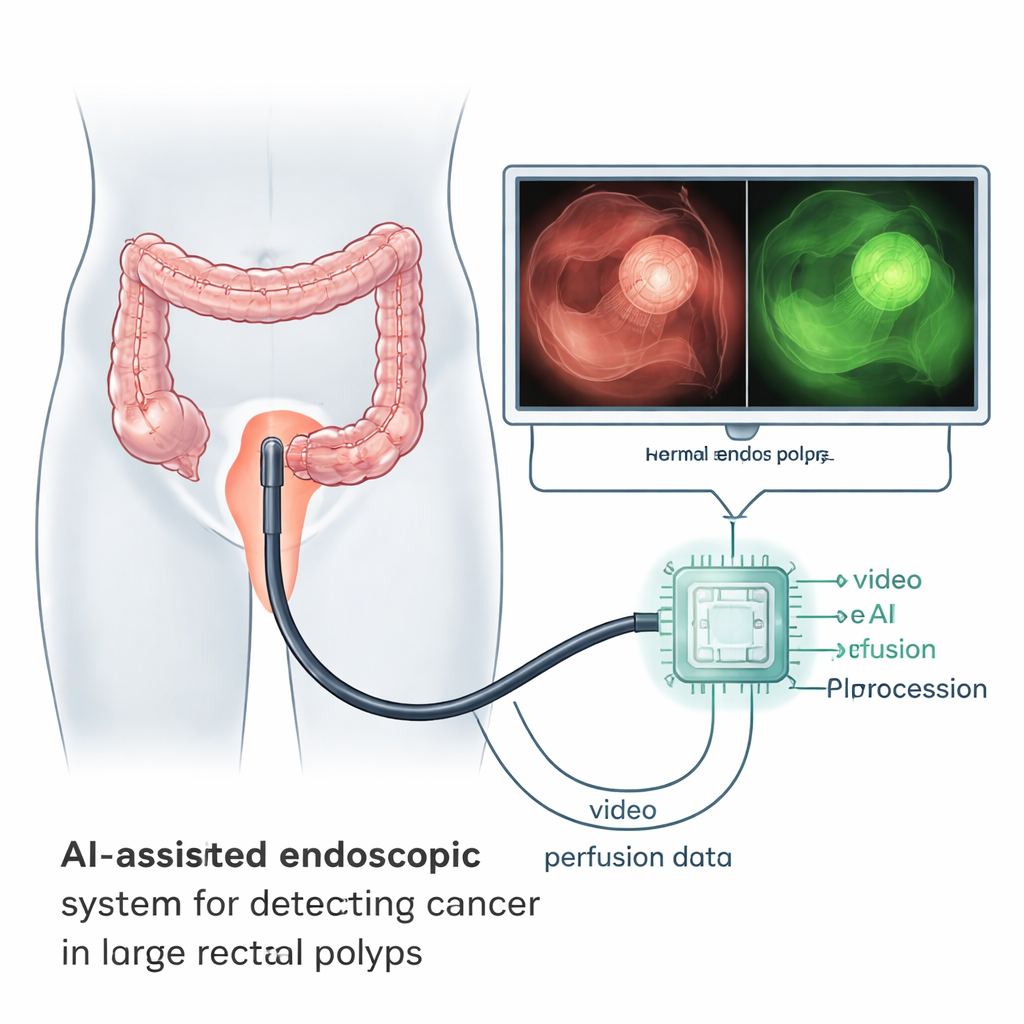
Luisteren naar hoe een tumor wordt gevoed
Kankers groeien niet zoals normaal weefsel. Ze stimuleren de vorming van nieuwe, abnormale bloedvaten die lekken en op een ongeordende manier vertakken. Deze veranderingen creëren karakteristieke patronen in hoe bloed en ingespoten kleurstoffen in- en uitwassen van een tumor. De onderzoekers gebruikten een kleurstof genaamd indocyaninegroen, die oplicht onder nabij-infrarood licht, en namen korte video’s op tijdens endoscopische ingrepen bij patiënten met grote rectale poliepen en vroegtijdige rectumkankers. Door de helderheid van de gloed over meerdere minuten te volgen, konden ze een soort “perfusie‑vingerafdruk” vastleggen voor zowel verdachte als gezonde gebieden binnen dezelfde patiënt.
Gloedpatronen omzetten in data
Elke video werd geanalyseerd met aangepaste software die het zichtbare deel van de darmwand in een raster van kleine vierkantjes verdeelde en deze over de tijd volgde, zelfs als de camera en het weefsel bewogen. Voor elk vierkantje mat het programma hoe helder de fluorescentie werd, hoe snel het piekte en hoe snel het vervaagde. Vervolgens werden deze curves geschoond en genormaliseerd zodat ze direct vergeleken konden worden. Uit deze tijdreeksen haalde het team eenvoudige numerieke kenmerken zoals het maximale signaal en de daling van het signaal op specifieke tijden na de piek. Ze onderzochten ook hoe ongelijk deze waarden waren binnen het abnormale gebied, met een statistiek die variatie binnen de tumor vergelijkt met nabijgelegen gezond weefsel.
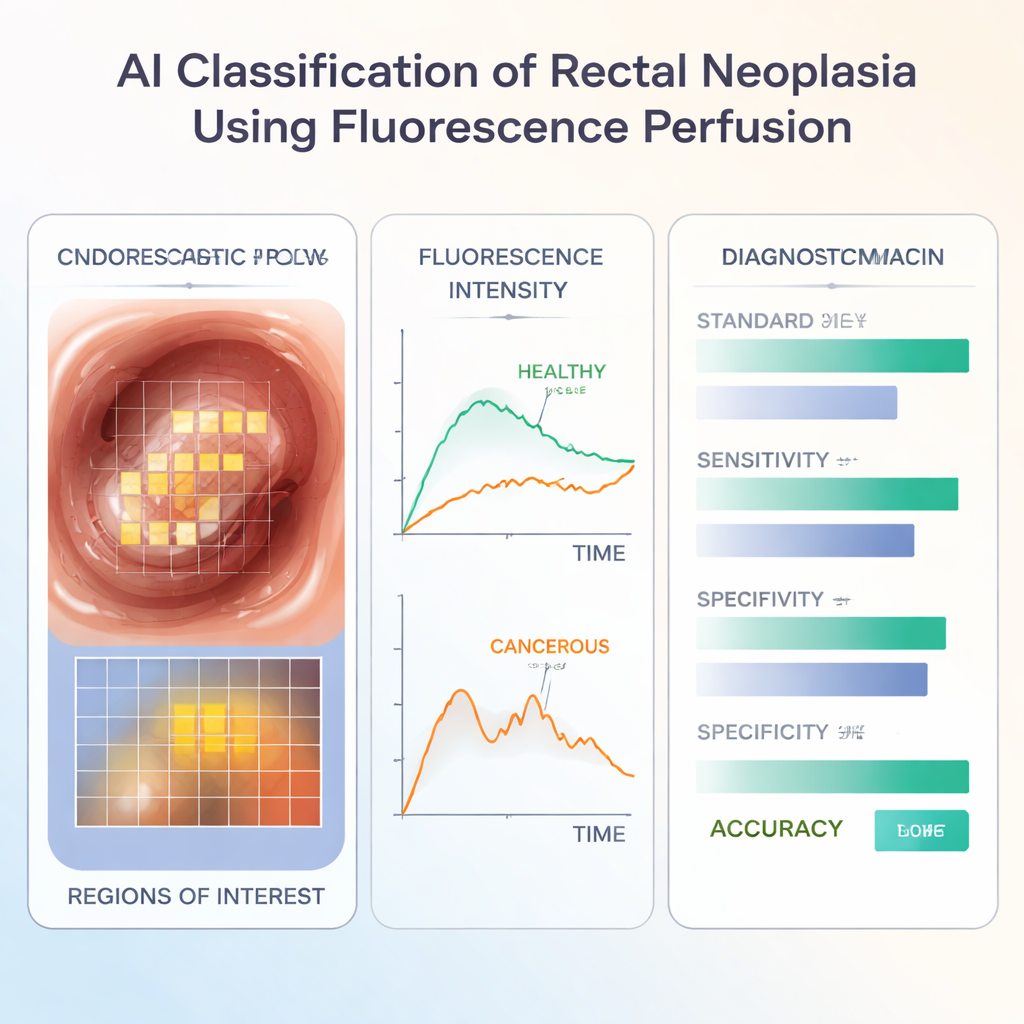
De kunstmatige intelligentie trainen
De groep bestudeerde 190 video’s van 182 patiënten behandeld in zes ziekenhuizen in vier landen; bij ongeveer drie op de vijf patiënten werd uiteindelijk kanker onder de microscoop bevestigd. Ze trainden een machine‑learningmodel (een XGBoost‑classifier) om het verschil te leren tussen goedaardige en kwaadaardige laesies uitsluitend op basis van de kleurstof‑flowkenmerken, zonder naar de normale kleurbeelden te kijken. Wanneer het model op nieuwe gevallen werd toegepast, identificeerde het kanker correct bij een substantieel merendeel van de patiënten, en presteerde het vergelijkbaar met of iets beter dan veel gangbare hulpmiddelen in de praktijk, zoals endoscopische biopsieën, preoperatieve MRI‑scans en de visuele indruk van de ervaren chirurg.
Toevoegen van klinische aanwijzingen uit de praktijk
In de dagelijkse praktijk vertrouwen artsen zelden op één enkele test. Daarom combineerden de onderzoekers de output van de AI met informatie die al beschikbaar is: MRI‑rapporten en het oordeel van de opererende chirurg. Wanneer deze in dezelfde computerpijplijn werden gevoed, verbeterde het vermogen om kanker te detecteren, vooral bij het correct uitsluiten van ziekte in goedaardige laesies. In het beste scenario detecteerde het gecombineerde systeem ongeveer 86% van de kankers en voorkwam het valse alarmen in ruwweg 71% van de niet‑kankergevallen. De aanpak werkte ook redelijk goed in subgroepen van patiënten die meer typisch zijn voor vroegtijdige, lokaal verwijderbare ziekte.
Wat dit voor toekomstige zorg zou kunnen betekenen
De studie toont aan dat kankers in grote rectale poliepen een detecteerbare handtekening achterlaten in hoe bloed en kleurstof erdoorheen stromen, en dat deze handtekening automatisch door AI kan worden opgepikt. Hoewel het werk tot nu toe is uitgevoerd op opgenomen video’s en nog bewezen moet worden in realtime klinische proeven, wijst het op een toekomst waarin een colonoscopist tijdens de ingreep gewaarschuwd kan worden dat een ogenschijnlijk onschuldige poliep waarschijnlijk een invasieve kanker verbergt. Die informatie zou kunnen helpen bij het bepalen waar te biopteren, of de laesie lokaal te verwijderen, of de patiënt door te verwijzen voor uitgebreidere chirurgie, en zo zowel gemiste kankers als onnodige grote operaties te verminderen.
Bronvermelding: Boland, P.A., MacAonghusa, P., Singaravelu, A. et al. Artificial intelligence classification of rectal neoplasia by endoscopic fluorescence perfusion analysis. Sci Rep 16, 4761 (2026). https://doi.org/10.1038/s41598-026-35233-x
Trefwoorden: rectumkanker, endoscopische beeldvorming, fluorescentie‑perfusie, kunstmatige intelligentie, machine learning