Clear Sky Science · nl
Chitosan-dextran sulfaat nanocapsules voor verbeterde werkzaamheid van tigecycline tegen non-tyfeuze Salmonella enterica
Waarom dit belangrijk is voor voedselveiligheid
De meeste mensen kennen Salmonella als een vervelende oorzaak van voedselvergiftiging, vaak gekoppeld aan onvoldoende verhit gevogelte. Minder bekend is dat sommige stammen zo resistent zijn geworden dat zelfs krachtige “laatste-redmiddel”-middelen kunnen falen. Deze studie onderzoekt een nanotechnologische aanpak om één van die middelen, tigecycline, nieuw leven in te blazen door het in piepkleine suiker-gebaseerde kapsels te verpakken die het helpen binnen te dringen in geïnfecteerde cellen en belangrijke resistentiemechanismen in Salmonella uit te schakelen.
De groeiende dreiging van hardnekkige Salmonella
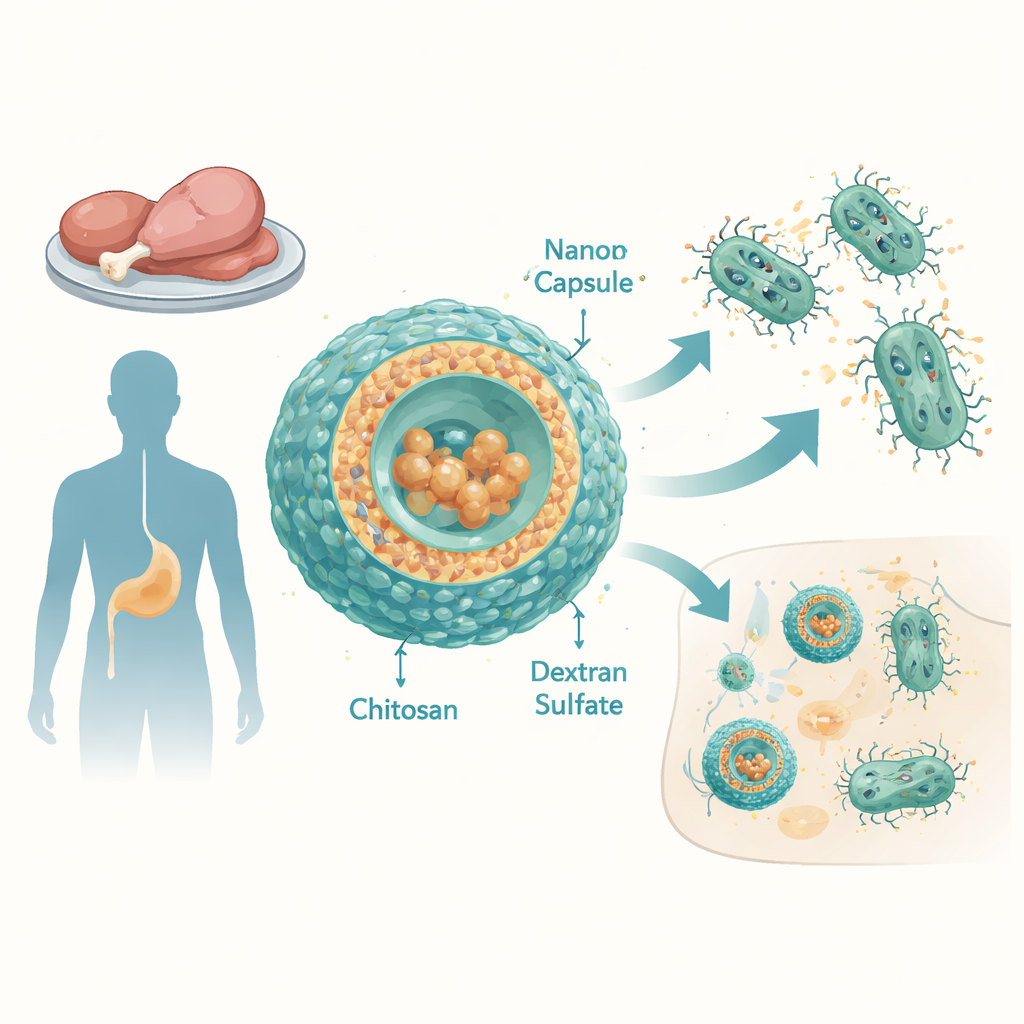
Non-tyfeuze Salmonella (NTS) serovars zijn wereldwijd een veelvoorkomende oorzaak van diarree en bloedbaaninfecties, vooral in lage- en middeninkomenslanden. De onderzoekers bestudeerden 12 Salmonella enterica-stammen afkomstig van kip- en eendenvlees in Egypte. Deze stammen waren resistent tegen veelgebruikte antibiotica, waaronder penicillines, cefalosporines, tetracyclines en anderen, en vertoonden hoge multi-antibiotica-resistentiescores. Zelfs tigecycline, een breedspectrummiddel dat wordt bewaard voor lastige gevallen, presteerde slecht: de bacteriën konden zeer hoge concentraties verdragen. Een belangrijke reden was overactieve “effluxpompen” — moleculaire machines in het bacteriële membraan die antibiotica constant weer uit de cel pompen.
Het bouwen van een slimmer geneesmiddelkapsel
Om dit te omzeilen ontwierp het team nanometerschalen capsules gemaakt van twee natuurlijk gewonnen polymeren: chitosan, gewonnen uit chitin (het materiaal in schaaldieren), en dextran sulfaat, een vertakte suikermolecuul. Door de verhoudingen van deze componenten zorgvuldig af te stemmen, produceerden ze stabiele deeltjes van ongeveer 100–150 nanometer, met een positieve oppervlakte-lading die helpt bij interactie met bacteriële en gastheercelmembraan. Tigecycline werd met opvallend hoge efficiëntie in deze deeltjes geladen — vrijwel het hele geneesmiddel belandde in de kapsels. In laboratoriumtests die voorwaarden in de bloedbaan nabootsen, gaven de kapsels het grootste deel van hun tigecycline binnen enkele uren vrij, wat suggereert dat ze een sterke piek van antibioticum op infectieplaatsen kunnen afleveren.
Bacteriële verdedigingen uitschakelen
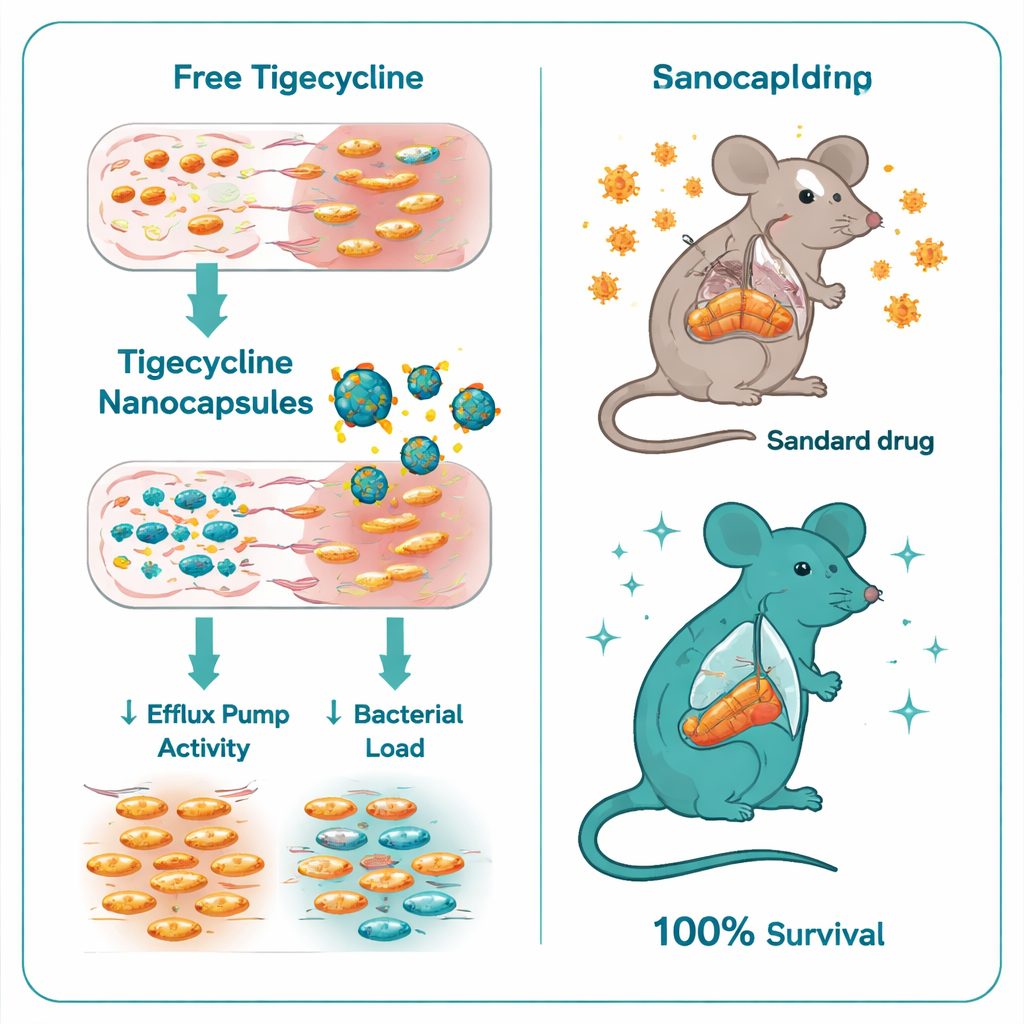
Wanneer de onderzoekers gewone tigecycline vergeleken met de tigecycline-geladen chitosan–dextran sulfaat nanocapsules, was het verschil opvallend. De minimale geneesmiddelconcentratie nodig om bacteriegroei te stoppen daalde van 32–128 microgram per milliliter voor gewone tigecycline tot slechts 0,5–1 microgram per milliliter met de nanocapsules — een zes- tot zevenvoudige verbetering. Time-kill experimenten toonden aan dat de ingekapselde vorm Salmonella veel sneller en grondiger doodde. Op genetisch niveau dempten de nanocapsules ook belangrijke resistentieregelaars: de expressie van de ramA- en acrB-genen, die helpen bij de controle en vorming van grote effluxpompen, daalde meerdere keren bij behandelde bacteriën. Met andere woorden, de kapsels leverden niet alleen meer geneesmiddel; ze hielpen ook een van de belangrijkste ontsnappingsroutes van de bacterie uit te schakelen.
Geïnfecteerde muizen beschermen tegen dodelijke ziekte
Het team testte de nieuwe formulering vervolgens in een muismodel van een ernstige Salmonella Typhimurium-infectie. Onbehandelde geïnfecteerde muizen stierven allemaal binnen acht dagen. Muizen die standaard tigecycline kregen deden het beter maar kenden nog steeds hoge sterfte, met slechts 40% overlevenden. In scherp contrast overleefde iedere muis die behandeld werd met de tigecycline-geladen nanocapsules. Deze dieren hadden veel minder bacteriën in lever en darmen, bloedwaarden die dichter bij normale lever- en nierfunctie lagen, en veel mildere weefselschade bij microscopisch onderzoek. Zelfs de “lege” chitosan–dextran sulfaat-kapsels, zonder antibioticum, boden enige bescherming, waarschijnlijk omdat chitosan zelf bescheiden antimicrobiële en ontstekingsremmende effecten heeft, maar de combinatie met tigecycline was duidelijk superieur.
Wat dit kan betekenen voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat het verpakken van een bestaand antibioticum in een slim, biocompatibel nanokapsel zijn effectiviteit tegen sterk resistente Salmonella kan herstellen. Door het geneesmiddel te helpen bereiken van bacteriën die zich schuilhouden in cellen en door de pompen die het geneesmiddel normaal wegpompen te dempen, veranderde het chitosan–dextran sulfaat-systeem een worstelend laatste-redmiddel in een zeer effectieve behandeling bij muizen, met 100% overleving. Hoewel er meer werk nodig is voordat deze aanpak bij mensen of landbouwhuisdieren kan worden toegepast, biedt het een veelbelovende weg om de bruikbare levensduur van belangrijke antibiotica te verlengen en de veiligheid van onze voedselvoorziening te verbeteren zonder helemaal nieuwe medicijnen te hoeven uitvinden.
Bronvermelding: Omar, M.R., Saeed, A.A., Malhat, S.M. et al. Chitosan-dextran sulfate nanocapsules for enhanced tigecycline efficacy against non-typhoidal Salmonella enterica. Sci Rep 16, 5016 (2026). https://doi.org/10.1038/s41598-026-35229-7
Trefwoorden: Salmonella, antibioticaresistentie, nanodeeltjes, geneesmiddelafgifte, tigecycline