Clear Sky Science · nl
Bacteriën uit voedsel en darmmicrobioom produceren methylglyoxal en dit metaboliet leidt tot de vorming van bioactieve 1-acetyl-β-carboline alkaloïden
Waarom het scheikundelab in je darm ertoe doet
In onze darmen en in veel gefermenteerde voedingsmiddelen zetten biljoenen bacteriën continu de suikers die we eten om in een reeks chemische bijproducten. Deze studie onderzoekt één zodanig pad in detail: hoe sommige veelvoorkomende bacteriën suikers omzetten in een zeer reactieve verbinding genaamd methylglyoxal, en vervolgens in een familie bioactieve moleculen genoemd 1-acetyl-β-carbolines. Omdat deze stoffen zowel met ziekteprocessen als met potentiële nieuwe geneesmiddelen worden geassocieerd, kan het begrijpen wanneer en hoe bacteriën ze maken ons beeld van voedsel, het microbioom en gezondheid veranderen.
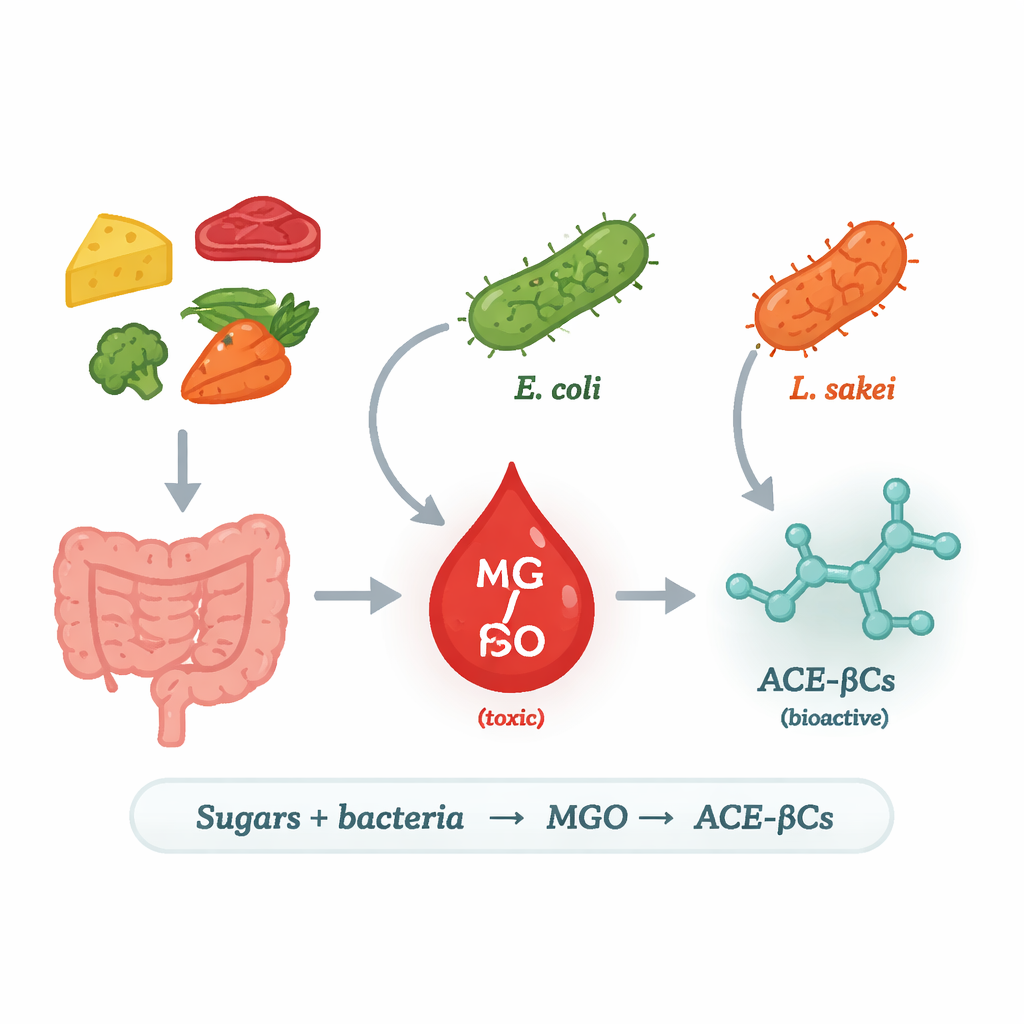
Van alledaagse suikers naar een risicovolle verbinding
De onderzoekers richtten zich op methylglyoxal (MGO), een zeer reactief, toxisch bijproduct van suikerafbraak. Bij mensen wordt overtollig MGO in verband gebracht met diabetes, hartaandoeningen en neurodegeneratie omdat het eiwitten en DNA kan beschadigen. Onze cellen houden MGO normaal gesproken onder controle met ontgiftingssystemen, maar zij zijn niet de enige bron: bacteriën kunnen MGO ook produceren. Bij sommige microben zet een enzym dat methylglyoxal synthase (MgsA) heet een tussenproduct van suikerverwerking direct om in MGO, waardoor een “kortsluiting” in de energiestofwisseling ontstaat. Het team vroeg welke voedsel- en darmbacteriën deze route gebruiken, onder welke omstandigheden, en wat er gebeurt met het MGO dat ze vrijgeven.
Wie zijn de bacteriële producenten?
Om dit te beantwoorden, kweekten de wetenschappers meerdere stammen melkzuurbacteriën die vaak in voedsel voorkomen, samen met een laboratoriummodel van Escherichia coli, in een gecontroleerd medium met ofwel glucose ofwel galactose. Ze volgden vervolgens MGO en twee verwante alkaloïden in het kweekvocht in de tijd met behulp van hoge-resolutie chromatografie en massaspectrometrie. Alleen E. coli en de vleesgeassocieerde soort Lactilactobacillus sakei produceerden noemenswaardige hoeveelheden MGO en de alkaloïden; andere geteste melkzuurbacteriën niet. Een genoomzoektocht onthulde het cruciale verschil: E. coli en L. sakei dragen het gen voor MgsA, terwijl de meeste van hun melkzuurverwanten dat niet doen. Wanneer de onderzoekers het mgsA-gen van L. sakei in een niet-producerende stam plaatsten, begon die gemodificeerde bacterie beide — MGO en de alkaloïden — te maken, waarmee MgsA duidelijk aan dit pad werd gekoppeld.
Hoe toxisch MGO bioactieve alkaloïden wordt
De volgende vraag was wat er met het MGO gebeurt zodra het gevormd is. Het team richtte zich op 1-acetyl-β-carboline alkaloïden (ACE-βCs), kleine moleculen met gerapporteerde antimicrobiële, ontstekingsremmende en antikankeractiviteiten. Ze toonden aan dat wanneer MGO-producerende bacteriën werden gekweekt in aanwezigheid van het aminozuur L-tryptofaan, de niveaus van twee ACE-βCs — 1-acetyl-β-carboline en diens 3-carboxylzuurvorm — sterk toenamen. Het toevoegen van extra MGO aan het medium versterkte eveneens hun vorming. Dit duidt erop dat MGO uit de cellen lekt en spontaan reageert met L-tryptofaan in het omringende vocht, zonder aanvullende enzymen, om deze bioactieve verbindingen te genereren. Met andere woorden: dezelfde chemie die MGO gevaarlijk maakt, zet het ook om in complexere moleculen die mogelijk nuttige effecten hebben.
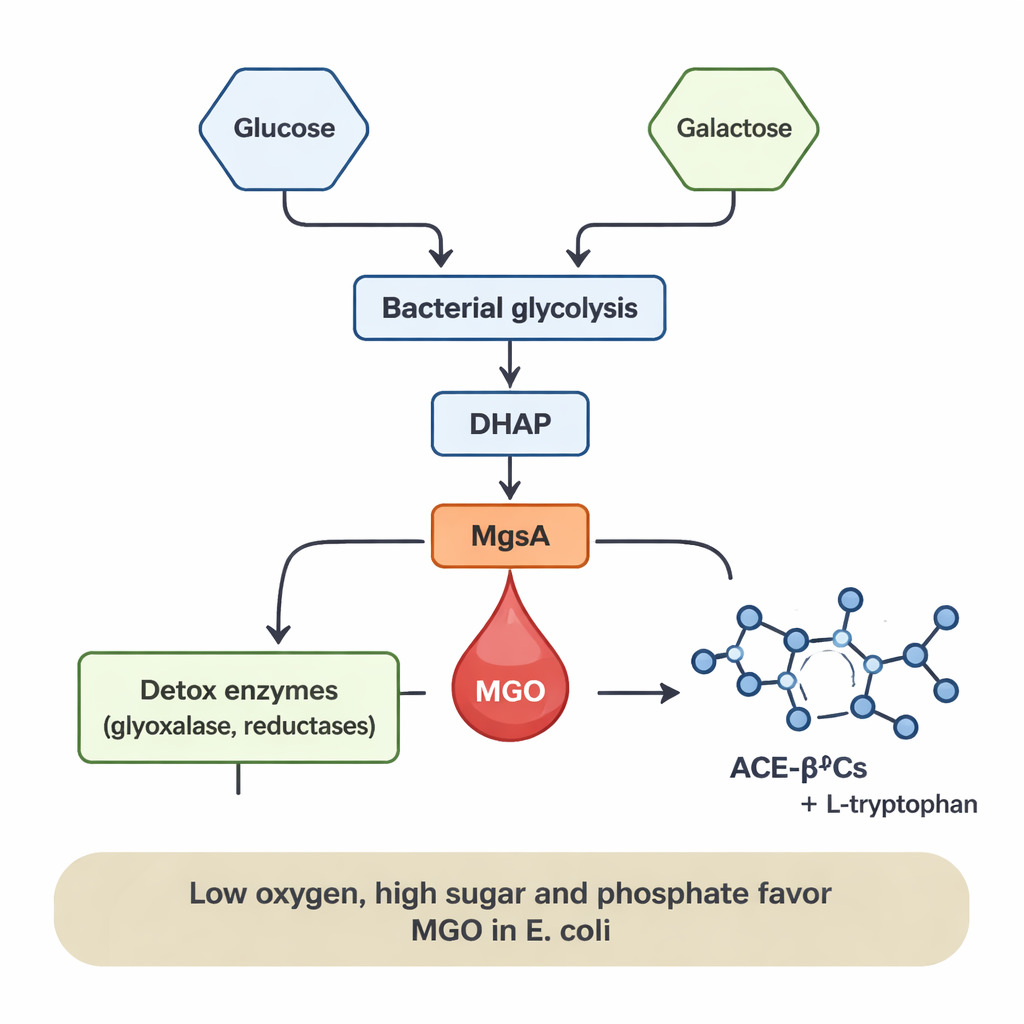
Wat de productie omhoog of omlaag zet
De MGO-productie was niet constant; ze hing sterk af van het dieet en de omgeving van de bacteriën. Bij E. coli verscheen MGO alleen wanneer glucose aanwezig was, en de niveaus stegen naarmate de glucosespiegels toenamen. Het toevoegen van fosfaat, een veelvoorkomend mineraalvoedingsstof, versterkte de MGO-vorming meerdere malen, waarschijnlijk omdat het de ophoping van gefosforyleerde suiker-tussenproducten bevordert die in de MgsA-kortsluiting terechtkomen. Lage zuurstofniveaus (anaeroob) — vergelijkbaar met die in de menselijke darm — bevorderden ook de MGO-afgifte, terwijl goed geaëreerde, zuurstofrijke omstandigheden die sterk verminderden, ondanks dat de bacteriën nog steeds goed groeiden. Ter vergelijking genereerde L. sakei voornamelijk MGO wanneer het op galactose werd gekweekt, en de productie nam toe bij hogere galactosespiegels. Deze patronen suggereren dat telkens wanneer de suikerdoorstroming door de bacteriële stofwisseling hoog is en zuurstof beperkt is, MGO kan fungeren als een “drukventiel” dat de spanning van ophopende suiker-tussenproducten verlicht.
Wat dit kan betekenen voor voedsel en gezondheid
De bevindingen suggereren dat niet alle darm- of voedselbacteriën gelijk zijn in hun vermogen om MGO en ACE-βCs te maken. Soorten die het MgsA-enzym dragen, zoals bepaalde L. sakei-stammen en E. coli, kunnen belangrijke bijdragers zijn, vooral in suikerrijke, zuurstofarme omgevingen zoals de darm of sommige fermentaties. Het MGO dat ze uitscheiden kan bijdragen aan de totale chemische belasting van gastweefsels, maar de omzetting ervan in ACE-βC-alkaloïden kan dit reactieve verbinding deels “opvegen” terwijl er tegelijkertijd moleculen met eigen biologische effecten ontstaan. Hoewel deze studie in laboratoriumculturen is uitgevoerd, belicht ze een plausibele route waarbij dieet, microbiotasamenstelling en bacteriële stofwisseling samen de balans tussen schadelijke en mogelijk gunstige chemicaliën in ons lichaam vormgeven, en ze wijst op ACE-βCs als mogelijke merkers van bacteriële MGO-productie in voedsel en de darm.
Bronvermelding: Herraiz, T., Sánchez-Arroyo, A., de las Rivas, B. et al. Bacteria from foods and gut microbiota produce methylglyoxal and this metabolite leads to the formation of bioactive 1-acetyl-β-carboline alkaloids. Sci Rep 16, 4905 (2026). https://doi.org/10.1038/s41598-026-35162-9
Trefwoorden: darmmicrobioom, methylglyoxal, bacteriële stofwisseling, voedingsfermentatie, beta-carboline alkaloïden