Clear Sky Science · nl
Afleiding van een intrinsieke biomarker voor hersenactiviteit voor de vroegste voorspelling van cognitieve achteruitgang
Waarom vroege veranderingen in de hersenen ertoe doen
Veel oudere volwassenen merken subtiele geheugenproblemen op lang voordat een arts dementie kan vaststellen. In dit stadium lijken standaardhersenfoto’s en bloedtesten vaak normaal, terwijl het onderliggende ziekteproces mogelijk al gestart is. Deze studie onderzoekt of een eenvoudige, niet-invasieve hersengolventest — het elektro-encefalogram (EEG) — zeer vroege veranderingen in hersenfunctie kan blootleggen en betrouwbaar kan voorspellen wie vele jaren later waarschijnlijk ernstige cognitieve achteruitgang zal ervaren.
Luisteren naar de stille signalen van de hersenen
De onderzoekers richtten zich op mensen met “subjectieve cognitieve achteruitgang” (SCA): oudere volwassenen die het gevoel hebben dat hun geheugen achteruitgaat maar nog normaal presteren op standaardtests. Achtentachtig van zulke vrijwilligers, tussen 52 en 85 jaar, ondergingen 20 minuten rust-EEG met gesloten ogen en werden vervolgens 5–7 jaar gevolgd. Tijdens de follow-up hielden artsen de cognitieve toestand van elke persoon bij met gevestigde beoordelingsschalen. Tegen het einde van deze periode bleven sommige deelnemers stabiel, terwijl anderen verslechterden tot milde cognitieve stoornis of dementie ontwikkelden. Deze uitkomsten stelden het team in staat te onderzoeken of subtiele patronen in het oorspronkelijke EEG hadden kunnen voorspellen wie later achteruit zou gaan.
Hersengolven omzetten in een voorspellende vingerafdruk
In plaats van het EEG visueel te inspecteren, gebruikte het team kwantitatief EEG (qEEG), dat ruwe hersengolven omzet in duizenden numerieke kenmerken. Deze kenmerken vatten samen hoe sterk verschillende frequentiebanden zijn (zoals alfa- en theta-ritmes), hoe goed verre hersengebieden met elkaar synchroniseren (connectiviteit en faseverschuiving), en hoe complex of gedesorganiseerd het algemene activiteitspatroon lijkt. Omdat normaal verouderen ook het EEG verandert, corrigeerden de onderzoekers alle kenmerken wiskundig voor leeftijd en standaardiseerden ze vervolgens zodat “nul” de verwachte waarde voor een gezond persoon van dezelfde leeftijd vertegenwoordigt. Om overfitting te voorkomen, beperkte men systematisch meer dan 6.000 kandidaat-maatregelen tot een compacte set die stabiel, niet-redundant en het beste in staat was om mensen die stabiel zouden blijven te scheiden van degenen die zouden verslechteren.
Machine learning als een kristallen bol
Met deze gereduceerde set kenmerken trainde het team verschillende machine-learningmodellen — logistieke regressie, support vector machines en random forests — om de kans van elke deelnemer op toekomstige achteruitgang te schatten. Herhaalde cross-validatie en een gespecialiseerde bootstrap-methode werden gebruikt om de prestatie zo realistisch mogelijk te beoordelen. Over de modellen heen lag de voorspellingsnauwkeurigheid rond 80%, met een area under the receiver operating characteristic curve (AUC) van ongeveer 0,90, wat duidt op sterke discriminatie tussen stabiele en verslechterende individuen. De uiteindelijke vergrendelde modellen gebruikten slechts 14 qEEG-kenmerken, grotendeels afkomstig uit frontale hersengebieden die met een kleine set elektroden waren opgenomen, waardoor de aanpak praktisch toepasbaar is voor routinematig klinisch gebruik.
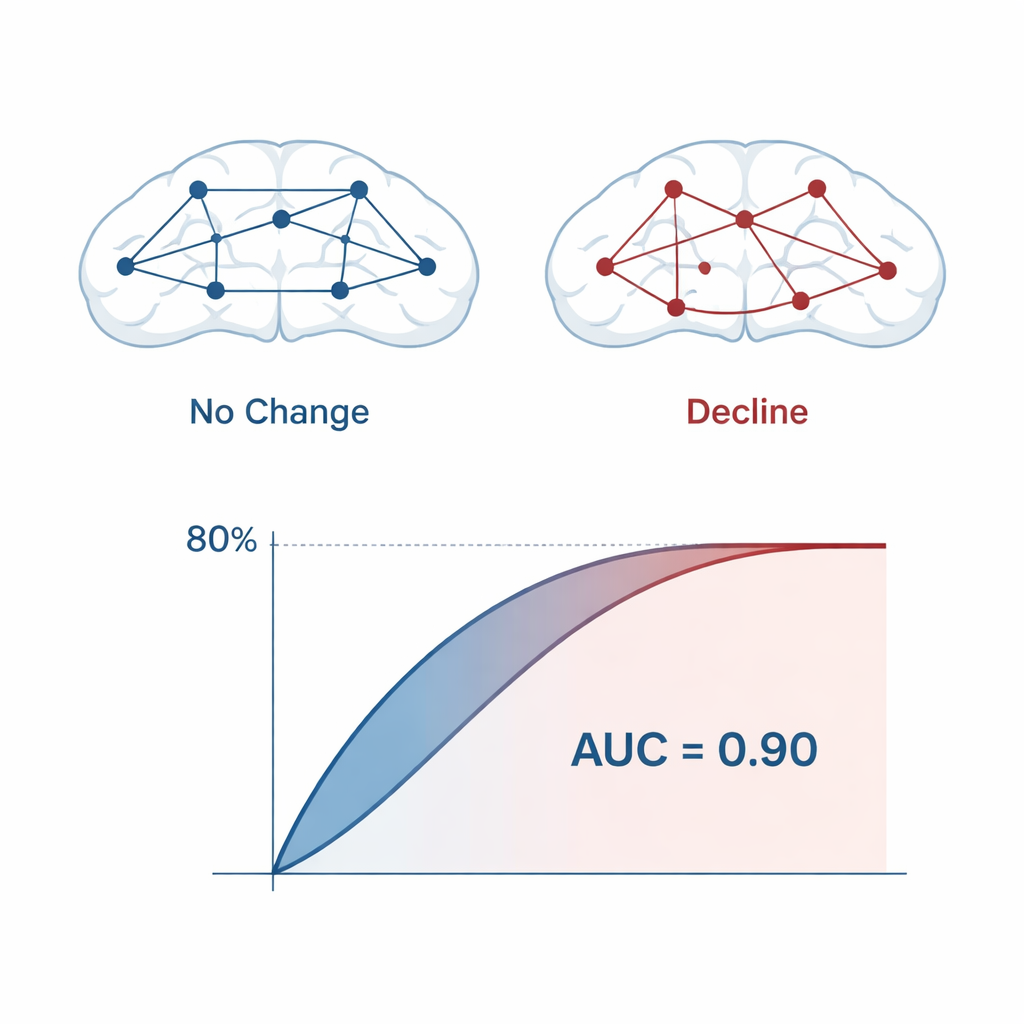
Wat er verandert in de hersenen
De kenmerken die het meest verantwoordelijk waren voor accurate voorspelling wezen op vroege verstoring in hoe hersengebieden met elkaar communiceren. Maten van connectiviteit, vooral faseverschuiving en asymmetrie tussen linker- en rechterfrontale regio’s, waren cruciaal voor het model. Afwijkingen in de alfa- en theta-frequentiebanden vielen op: verhoogde of verschoven theta-activiteit is in ander onderzoek gekoppeld aan hippocampale atrofie en cortexverdunning, terwijl veranderingen in alfa-vermogen en -frequentie mogelijk de eerste compensatiepogingen van de hersenen voor opkomende schade weerspiegelen. Belangrijk is dat geen enkele EEG-maat op zichzelf het hele verhaal kon vertellen. Het was de specifieke combinatie — de biomarker-”vingerafdruk” — die een verhoogd risico aangaf jaren voordat volledige symptomen verschenen.
Het instrument testen in de echte wereld
Om te zien of hun biomarker buiten de oorspronkelijke groep generaliseert, testten de onderzoekers deze op twee onafhankelijke cohorten uit de Verenigde Staten en Italië, elk met hun eigen opnameopstellingen en patiëntkenmerken. Zoals te verwachten bij echt nieuwe data daalde de nauwkeurigheid bescheiden, naar ongeveer 60–70%, maar het model presteerde nog steeds veel beter dan toeval, wat suggereert dat het signaal dat het vastlegt robuust is. Het team toonde ook aan dat clinici de beslissingsdrempel kunnen aanpassen: deze verlagen verhoogt de sensitiviteit (meer toekomstige decliners detecteren ten koste van meer valse alarmen), terwijl deze verhogen de specificiteit vergroot (minder false positives maar meer gemiste gevallen). Deze flexibiliteit stelt zorgverleners in staat het hulpmiddel af te stemmen op verschillende klinische prioriteiten.
Wat dit betekent voor patiënten en clinici
In eenvoudige bewoordingen suggereert dit werk dat een korte, pijnloze EEG-opname — met slechts een handvol elektroden boven het voorhoofd — kan helpen oudere volwassenen te identificeren die er vandaag normaal uitzien maar een hoog risico lopen op cognitieve achteruitgang in de komende jaren. Hoewel grotere studies en vergelijkingen met andere biomarkers nog nodig zijn, is de aanpak goedkoop, niet-invasief en herhaalbaar, wat het aantrekkelijk maakt voor brede screening, vooral in situaties waar geavanceerde beeldvorming of ruggenmergvochtonderzoeken onpraktisch zijn. Wanneer verder gevalideerd, zouden zulke EEG-gebaseerde biomarkers artsen kunnen helpen vroeger in te grijpen, ziekteprogressie te monitoren en deelnemers te selecteren voor klinische proeven in het stadium waarin behandelingen het meest kansrijk zijn om blijvende effecten te bereiken.
Bronvermelding: Prichep, L.S., Zaidi, S.N., Brink, K. et al. Derivation of an intrinsic brain activity biomarker for the earliest prediction of cognitive decline. Sci Rep 16, 5500 (2026). https://doi.org/10.1038/s41598-026-35144-x
Trefwoorden: vroegtijdige dementievoorspelling, EEG-hersengolven, subjectieve cognitieve achteruitgang, machine learning-biomarker, Alzheimer-risico