Clear Sky Science · nl
Ontwerp- en prestatieanalyse van een verticaal gestapelde gate-all-around nanosheet FET met ingebedde nanokamer voor biosensor toepassingen
Kleinere sensoren voor eerdere waarschuwingen
Het vroegtijdig opsporen van kanker hangt vaak af van hoe snel en nauwkeurig we zeer kleine sporen van ziekte in bloed of andere lichaamsvloeistoffen kunnen detecteren. Dit artikel onderzoekt een nieuw type ultrasensor — gebouwd met dezelfde technologie die in geavanceerde computerchips wordt gebruikt — die kankerverbandige moleculen met veel hogere gevoeligheid kan detecteren dan veel bestaande apparaten, terwijl hij zeer weinig vermogen verbruikt.
Een transistor als kankerdetector
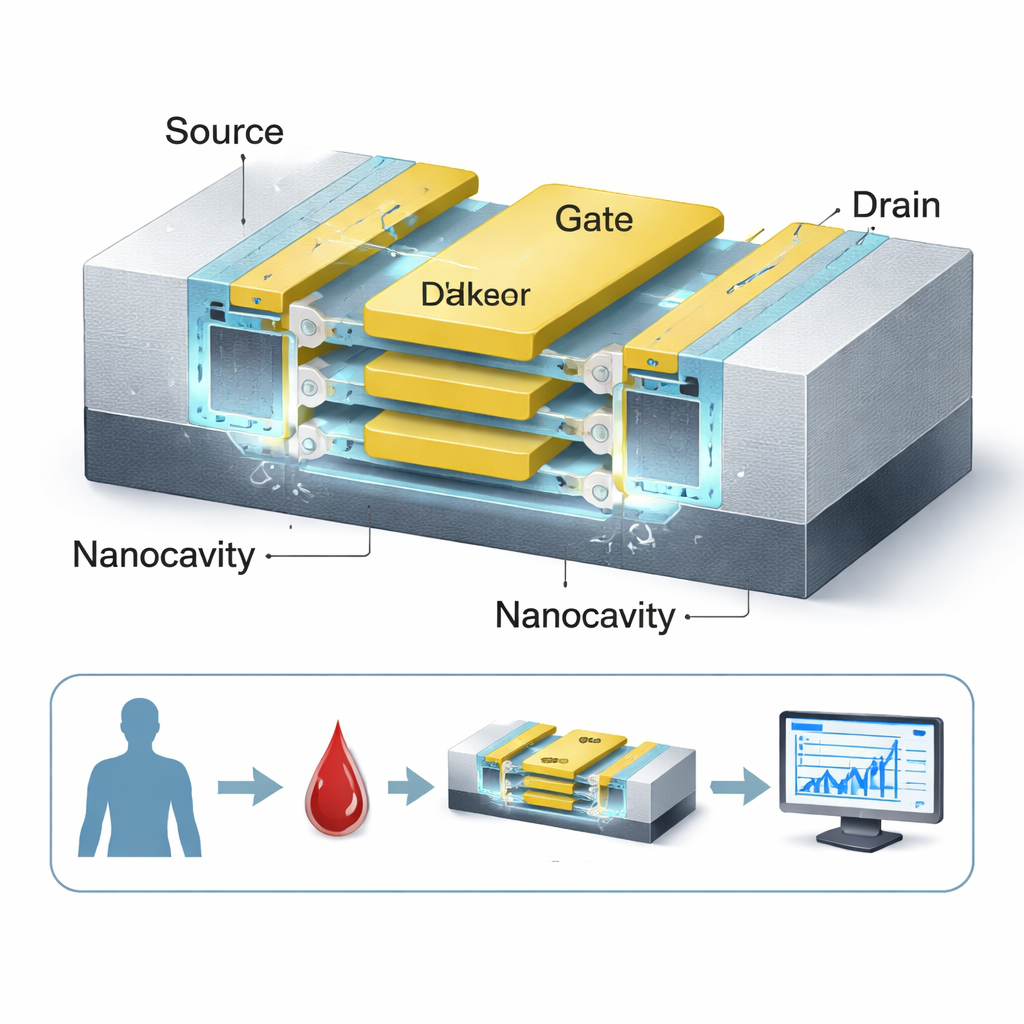
Centraal in het werk staat een herontworpen transistor, het basiselement voor schakelen in de elektronica. De auteurs vertrekken van een geavanceerd type apparaat dat een nanosheet FET wordt genoemd en dat al door grote chipfabrikanten wordt toegepast voor 3 nm‑processors. Ze herbestemmen het als biosensor door kleine holle ruimten, of nanokamers, rond het geïsoleerde gate‑elektrode dat de stroom regelt, uit te frezen. Wanneer kankerverwante biomoleculen — zoals cellen van colorectale of niertumoren, DNA‑strengen of gelatineachtige eiwitten — zich in deze kamers nestelen, veranderen ze subtiel hoe elektrische lading zich in het apparaat gedraagt. De transistor ‘voelt’ deze verandering als een verschuiving in de stroom, en zet zo een biochemische gebeurtenis om in een elektrisch signaal dat gemeten kan worden.
Laagstapeling voor sterkere signalen
Een belangrijk ontwerpprincipe is dat het sensor‑kanaal geen enkele draad is maar drie ultrasmalle silicium‑lagen die verticaal zijn gestapeld en allemaal door een gemeenschappelijke gate worden omsloten. Deze gate‑all‑around‑structuur geeft de gate veel strakkere controle over het kanaal dan bij traditionele vlakke transistors, wat de aan/uit‑schakeling verscherpt en de meetbare verandering vergroot wanneer biomoleculen aanwezig zijn. Twee nanokamers zijn gepositioneerd aan weerszijden van een high‑k isolatielaag (HfO₂), waardoor het gebied waar moleculen kunnen interacteren met het elektrische veld wordt gemaximaliseerd. Omdat het kanaal ‘doping‑loos’ is — het vermijdt zware chemische onzuiverheden — is de respons van de sensor uniformer en minder kwetsbaar voor variaties in de fabricage, wat een voordeel is voor betrouwbare medische tests.
Fijnstemmen van kleine kamers voor maximale respons
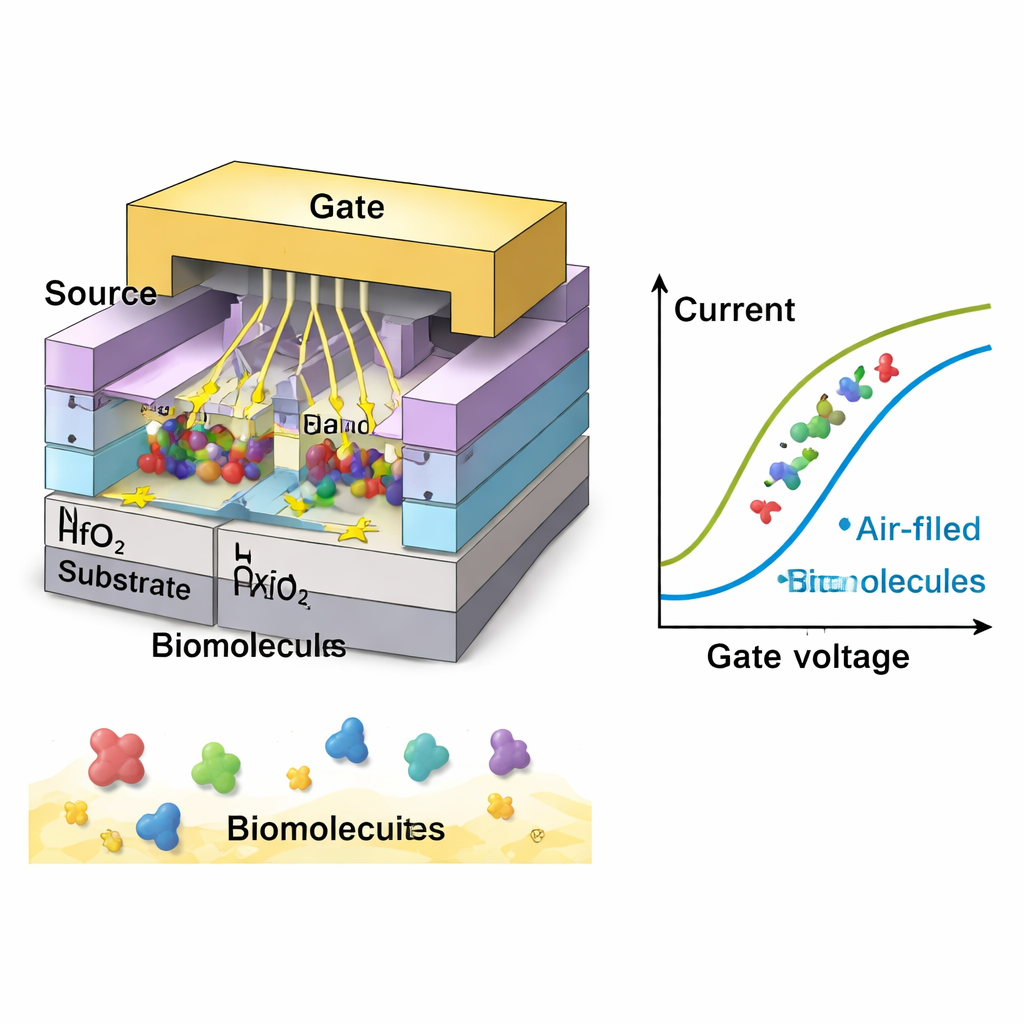
Met behulp van gedetailleerde computersimulaties (TCAD) passen de onderzoekers systematisch de geometrie van de kamers aan: hun lengte, dikte en hoe vol ze met moleculen zitten. Kortere en dunnere kamers brengen de gate en het kanaal dichter in elektrostatisch contact, verhogen de aan‑stroom en verlagen de zogeheten subthreshold swing — een maat voor hoe scherp het apparaat inschakelt. In hun optimale ontwerp bereikt de sensor een opmerkelijk lage swing van ongeveer 28 millivolt per decade, ruim onder de 60 mV/dec‑limiet van standaardtransistors. Dit betekent dat het apparaat sterk reageert op zeer kleine spanningsveranderingen, een cruciale eigenschap om lage concentraties biomoleculen te detecteren. Ze laten ook zien dat naarmate meer van het kamervolume wordt ingenomen — of naarmate moleculen dichter bij het punt komen waar de stroom begint — het signaal sterker wordt, wat verduidelijkt hoe dichtheid en plaatsing van doelmoleculen de prestatie beïnvloeden.
Kankerclues aflezen in elektrische signalen
Het team onderzoekt vervolgens hoe verschillende typen biomoleculen er elektrisch uitzien. Neutrale soorten met een hogere intrinsieke permittiviteit (een elektrische eigenschap die verband houdt met hun polarisatie in een veld) leiden tot grotere stroomveranderingen en betere gevoeligheid, met de sterkste respons bij een waarde die typisch is voor gelatine en sommige dichte biologische weefsels. Gelijksoortig geladen moleculen, zoals DNA of bepaalde celoppervlakken, kunnen het signaal nog meer versterken. In de simulaties geven negatief geladen biomoleculen de grootste stroomverschuiving, gevolgd door positieve ladingen en dan neutrale deeltjes. Onder optimale omstandigheden bereikt het apparaat een stroomgevoeligheid die meer dan 3.000 keer hoger is dan de nulwaarde en meer dan 9.000 voor sterk negatieve ladingen — beter presterend dan meerdere eerdere nanosheet‑gebaseerde biosensoren. De sensor vertoont ook snelle responstijden, stabiele werking rond kamertemperatuur en goede specificiteit, wat betekent dat hij doelmoleculen kan onderscheiden van vergelijkbare maar ongewenste soorten.
Op weg naar praktische, chip‑niveau kankertests
Om te garanderen dat dit concept realistisch is, schetsen de auteurs een fabricageproces dat nauw aansluit bij de huidige geavanceerde chipproductie, met gebruik van standaard silicon‑on‑insulator wafers, bekende oxide‑ en metallaagjes en gangbare etsstappen om de nanokamers te vormen. Omdat de structuur compact blijft en compatibel is met mainstream CMOS‑processen, zou ze in principe geïntegreerd kunnen worden in dichte arrays op één enkele chip. Voor een niet‑specialistische lezer is de conclusie dat dit werk transistor‑gebaseerde biosensoren dichter bij praktische lab‑on‑a‑chip‑apparaten brengt die mogelijk op een dag snel kunnen screenen op kankermarkers, met hoge gevoeligheid en zonder labels of complexe chemie, gebruikmakend van technologie die sterk lijkt op die waarin moderne elektronica al voorziet.
Bronvermelding: Prasanna, R.L., Karumuri, S.R., Sreenivasulu, V.B. et al. Design and performance analysis of a vertically stacked gate-all-around nanosheet FET with embedded nanocavity for biosensing applications. Sci Rep 16, 5508 (2026). https://doi.org/10.1038/s41598-026-35132-1
Trefwoorden: kanker‑biosensor, nanosheet FET, lab-on-a-chip, nanokamer sensor, vroege detectie