Clear Sky Science · nl
Melkzuur reguleert de YTHDF2-FTH1-as om ferroptose van cardiomyocyten te bevorderen en myocardiale ischemie-reperfusie schade te verergeren
Waarom hartpatiënten om deze chemie zouden moeten geven
Wanneer artsen na een hartaanval een afgesloten kransslagader weer openen, redt de toestroom van vers bloed spierweefsel maar kan ook extra schade veroorzaken, bekend als ischemie–reperfusie schade. Deze studie legt een onverwachte boosdoener in hartcellen bloot: het veelvoorkomende stofwisselingsbijproduct melkzuur. De auteurs tonen aan dat melkzuur een moleculaire schakel kan omzetten die hartcellen richting een specifiek type ijzergemedieerde celdood drijft, waardoor de schade verergert. Inzicht in deze verborgen route kan wijzen op nieuwe medicijnen die het hart beter beschermen tijdens noodbehandeling.
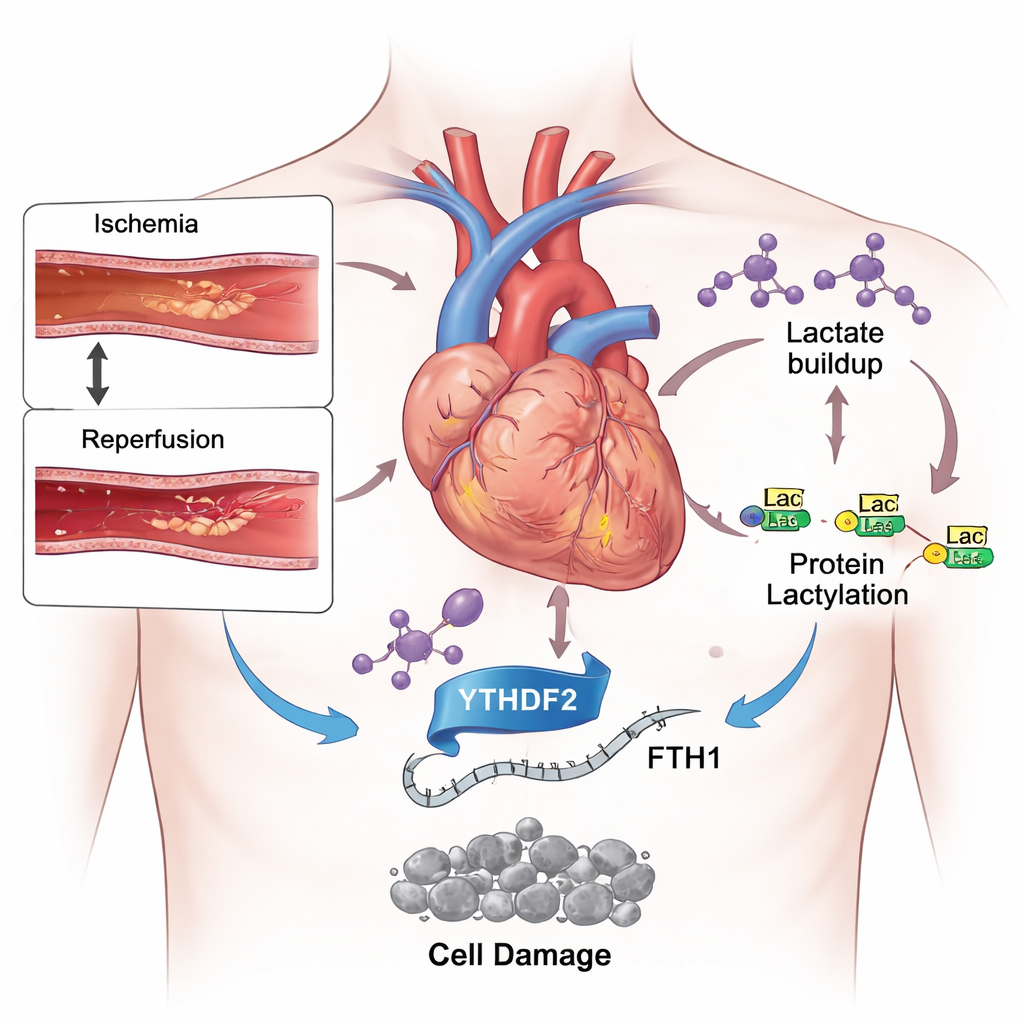
Een tweesnijdend zwaard bij de behandeling van een hartaanval
De moderne geneeskunde is erg bedreven geraakt in het snel weer openen van verstopte kransslagaders, waardoor de initiële schade van een hartaanval wordt beperkt. Toch kunnen patiënten nog steeds grote delen van hartspier verliezen nadat de bloedstroom is hersteld. Een reden is dat de plotselinge terugkeer van zuurstof en voedingsstoffen een storm van chemische stress in hartcellen veroorzaakt. Onder de verschillende typen celdood die in deze situatie worden geactiveerd, heeft een relatief nieuw type, ferroptose, veel aandacht gekregen. In tegenstelling tot meer bekende vormen zoals apoptose, hangt ferroptose af van ijzer en ongeremde oxidatie van vetten in celmembranen, wat het hart blijvend kan verzwakken.
Hoe melkzuur meer wordt dan alleen 'spierverbranding'
Tijdens een hartaanval schakelt de verhongerde hartspier zijn brandstofgebruik om naar glycolyse, een noodsysteem dat snel suiker afbreekt maar grote hoeveelheden melkzuur produceert. Met muismodellen die aan een korte afsluiting en heropening van een kransslagader werden blootgesteld, en met gekweekte hartachtige cellen die aan lage zuurstof en daarna reoxygenering werden blootgesteld, vonden de onderzoekers sterk verhoogde melkzuurniveaus. Tegelijkertijd detecteerden ze meer van een chemische markering genaamd lactylatie op veel eiwitten en op histonen, de steigers die DNA ordenen. Wanneer ze dieren een middel gaven dat glycolyse vertraagt en de melkzuurproductie vermindert, verminderde de hartschade, daalden bloedmarkers voor beschadiging en verbeterde de balans tussen schadelijk ijzer en beschermende antioxidanten. Deze resultaten suggereren dat overtollig melkzuur niet slechts een bijproduct van stress is, maar een actieve veroorzaker van schade.
Een moleculaire schakel die de teugel van ijzer versoepelt
Dieper gravend richtte het team zich op YTHDF2, een eiwit dat chemische labels op RNA leest en beslist hoe snel bepaalde boodschappen worden afgebroken. Ze ontdekten dat ischemie–reperfusie en toegevoegde melkzuur beide YTHDF2-niveaus verhoogden en de lactylatie rond het gen dat het codeert vergrootten, waardoor de productie ervan werd versterkt. Een van de belangrijkste doelwitten van YTHDF2 bleek het RNA voor ferritine heavy chain 1 (FTH1) te zijn, een kerncomponent van de ijzeropslagkooi van de cel. FTH1 bergt ijzer normaal gesproken veilig op en voorkomt dat het schadelijke reacties aanwakkert. In gestressde hartcellen bond YTHDF2 sterker aan FTH1-RNA en versnelde het de afbraak daarvan, waardoor cellen minder ferritinekooitjes overhielden, meer vrij ijzer hadden, de oxidatieve stress toenam en typische tekenen van ferroptose verschenen.
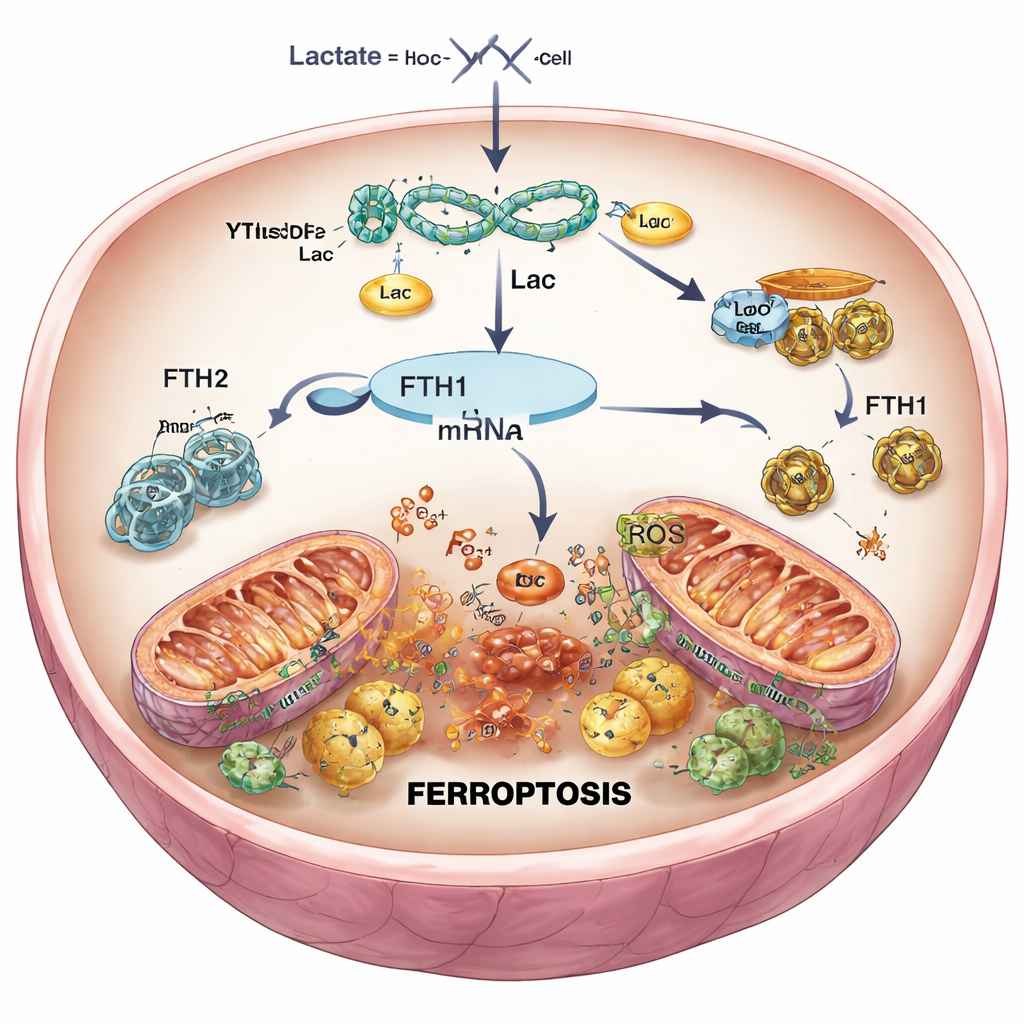
Het doodsignaal in hartcellen dempen
Om oorzaak en gevolg te testen, gebruikten de onderzoekers genetische middelen om YTHDF2 selectief te verminderen in hartcellen en in muizen. Wanneer YTHDF2 werd uitgezet, herstelden FTH1-niveaus zich, daalden ijzer en reactieve zuurstofsoorten, behielden mitochondriën een normalere vorm en verbeterde de algehele celsurvival na gesimuleerde reperfusie. Bij muizen resulteerde minder YTHDF2 in kleinere infarctlittekens en gezonder uitziend weefsel. Echter, toen FTH1 gelijktijdig werd verminderd, verdwenen deze voordelen grotendeels: ijzer steeg weer, oxidatieve schade keerde terug en de infarctgrootte nam toe. Dit bevestigde dat YTHDF2 ferroptose voornamelijk bevordert door FTH1 te onderdrukken, waardoor de controle over ijzer in hartcellen verslapt.
Wat dit betekent voor toekomstige harttherapieën
Samengevoegd schetst de studie een nieuwe keten van gebeurtenissen: een afgesloten en vervolgens heropende ader veroorzaakt melkzuuropbouw; melkzuur verhoogt YTHDF2 via lactylatie; YTHDF2 vernietigt vervolgens de RNA-instructies voor het ijzerbewakende eiwit FTH1; en de resulterende ijzerstapeling triggert ferroptose, waardoor hartschade verdiept. Voor patiënten is de boodschap hoopgevend: deze route biedt meerdere nieuwe aangrijpingspunten voor interventie. Geneesmiddelen die schadelijke melkzuursignalering beperken, de specifieke modificatie van YTHDF2 blokkeren of FTH1-functie behouden, zouden reperfusie in noodgevallen veiliger kunnen maken en meer hartspier kunnen beschermen. Hoewel deze bevindingen nog bevestigd moeten worden in menselijk weefsel, openen ze een veelbelovende weg naar zachtere, effectievere behandelingen voor overlevenden van een hartaanval.
Bronvermelding: Xiang, Z., Xiang, B., Ouyang, T. et al. Lactate regulates the YTHDF2-FTH1 axis to promote cardiomyocyte ferroptosis and aggravate myocardial ischemia-reperfusion injury. Sci Rep 16, 4865 (2026). https://doi.org/10.1038/s41598-026-35130-3
Trefwoorden: hartaanval, melkzuur, ijzergemedieerde celdood, ischemie-reperfusie schade, bescherming van cardiomyocyten