Clear Sky Science · nl
Het sequentieel gebruik van wegwerpproducten in IVF veroorzaakt geen cumulatieve toxiciteit, tenzij een defect apparaat de hele procedure aantast
Waarom alledaagse labinstrumenten belangrijk zijn voor het maken van baby’s
De meeste mensen denken bij in vitro fertilisatie (IVF) aan hormonen, eicelpunctie en embryoselectie. Weinig mensen realiseren zich dat succes ook afhangt van de tientallen plastic items — buisjes, schaaltjes, rietjes en katheters — die eicellen, zaadcellen en embryo’s tijdens het proces aanraken. Deze studie stelt een eenvoudige maar belangrijke vraag: wanneer al deze wegwerpartikelen na elkaar worden gebruikt in een normaal IVF‑traject, stapelen hun kleine chemische lekkages zich dan op en schaden ze embryo’s, of is het gevaar vooral terug te voeren op zelden opgemerkte defecte apparaten?
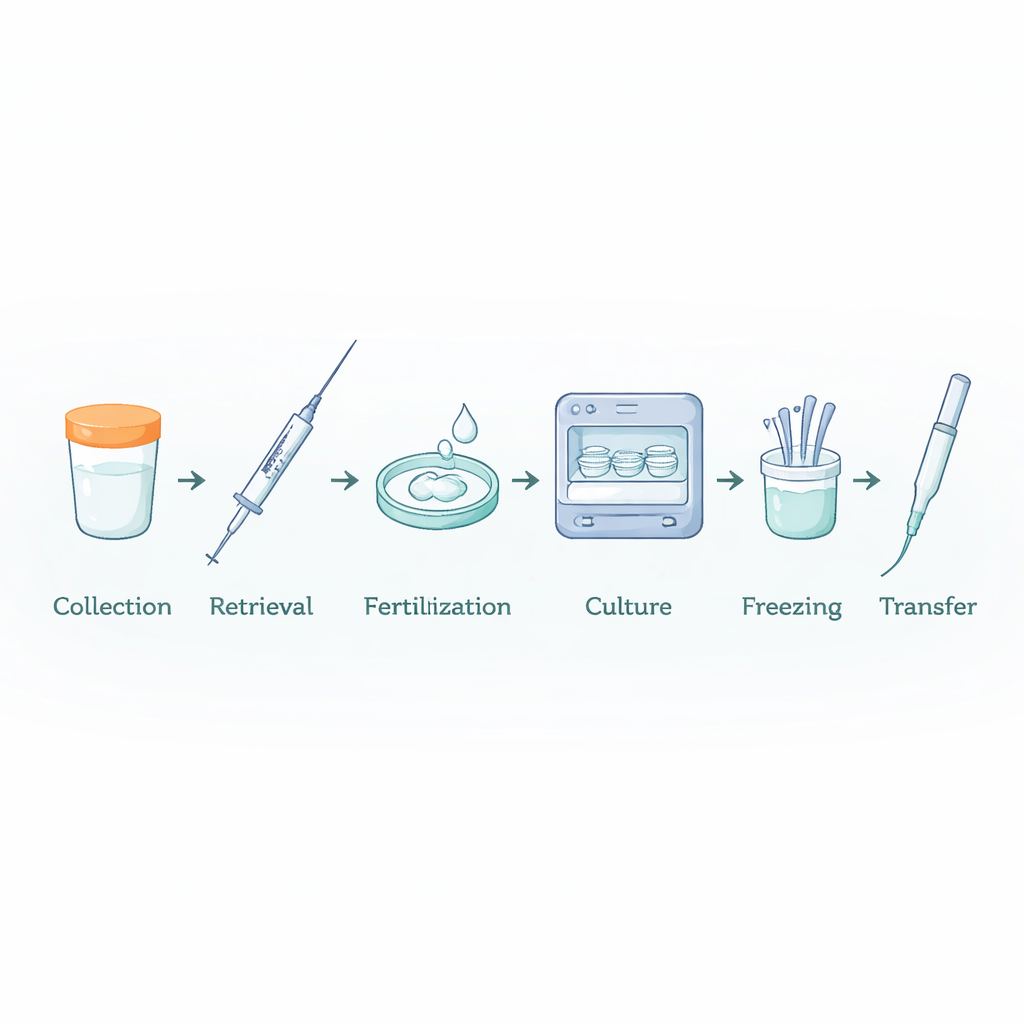
De verborgen chemie rond IVF‑embryo’s
Moderne IVF probeert het menselijk lichaam zo nauwkeurig mogelijk na te bootsen door temperatuur, zuurgraad en zuurstofniveaus te controleren zodat embryo’s veilig kunnen groeien. Toch berust elke stap op plastic verbruiksartikelen die kleine hoeveelheden chemische stoffen in het omringende medium kunnen afgeven. Deze stoffen kunnen afkomstig zijn van het plastic zelf, van additieven die flexibiliteit of transparantie verbeteren, of van residuen die tijdens fabricage en sterilisatie achterblijven. Eerder onderzoek toonde aan dat sommige combinaties van hulpmiddelen samen de zaadkwaliteit kunnen verminderen, wat de bezorgdheid vergroot dat embryo’s — mogelijk nog kwetsbaarder — ook zouden kunnen lijden onder ophoping van verontreinigingen gedurende een volledige IVF‑procedure.
IVF‑apparatuur in een muisveiligheidstest
Om dit te onderzoeken, reconstrueerden de onderzoekers tien typische IVF‑"trajecten", van spermaverzameling en -voorbereiding tot bevruchting, embryocultuur, invriezen, ontdooien en transfer. Elk traject gebruikte 7 tot 25 verschillende wegwerpartikelen in dezelfde volgorde en onder dezelfde tijden en temperaturen als in echte klinieken. In plaats van menselijke embryo’s bloot te stellen, leidden ze kweekmedium door de apparaten en gebruikten dat medium vervolgens om muisembryo’s te laten groeien in een standaard veiligheidstest, de Mouse Embryo Assay. Verse, bevruchte muizeitjes werden vijf dagen gevolgd, waarbij werd gecontroleerd of ze normaal deelden, het blastocyststadium bereikten (een holle bol cellen klaar om in te hechten) en hoeveel cellen elke blastocyst bevatte — een gevoelige maat voor embryo‑gezondheid.
Wanneer één slecht apparaat de hele keten bederft
De meeste combinaties van apparaten gedroegen zich goed: embryo’s gekweekt in media die blootgesteld waren aan acht van de tien apparaattrajecten ontwikkelden zich even goed als in schone controlematerialen. Twee combinaties staken echter duidelijk af. Een betrof hoogbeveiligde spermavriesrietjes en de andere richtte zich op embryo‑transfer met een specifiek kathetermodel. In deze twee gevallen bereikten minder embryo’s het gevorderde blastocyststadium, en degenen die dat wel deden hadden minder cellen, wat wijst op stress of schade. Om de schuldige te achterhalen, testte het team elk component afzonderlijk en in herhaalde batches. Dezelfde types zaadrietjes en katheters vertoonden consequent toxiciteit, vooral wanneer ze werden gebruikt onder routinematige omstandigheden zoals het bevochtigen van de wattenstop in het rietje of het voorverwarmen van de katheter — stappen die waarschijnlijk de afgifte van vluchtige chemicaliën of hormoonachtige stoffen uit het materiaal vergroten.
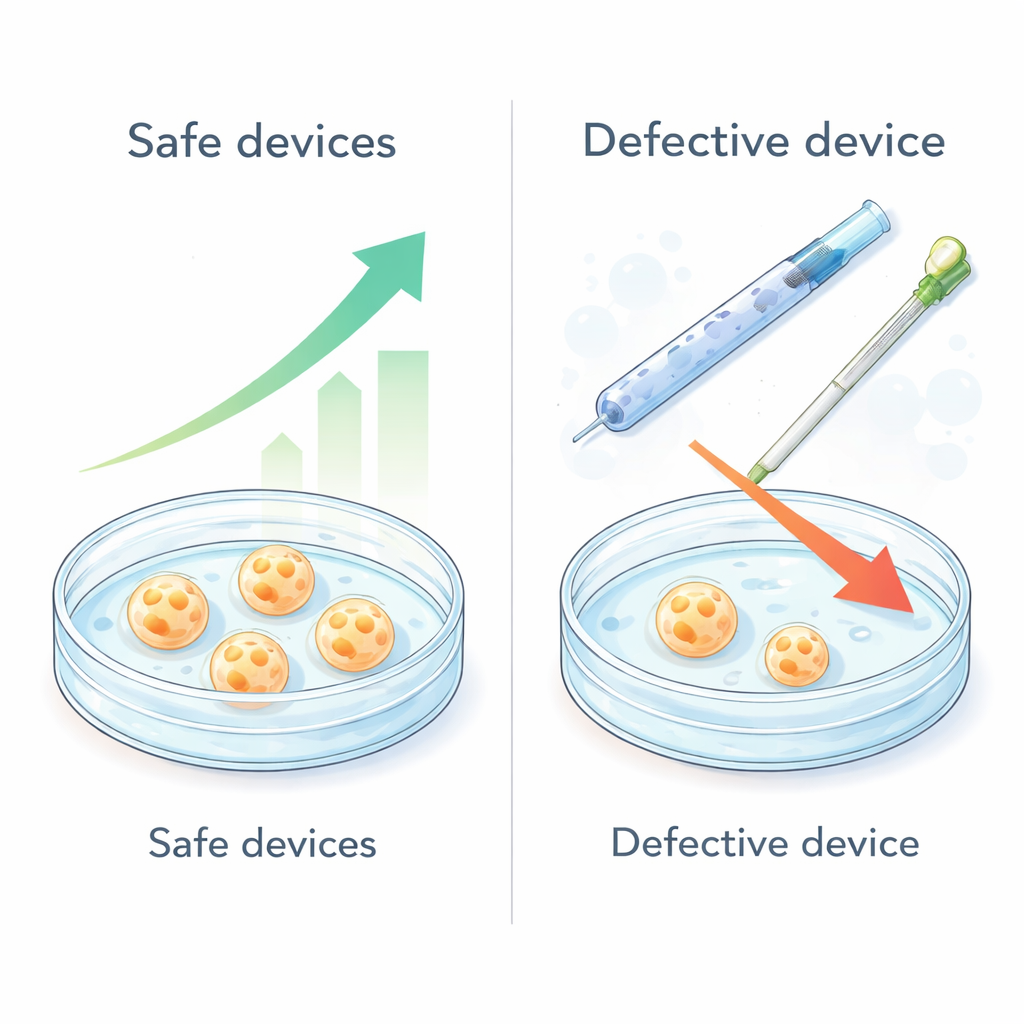
Waarom veiligheidslabels niet het laatste woord zijn
Opvallend was dat de problematische rietjes en katheters al door de interne veiligheidscontroles van de fabrikanten waren gekomen en de vereiste wettelijke markeringen droegen. De mismatch lijkt te ontstaan door de manier waarop de standaard muisassay wordt uitgevoerd. Verschillende bedrijven kunnen verschillende muislijnen, kweekcondities of eindpunten gebruiken, waarvan sommige minder gevoelig zijn voor subtiele toxiciteit. De huidige studie gebruikte een zwaardere benadering, inclusief gedetailleerde tellingen van blastocystcellen, en vond "false negatives" die eerdere tests misten. Het werk herinnert er ook aan dat plastics complexe mengsels kunnen afgeven — waaronder vluchtige organische verbindingen en bisfenolen — die zelfs in lage concentraties schadelijk kunnen zijn, vooral voor vroege embryo’s waarvan de ontwikkeling en de lange termijn‑gezondheid door kleine epigenetische veranderingen kunnen worden beïnvloed.
Wat dit betekent voor patiënten en klinieken
Voor mensen die een IVF‑traject ondergaan is het geruststellende nieuws dat het eenvoudigweg na elkaar gebruiken van veel wegwerpartikelen niet automatisch een toxische omgeving creëert. Het gevaar ontstaat wanneer één defect of slecht getest item wordt geïntroduceerd, waarna het de hele procedure kan compromitteren. Voor klinieken en toezichthouders is de boodschap dringender: vertrouw niet alleen op fabrikantenverklaringen. Elk laboratorium zou nieuwe partijen van kritieke apparaten moeten verifiëren met gevoelige embryo‑gebaseerde tests, en autoriteiten zouden moeten aandringen op geharmoniseerde, strengere testprotocollen. Door de kwaliteitscontrole van de "onzichtbare" hulpmiddelen van IVF aan te scherpen, kunnen we embryo’s beter beschermen, het aantal misslukte cycli door verborgen toxiciteit verminderen en patiënten een veiliger, betrouwbaarder pad naar het ouderschap bieden.
Bronvermelding: Delaroche, L., Besnard, L., Bazin, F. et al. The sequential use of IVF disposable devices doesn’t cause cumulative toxicity unless a defective device compromises the entire procedure. Sci Rep 16, 5491 (2026). https://doi.org/10.1038/s41598-026-35128-x
Trefwoorden: IVF-veiligheid, embryotoxiciteit, laboratoriumplastic, muisembryo-assay, wegwerp medische apparaten