Clear Sky Science · nl
Dubbel-specifieke fosfatase 6 verstoort de remmende werking van forkhead box O1 op CYP4A11 die vetophoping in de lever bevordert
Waarom vet in de lever belangrijk is
Te veel vet in de lever, vaak aangeduid als vetsleverziekte, komt steeds vaker voor door moderne diëten die rijk zijn aan suiker en vet. Hoewel veel mensen bekend zijn met cholesterol of bloedsuiker, weten minder mensen dat kleine moleculaire schakelaars in levercellen helpen bepalen of vet wordt verbrand of opgeslagen. Deze studie bekijkt drie van die schakelaars — eiwitten genaamd DUSP6, FOXO1 en CYP4A11 — en onthult hoe hun machtsspel levercellen kan duwen richting het opslaan van overtollig vet. Inzicht in dit verborgen regelsysteem kan wijzen op nieuwe behandelingsmogelijkheden voor vetsleverziekte en aanverwante metabole problemen.
Een verborgen verkeersregelaar in levercellen
De onderzoekers richtten zich op een eiwit genaamd DUSP6, dat vooral bekendstaat om het uitschakelen van een cel‑signaleringstraject dat het ERK‑pad wordt genoemd. Eerder werk toonde aan dat muizen zonder DUSP6 verrassend resistent waren tegen dieet‑geïnduceerde vetslever en dat hun lever lagere niveaus van CYP4A‑enzymen had, die betrokken zijn bij vetverwerking. Hier onderzochten de onderzoekers wat DUSP6 doet in menselijk leverafgeleid materiaal en hoe het de menselijke versie van deze enzymen, CYP4A11, kan beïnvloeden. Ze gebruikten twee standaard leverkankercellijnen, HepG2 en HuH‑7, als vervangers voor menselijke levercellen en beladen deze met een mengsel van vetzuren (palmitinezuur en oliezuur) om een ongezonde, vetrijke omgeving na te bootsen. 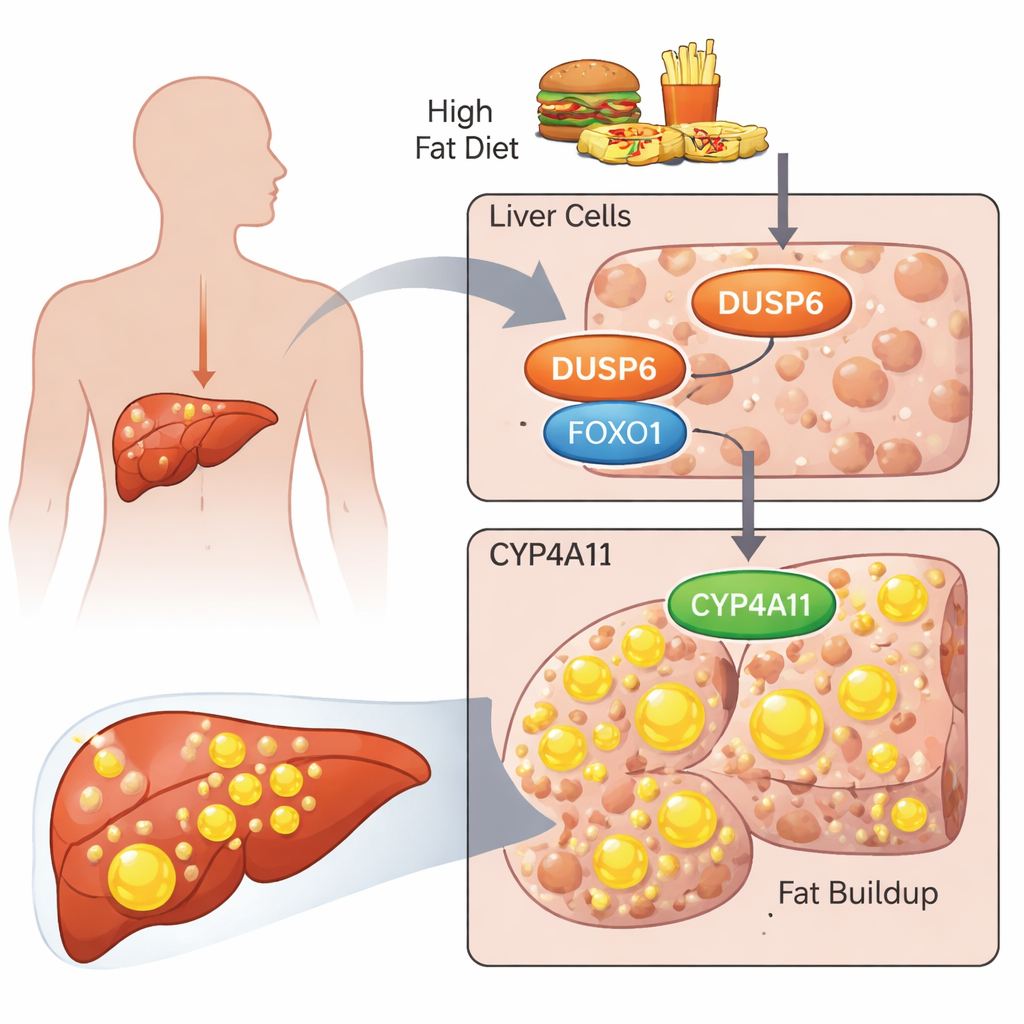
Van vetzuren naar een vetvolle cel
Wanneer de cellen werden blootgesteld aan deze vetzuren, hoorden ze zichtbaar vetdruppels op te hopen, die de wetenschappers kleurden en kwantificeerden. Tegelijkertijd stegen de niveaus van DUSP6 en CYP4A11, samen met geactiveerde vormen van twee belangrijke signaalproteïnen, AKT en FOXO1. Het neerhalen van DUSP6 met gerichte RNA‑moleculen keerde dit patroon om: de cellen slaagden minder vet op, CYP4A11‑niveaus daalden, maar geactiveerd ERK, AKT en FOXO1 namen juist toe. Het blokkeren van alleen het ERK‑pad maakte de vetophoping zelfs erger, terwijl het blokkeren van alleen AKT die ophoping verminderde. Wanneer zowel ERK als AKT tegelijkertijd werden geremd, daalde de vetophoping en namen de CYP4A11‑niveaus af. Deze experimenten koppelden CYP4A11 sterk aan de mate van vetophoping en suggereerden dat AKT‑activiteit bijzonder belangrijk is voor het stimuleren van vetopslag.
Een rem op vetbevorderende genen
Een andere sleutelspeler, FOXO1, is een transcriptiefactor — een eiwit dat de celkern kan binnengaan en genen aan of uit kan zetten. FOXO1 staat bekend als een rem op verschillende leden van dezelfde enzymfamilie als CYP4A11. Het team vond dat het verlagen van FOXO1‑niveaus de cellen meer vet liet opslaan en CYP4A11 verhoogde, terwijl het direct verhogen van CYP4A11 de cellen nog vetter maakte. Daarentegen verminderde het forceren van hogere FOXO1‑productie zowel CYP4A11 als vetophoping. Een middel dat de activiteit van CYP4A11 remt (HET0016) sneed in het extra vet dat werd veroorzaakt door lage FOXO1, wat de gedachte ondersteunt dat CYP4A11 niet slechts een toeschouwer is maar een stuurmiddel van lipidenopbouw. Chemische tests toonden aan dat HET0016 het niveau van 20‑HETE verlaagde, een product gemaakt door CYP4A11 dat in verband wordt gebracht met oxidatieve stress en ontsteking, wat deze route verder koppelt aan leverschade.
Hoe DUSP6 de rem uitschakelt
Om te begrijpen hoe FOXO1 CYP4A11 reguleert, onderzochten de wetenschappers het DNA‑gebied voor het CYP4A11‑gen en vonden sequenties waar FOXO1 kan binden. Met een chromatine‑immunoprecipitatie‑assay lieten ze zien dat FOXO1 — specifiek de niet‑gefosforyleerde vorm — rechtstreeks bindt aan de promoter van CYP4A11, consistent met een remmende rol op dit gen. Co‑immunoprecipitatie‑experimenten toonden aan dat DUSP6 fysiek interageert met FOXO1 maar niet met de gefosforyleerde versie ervan. Fractie‑ en microscopiestudies lieten zien dat DUSP6 zich in het cytoplasma van de cel bevindt en, wanneer aanwezig, meer FOXO1 uit de kern houdt. Wanneer DUSP6 werd neergehaald, verhuisde meer FOXO1 naar de kern, waar het DNA kon binden en CYP4A11 onderdrukken. In feite fungeert DUSP6 als een anker, die FOXO1 in het cytoplasma sekwestreert en voorkomt dat het zijn remmende taak op CYP4A11 uitvoert. 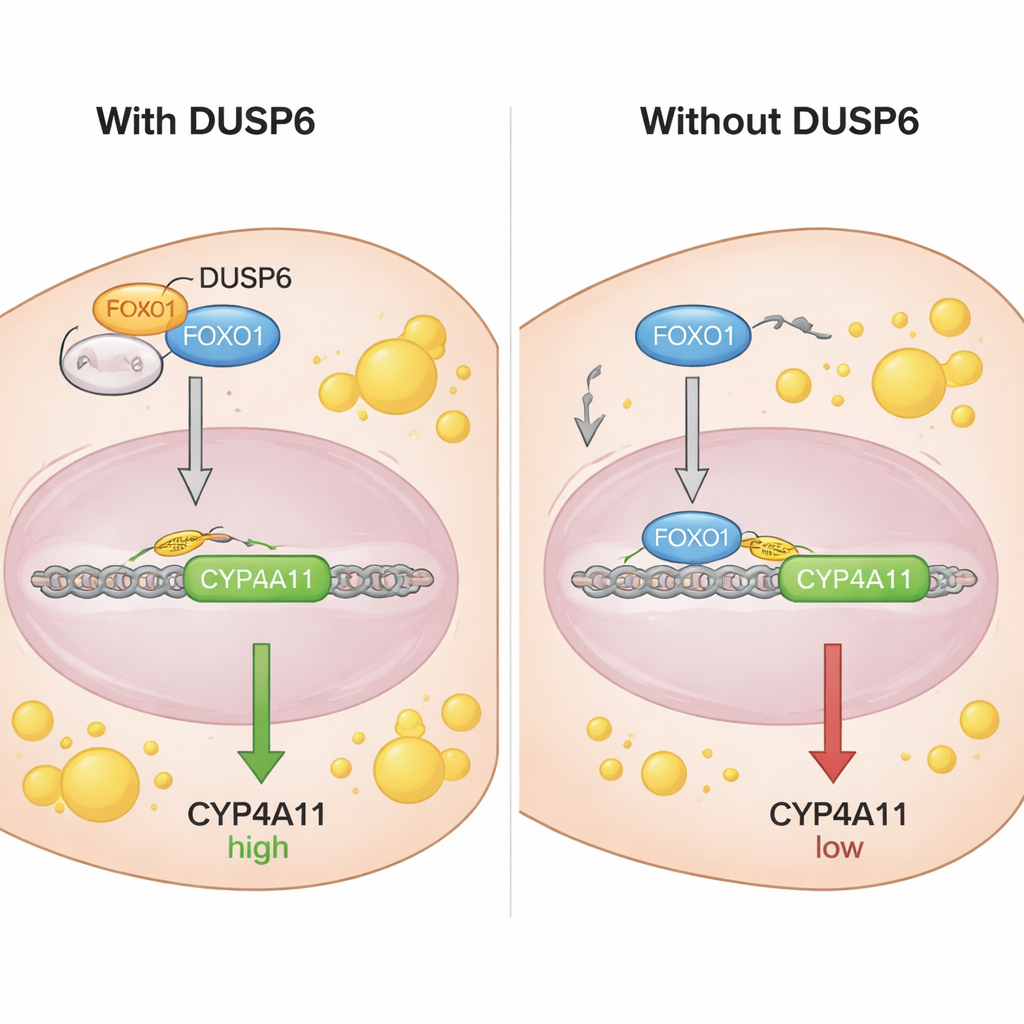
Wat dit betekent voor vetslever en verder
Simpel gezegd brengt dit werk een keten van gebeurtenissen in levercellen in kaart: DUSP6 houdt FOXO1 in het cytoplasma vast, waardoor FOXO1’s vermogen om het CYP4A11‑gen uit te schakelen verzwakt. Met FOXO1 op de zijlijn wordt CYP4A11 actiever, wat de cel helpt meer vet op te slaan en moleculen zoals 20‑HETE te produceren die mogelijk oxidatieve stress en ontsteking bevorderen. Hoewel deze bevindingen afkomstig zijn van gekweekte lever‑afgeleide cellen en niet van gezond menselijk leverweefsel, benadrukken ze DUSP6 en CYP4A11 als potentiële nieuwe doelwitten voor de behandeling van metabool‑gerelateerde steatotische leverziekte. Therapieën die DUSP6‑activiteit verminderen of de effecten van CYP4A11 dempen, zouden in theorie FOXO1’s remfunctie kunnen herstellen en helpen om levervet onder controle te houden.
Bronvermelding: Kimura, M., Saiki, Y., Iwata, K. et al. Dual-specificity phosphatase 6 interferes with the repressive activity of forkhead box O1 towards CYP4A11 that mediates lipid accumulation in the liver. Sci Rep 16, 4795 (2026). https://doi.org/10.1038/s41598-026-35118-z
Trefwoorden: vetsleverziekte, DUSP6, FOXO1, CYP4A11, levermetabolisme