Clear Sky Science · nl
DrugBank-mining met machine learning onthult nieuwe kandidaten voor BCL-2-remming
Waarom het vinden van slimmere kankertherapieën belangrijk is
Kankercellen weigeren vaak te sterven wanneer dat zou moeten. Veel tumoren overleven door het overmatig gebruik van een familie van “lichaamswacht”-eiwitten genaamd BCL-2, die het ingebouwde zelfmoordprogramma van de cel blokkeren. Er bestaan al geneesmiddelen die BCL-2 richten, maar die kunnen bijwerkingen veroorzaken en werken niet bij elke patiënt. Deze studie onderzoekt hoe moderne machine learning duizenden bestaande geneesmiddelen kan doorzoeken om nieuwe, veiliger kandidaten te vinden die BCL-2 kunnen uitschakelen en kankercellen kunnen helpen zichzelf te laten afsterven.
Hoe cellen kiezen tussen leven en dood
Gezond weefsel verwijdert voortdurend beschadigde of overbodige cellen via een gecontroleerd zelfvernietigingsproces dat bekendstaat als apoptose, of geprogrammeerde celdood. Een groep eiwitten, de BCL-2-familie, fungeert als een centraal schakelaar voor deze beslissing. Sommige leden duwen cellen richting overleving, terwijl anderen hen richting dood duwen. In veel vormen van kanker worden de overlevingsbevorderende leden, waaronder BCL-2 en zijn nauwe verwant BCL-XL, overmatig geproduceerd. Deze extra bescherming stelt kankercellen in staat doodsignalen te negeren en weerstand te bieden tegen chemotherapie. Om die reden is het blokkeren van BCL-2 een aantrekkelijke strategie in de kankerbehandeling geworden, maar huidige medicijnen treffen vaak ook verwante eiwitten, wat leidt tot bijwerkingen zoals gevaarlijke dalingen in het aantal bloedplaatjes.
Computers leren veelbelovende moleculen te herkennen
In plaats van van nul af aan naar nieuwe verbindingen te zoeken, gingen de onderzoekers naar databases met moleculen die al onderzocht of als geneesmiddel gebruikt zijn. Ze begonnen met een grote openbare bron genaamd ChEMBL, die experimentele metingen bevat van hoe sterk verschillende chemicaliën aan BCL-2 binden. Na zorgvuldige opschoning van deze informatie — het verwijderen van duplicaten, onzeker gemeten waarden en te grote of ongewone moleculen — hielden ze 601 goed gekarakteriseerde verbindingen over. Elk molecuul werd vertaald naar een soort digitale vingerafdruk die structurele kenmerken vastlegt. Deze vingerafdrukken werden gebruikt om zeven verschillende machine-learningmodellen te trainen en te vergelijken in de taak te bepalen of een nieuw molecuul waarschijnlijk een sterke BCL-2-remmer is of in wezen inactief. 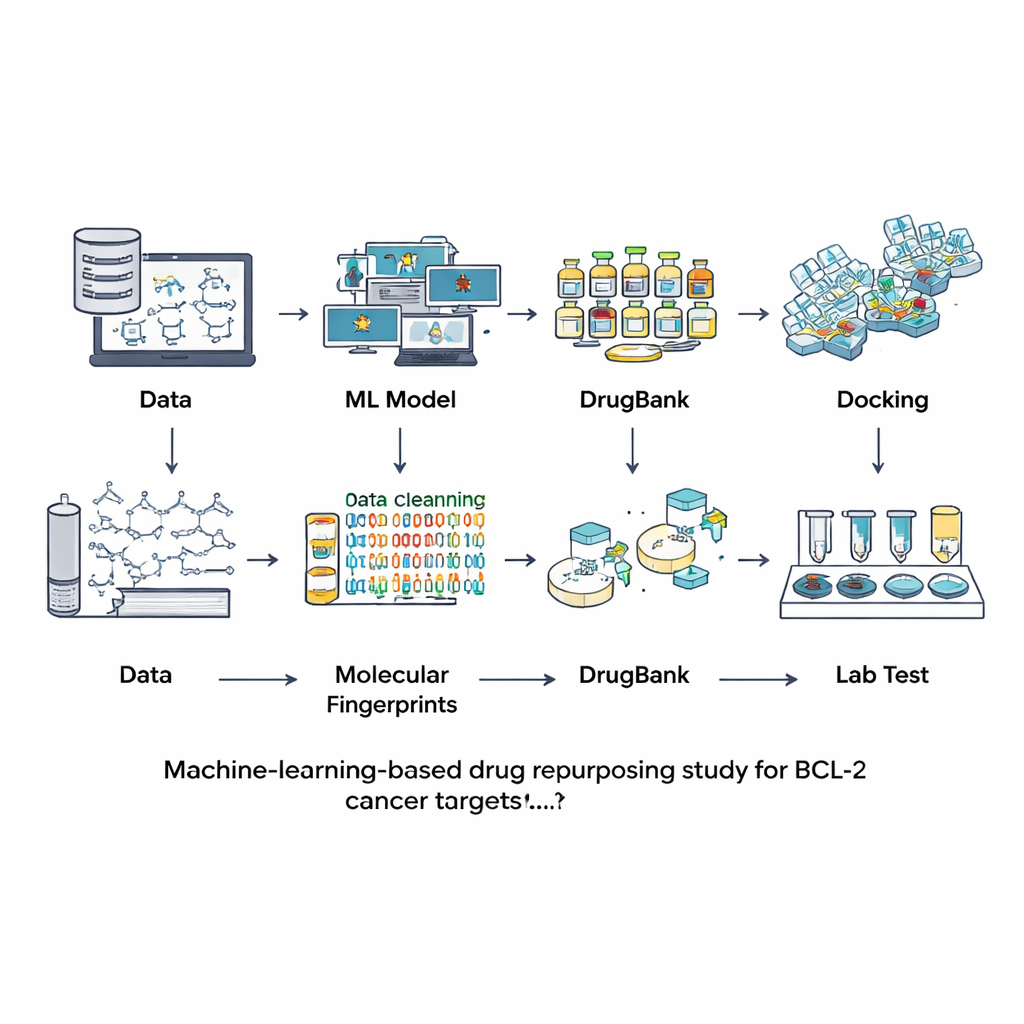
Het beste model kiezen en een geneesmiddelenbibliotheek doorzoeken
Het team evalueerde de modellen met een aparte testset die niet tijdens het trainen was gebruikt, waarbij ze niet alleen keken hoe vaak elk model gelijk had, maar ook hoe goed het actieve stoffen van inactieve onderscheidde en hoe gebalanceerd de voorspellingen waren. Een model genaamd LightGBM — een moderne, boomgebaseerde boostingsmethode — presteerde het beste op de meeste maatstaven, waaronder de algehele nauwkeurigheid en het vermogen betrouwbare waarschijnlijkheden toe te kennen. Met dit fijn afgestelde model gingen de onderzoekers naar DrugBank, een gecureerde verzameling van meer dan 12.000 toegelaten, experimentele en teruggetrokken geneesmiddelen. Na het berekenen van hetzelfde type vingerafdrukken vroegen ze aan LightGBM welke van deze moleculen eruitzagen als potentiële BCL-2-remmers. Slechts negen verbindingen scoorden hoog, ongeveer het top-0,1 procent van de hele bibliotheek, wat aangeeft dat het virtuele screen zeer selectief was. Vier van de negen waren al bekende BCL-2-remmers, wat het team geruststelde dat de aanpak degelijk was.
Van computerhits naar moleculaire interacties
Onder de overige hoog scorende moleculen richtten de onderzoekers zich op drie die eerder niet met BCL-2 in verband waren gebracht: Dersalazine, Opelconazole en Zongertinib. Om te onderzoeken of deze kandidaten plausibel in het bindingsvak van BCL-2 zouden passen, gebruikten ze docking, een computergestuurde techniek die voorspelt hoe een klein molecuul zich in het eiwitoppervlak nestelt. De simulaties suggereerden dat vooral Opelconazole en Zongertinib netwerken van gunstige contacten vormen met dezelfde sleutelaminozuren die een goed bestudeerd referentiegeneesmiddel, ABT-737, grijpen. Hun voorspelde bindingssterktes lagen dicht bij die van gevestigde remmers, wat erop wijst dat het machine-learningmodel inderdaad moleculen had ontdekt die BCL-2 kunnen uitschakelen. 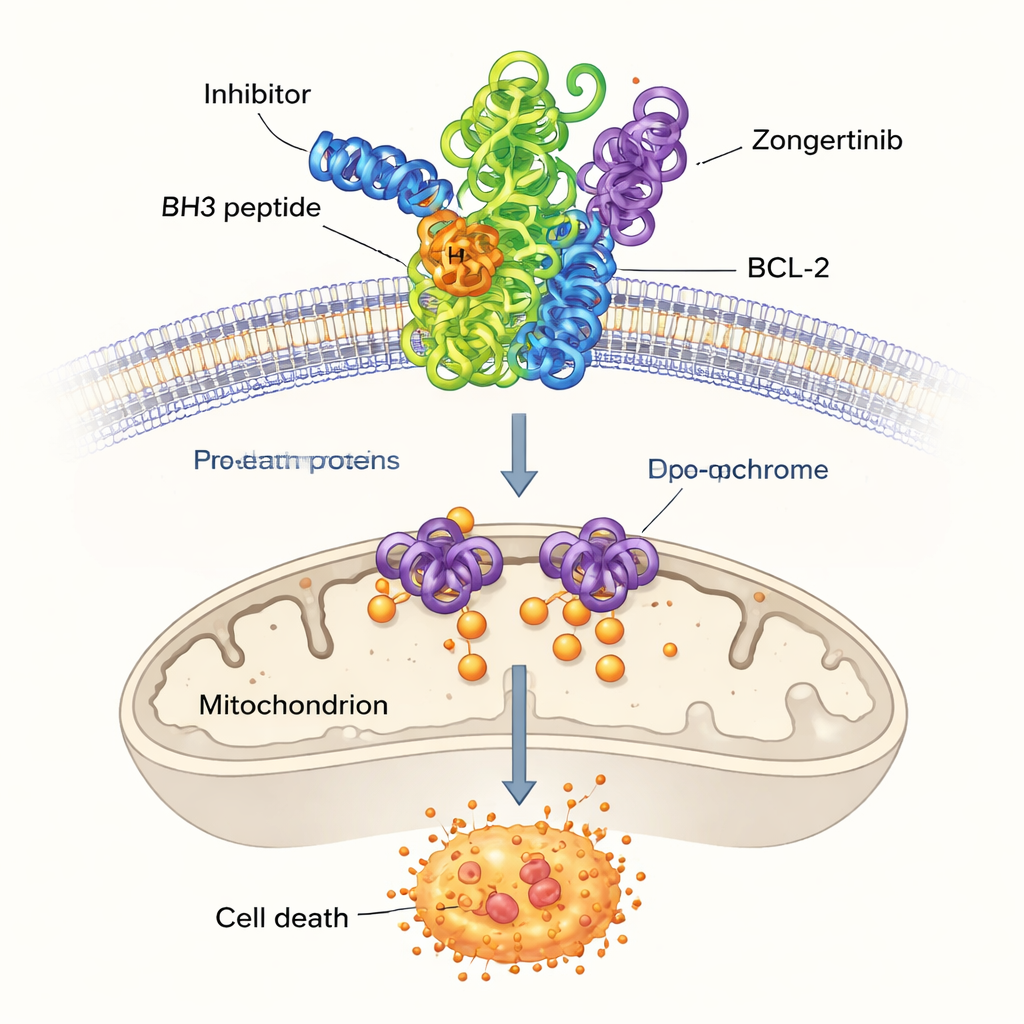
Voorspellingen in het laboratorium testen
Computationale aanwijzingen zijn alleen nuttig als ze standhouden onder reële omstandigheden. Het team testte daarom de drie kandidaten in een biochemische assay die meet hoe goed een verbinding kan voorkomen dat BCL-2 bindt aan een van zijn natuurlijke partners. Bij verschillende concentraties toonde Dersalazine weinig effect. Opelconazole en Zongertinib verminderden echter allebei de BCL-2-activiteit bij hoge doses, waarbij Opelconazole het signaal bijna uitschakelde. Hoewel deze concentraties hoger zijn dan ideaal voor een kliniekrijpe stof, tonen ze aan dat de kandidaten daadwerkelijk met BCL-2 interageren en valideren ze de volledige ontdekkingspipeline.
Wat dit betekent voor toekomstige kankertherapieën
Voor een niet-specialist is de kernboodschap dat de onderzoekers succesvol een computersysteem hebben getraind om te herkennen hoe een BCL-2-blokkerend molecuul “eruitziet”, en dat ze het vervolgens hebben gebruikt om een grote bibliotheek van bestaande geneesmiddelen en geneesmiddelachtige verbindingen te doorzoeken. De aanpak vond bekende BCL-2-geneesmiddelen terug en belichtte nieuwe kandidaten, waarvan er twee echte remmende activiteit toonden in laboratoriumtests. Hoewel er nog veel werk te doen is — het verbeteren van potentie, het begrijpen van veiligheid en testen in cellen en dieren — laat deze studie zien hoe machine learning en slimme datacuratie het zoeken naar betere kankertherapieën kunnen versnellen door verbindingen die we al kennen te hergebruiken en opnieuw te evalueren.
Bronvermelding: Park, J., Cho, S., Lee, H. et al. DrugBank mining with machine learning reveals novel candidates for BCL-2 inhibition. Sci Rep 16, 5482 (2026). https://doi.org/10.1038/s41598-026-35117-0
Trefwoorden: BCL-2-remmers, machine learning, herbestemming van geneesmiddelen, apoptose, kankertherapie