Clear Sky Science · nl
DMEK-transplantaten bereid uit hoornvliezen bewaard in TISSUE-C en CARRY-C (deswelling-medium) tonen vergelijkbare dichtheid van vitale endotheelcellen
Waarom dit belangrijk is voor het gezichtsvermogen
Voor duizenden mensen per jaar is een hoornvliestransplantatie de enige manier om helder zicht te herstellen. Chirurgen en oogbanken doen hun best het donormateriaal zo voor te bereiden dat er zoveel mogelijk levende cellen behouden blijven. Deze studie stelt een praktisch maar cruciaal vraagstuk: schaadt een gebruikelijke stap om donorkorneae te dunnen en ‘‘steviger’’ te maken vóór de operatie de fragiele cellen die het hoornvlies doorzichtig houden, of is de schijnbare schade slechts een illusie veroorzaakt door de manier waarop we die cellen meten?
Hoe chirurgen een troebel venster van het oog herstellen
Het hoornvlies is het doorzichtige voorste venster van het oog. De binnenzijde wordt bekleed door een enkele laag pompende cellen die het helder houden door de waterinhoud te regelen. Als deze cellen falen, zwelt het hoornvlies op en wordt het troebel, wat het zicht vertroebelt. Moderne chirurgie vervangt vaak alleen deze dunne binnenlaag met een techniek genaamd DMEK, waarbij alleen het dunne membraan en de levende pompende cellen van een donornier worden getransplanteerd. Omdat elke extra levende cel helpt dat de transplantatie langer meegaat, tellen oogbanken routinematig deze cellen om te bepalen of een hoornvlies geschikt is voor gebruik.
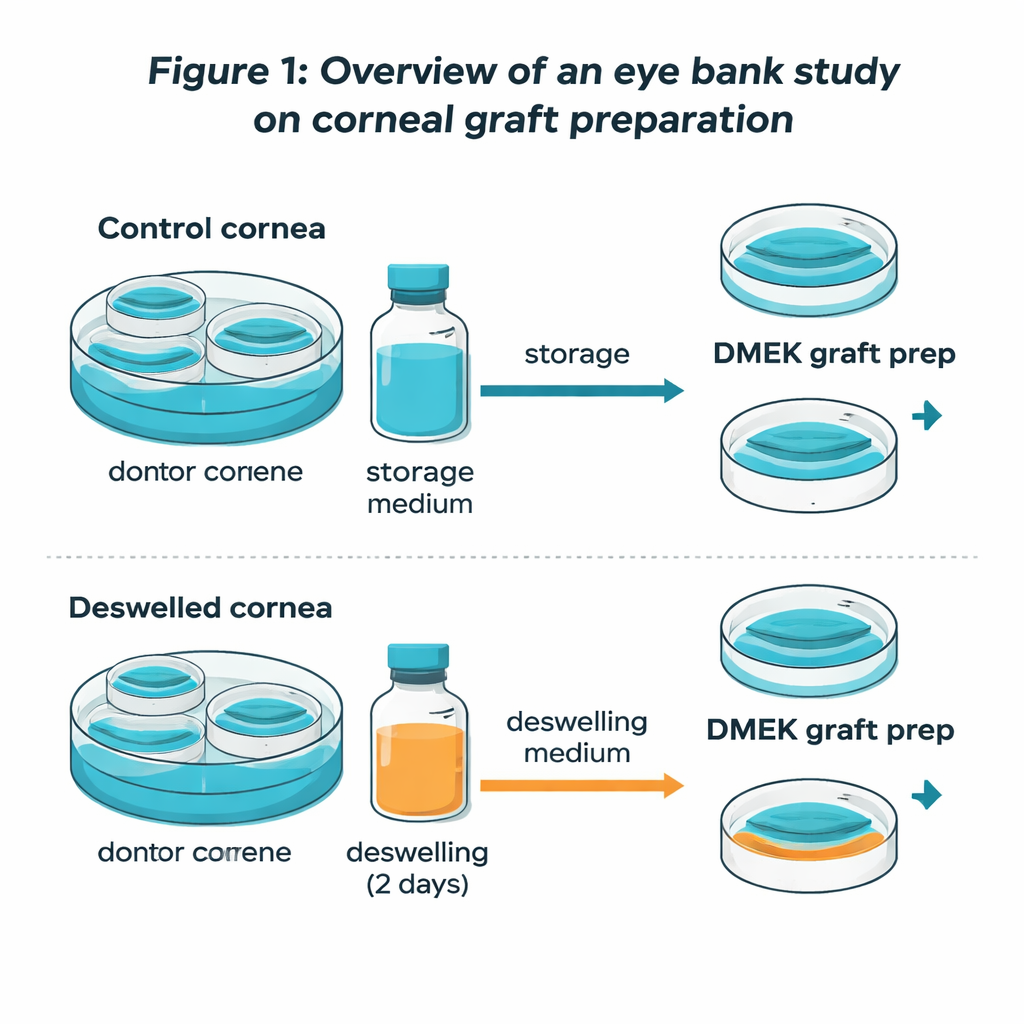
Waarom hoornvliezen worden uitgedund vóór de operatie
In veel Europese oogbanken worden donorkorneae enkele dagen in een warme bewaarvloeistof gehouden, zodat ze voor de operatie kunnen worden getest. In die tijd zwellen ze op als een spons in water, wat plooien op de binnenoppervlakte veroorzaakt en het chirurgische afpellen moeilijker kan maken. Om dit op te lossen verplaatsen oogbanken het hoornvlies vaak een paar dagen naar een speciaal ‘‘deswelling’’-medium dat een suikerachtig bestanddeel bevat genaamd dextran. Dit trekt water aan en herstelt een meer normale dikte. Oudere rapporten suggereerden echter dat zulke dextran-rijke media de pompende cellen zouden kunnen vergiftigen, omdat celmetingen daarna lager leken. Klinische studies bij patiënten lieten echter geen slechtere lange-termijnresultaten zien, wat een puzzel opleverde: doodde dextran echt cellen, of misleidden de tellingen?
Een directe vergelijking van gepaarde donorkorneae
Om dit aan te pakken gebruikten de onderzoekers acht paren menselijke donorkorneae die niet geschikt waren voor transplantatie maar nog wel waardevol voor onderzoek. Beide hoornvliezen in elk paar begonnen in hetzelfde standaard bewaarmedium en hadden bijna identieke initiële celmetingen. Twee weken later bleef het ene hoornvlies van elk paar in het oorspronkelijke medium, terwijl het partnerhoornvlies twee dagen in het dextran-deswelling-medium doorbracht voordat het werd voorbereid volgens DMEK-achtige procedures. Het team gebruikte vervolgens geavanceerde fluorescentkleurstoffen en beeldvorming om in kaart te brengen waar levende cellen voorkwamen over het centrale gebied en om niet alleen te berekenen hoe dicht ze opeengepakt zaten, maar ook hoeveel vitale cellen er in totaal aanwezig waren.

Wat de gebruikelijke cijfers verborgen hielden
Op het eerste gezicht leken de routinemetingen de oude zorgen te bevestigen: na deswelling waren de standaard celmetingen ongeveer een kwart lager dan in de hoornvliezen die opgezwollen bleven. Maar toen de wetenschappers levend-celkleuringen over het hele binnenoppervlak legden, verscheen een ander beeld. Opgezwollen hoornvliezen hadden veel diepe plooien met kale, dode zones die niet zichtbaar werden in de routinematige tellingen, die alleen gebieden bemonsteren waar cellen duidelijk te zien zijn. Deswellde hoornvliezen hadden daarentegen veel minder plooien en een gladder oppervlak. Naburige cellen waren gemigreerd om eerder lege plekken te bedekken, waardoor ze zich gelijkmatiger verspreidden. Dit maakte ze op een willekeurige plek iets minder dicht opeengepakt, waardoor het ‘‘cellen per vierkante millimeter’’-cijfer daalde, maar de totale voorraad levende cellen over het transplantatiegebied—de maat die echt telt voor overleving van het graft—was in beide groepen in wezen gelijk.
Wat dit betekent voor patiënten en oogbanken
Voor patiënten die wachten op zichtherstellende chirurgie zijn deze bevindingen geruststellend. Een korte, tweedaagse blootstelling aan een dextran-gebaseerd deswelling-medium verminderde niet daadwerkelijk het aantal levende pompende hoornvliescellen; het verspreidde ze alleen over een groter, gladder oppervlak. De lagere celmetingen gemeld door standaardmethoden bleken een meetartefact te zijn, geen echte toxiciteit. Door het hoornvlies te dunnen en cellen in staat te stellen in eerdere geplooide, niet-functionele gebieden te schuiven, kan deswelling zelfs helpen het weefsel voor te bereiden op een gelijkmatiger, gezonder oppervlak na transplantatie. De studie ondersteunt het voortdurende gebruik van dextran-bevattende deswelling-media voor DMEK-grafts—en waarschijnlijk ook voor volledige-dikte hoornvliestransplantaten—mits de blootstelling kort en zorgvuldig gecontroleerd is.
Bronvermelding: Ninotta, S., Sagnial, T., Goin, P. et al. DMEK grafts prepared from corneas stored in TISSUE-C and CARRY-C (deswelling medium) show similar viable endothelial cell density. Sci Rep 16, 4803 (2026). https://doi.org/10.1038/s41598-026-35103-6
Trefwoorden: hoornvliestransplantatie, DMEK, oogbank, dextran-deswelling, levensvatbaarheid endotheelcellen