Clear Sky Science · nl
Identificeer en karakteriseer een carbapenem-resistente Salmonella enteritidis-fage depolymerase Dpo52
Waarom dit onderzoek belangrijk is voor de dagelijkse gezondheid
Voedselvergiftiging door Salmonella is voor veel mensen bekend, maar een toenemend aantal van deze bacteriën is nu resistent tegen onze sterkste “laatste redmiddel”-antibiotica, de carbapenems. Zodra Salmonella zich vestigt in een slijmerige, beschermende laag die bekendstaat als een biofilm, wordt het nog moeilijker te doden. Deze studie onderzoekt een alternatief wapen: een virus dat bacteriën infecteert en een speciaal enzym dat het draagt, Dpo52, dat de beschermende laag van Salmonella kan weghalen en kan helpen voorkomen dat deze gevaarlijke kiemen zich vestigen.
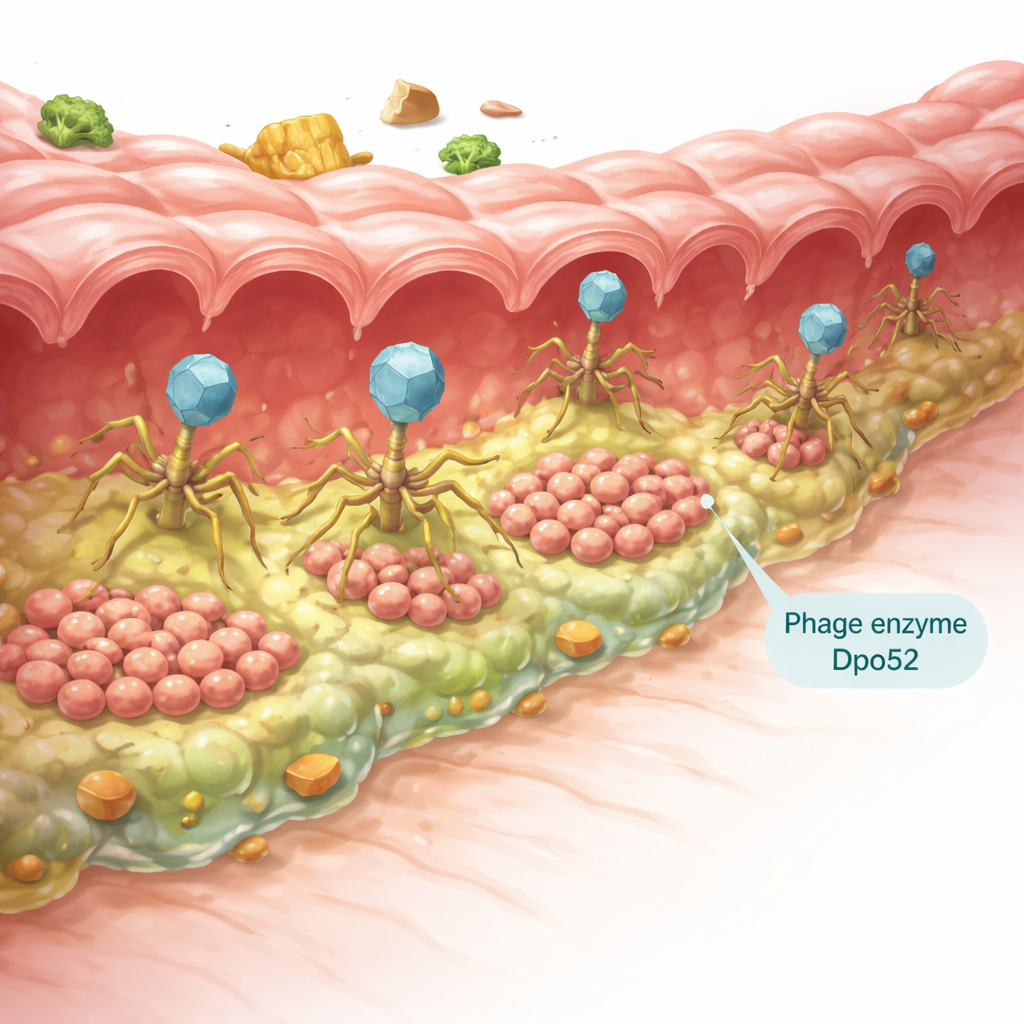
Een groeiend probleem op ons bord
Salmonella enteritidis is een van de meest voorkomende oorzaken van voedselgerelateerde ziekten wereldwijd, vaak in verband gebracht met besmette eieren, pluimvee en andere dierlijke producten. Artsen vertrouwen doorgaans op antibiotica om deze infecties te bestrijden, maar veel Salmonella-stammen hebben geleerd om meerdere middelen te ontwijken, inclusief carbapenems die normaal voor ernstige gevallen worden bewaard. Een belangrijke reden is dat de bacteriën biofilms vormen — slijmerige gemeenschappen die aan oppervlakken blijven plakken, zoals de darmwand, voedselverwerkingsapparatuur of voedsel zelf. Binnen deze biofilms zijn bacteriën afgeschermd van antibiotica en van het immuunsysteem, waardoor een routine-infectie een veel groter probleem wordt.
Van bacteriële virussen helpers maken
De onderzoekers concentreerden zich op bacteriofagen, kortweg fagen — virussen die specifiek bacteriën infecteren. Ze isoleerden een faag uit ziekenhuisrioolwater in China die carbapenem-resistente S. enteritidis aanvalt en noemden hem vB_Sen_S3P. Deze faag kon 22 van de 30 uit patiënten afkomstige Salmonella-isolaten infecteren, inclusief de meest medicijnresistente. Elektronenmicroscoopbeelden toonden een klassieke faagstructuur met een geometrische kop en een korte staart, en groeiproeven lieten zien dat hij zich snel vermenigvuldigt en duizenden nieuwe deeltjes vrijgeeft uit elke geïnfecteerde bacterie. Genetische sequencing bevestigde dat deze faag geen bekende antibioticaresistentie- of virulentiegenen draagt, wat hem een veelbelovende kandidaat maakt voor veilig therapeutisch gebruik.
Het speciale enzym dat het slijm weghaalt
In het DNA van de faag identificeerde het team een gen genaamd ORF52 dat waarschijnlijk codeert voor een depolymerase — een enzym dat de lange suikerketens die de bacteriële kapsel en de biofilmmatrix vormen, afbreekt. Zij kloonden dit gen in laboratorium-E. coli, produceerden het eiwit en noemden het Dpo52. Structurele voorspellingen suggereerden dat een deel van Dpo52 herkent en zich bindt aan het oppervlak van Salmonella, terwijl een ander deel werkt als een moleculair “knippertje” voor de extracellulaire suikers. In laboratoriumtests gaven druppels gezuiverd Dpo52 op Salmonella-bodemculturen duidelijke halozones — bewijs dat het enzym het beschermende materiaal rond de cellen wegknabbelde zonder de bacteriën direct te doden.
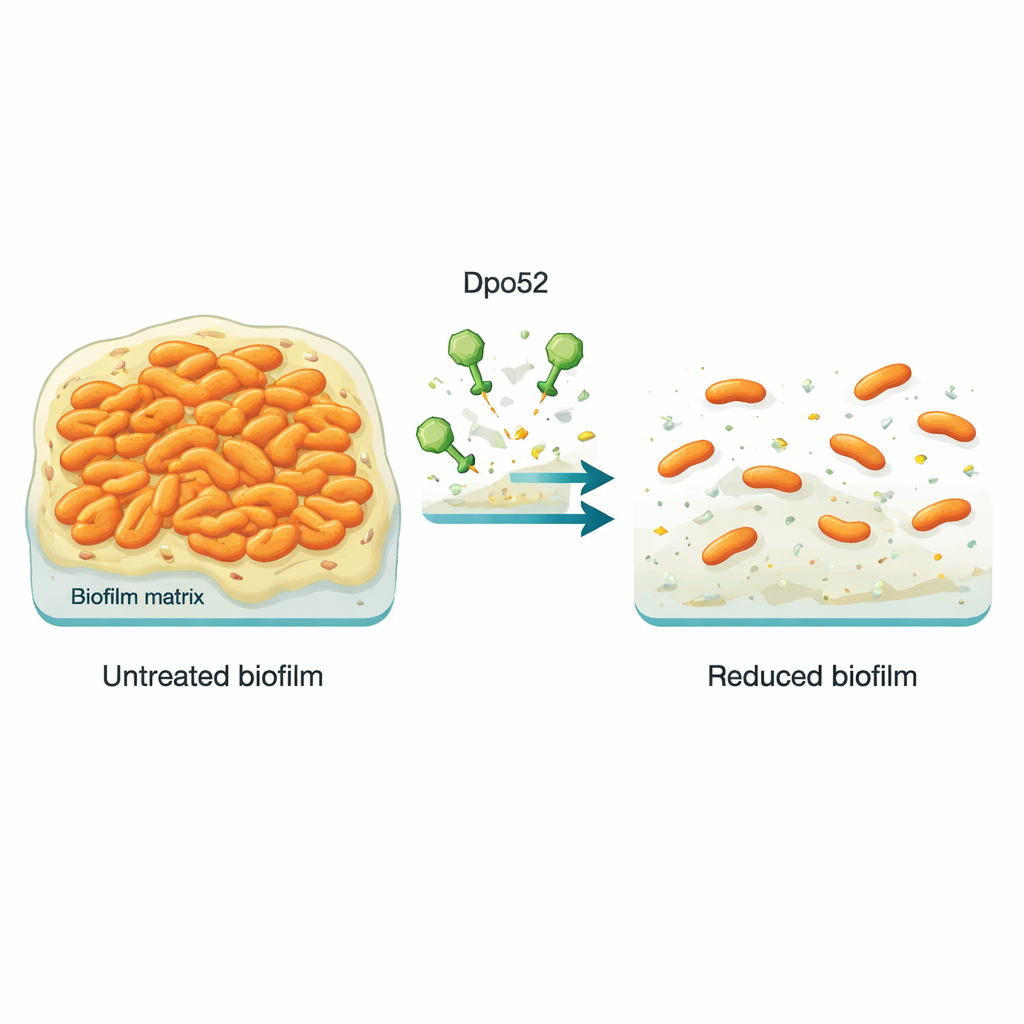
Biofilm stoppen voordat het zich vormt
Om te onderzoeken of Dpo52 de vorming van biofilms kon voorkomen, kweekt de groep twee carbapenem-resistente Salmonella-stammen in kleine plastic putjes, met en zonder verschillende doses van het enzym. Na incubatie kleurden ze de putjes om te meten hoeveel kleverige biofilm zich had opgehoopt. Putjes behandeld met matige tot hoge hoeveelheden Dpo52 vertoonden veel minder kleuring, wat aantoont dat het enzym de biofilmvorming sterk verminderde in een dosisafhankelijke manier. Wanneer biofilms echter eerst de kans kregen te rijpen en vervolgens werden behandeld, kon Dpo52 ze niet meer uiteenhalen, waarschijnlijk omdat de dichte, meerlagige structuur het enzym verhinderde om de volledige suikermatrix te bereiken.
Veiligheid, stabiliteit en toekomstig gebruik
Dpo52 bleek robuust: het bleef actief over een breed scala aan temperaturen, van koelkastkoud tot 60 °C, en van matig zure tot alkalische omstandigheden. Belangrijk was dat tests op menselijke immuuncellen (macrofagen-achtige THP‑1-cellen) geen detecteerbare toxiciteit aantoonden, zelfs niet bij hoge doses. Microscopen bevestigden dat Dpo52 de bleke kapsel rond Salmonella-cellen verwijderde, wat consistent is met zijn rol in het verteren van extracellulaire polysachariden. Samen suggereren deze eigenschappen dat Dpo52 aan oppervlakken, in voedsel of in faaggebaseerde therapieën kan worden toegevoegd als een gericht middel om te voorkomen dat medicijnresistente Salmonella hardnekkige biofilms vormt.
Wat dit betekent voor de strijd tegen hardnekkige infecties
Voor niet-specialistische lezers is de kernboodschap dat dit werk een hooggespecificeerd, niet-toxisch enzym identificeert dat helpt de beschermende “slijmlaag” van gevaarlijke, medicijnresistente Salmonella weg te strippen voordat ze zich kunnen vastzetten. Hoewel Dpo52 niet volledig rijpe biofilms oplost, toont het sterk potentieel als preventieve maatregel — gebruikt alleen of naast fagen en antibiotica — om voedsel- en medische omgevingen veiliger te houden. Naarmate wetenschappers zulke enzymen verfijnen en hun werkingsbreedte vergroten, zouden ze een belangrijk onderdeel kunnen worden van onze toekomstige gereedschapskist tegen antibioticaresistente infecties.
Bronvermelding: Li, W., Yuan, M., Che, J. et al. Identify and characterize a carbapenem-resistant Salmonella enteritidis phage depolymerase Dpo52. Sci Rep 16, 4906 (2026). https://doi.org/10.1038/s41598-026-35081-9
Trefwoorden: Salmonella, antibioticaresistentie, bacteriofaagtherapie, biofilms, depolymerase-enzymen