Clear Sky Science · nl
Kristalstructuur van Echinococcus multilocularis-cystatine B onthult een nieuw kenmerk in klassieke stefines
Waarom het geheime wapen van een leverparasiet ertoe doet
Alveolaire echinokokkose is een lastige naam voor een kleine lintworminfectie die zich in de lever gedraagt als een langzaam groeiende kanker. De ziekte is vaak dodelijk; beschikbare medicijnen werken slecht en kunnen ernstige bijwerkingen hebben. Deze studie richt zich op één specifiek molecuul dat de parasiet produceert — een eiwit genaamd EmCystatin-B — om te begrijpen hoe het de worm kan helpen onze verdediging te omzeilen en hoe het mogelijk een doelwit voor nieuwe behandelingen kan worden.
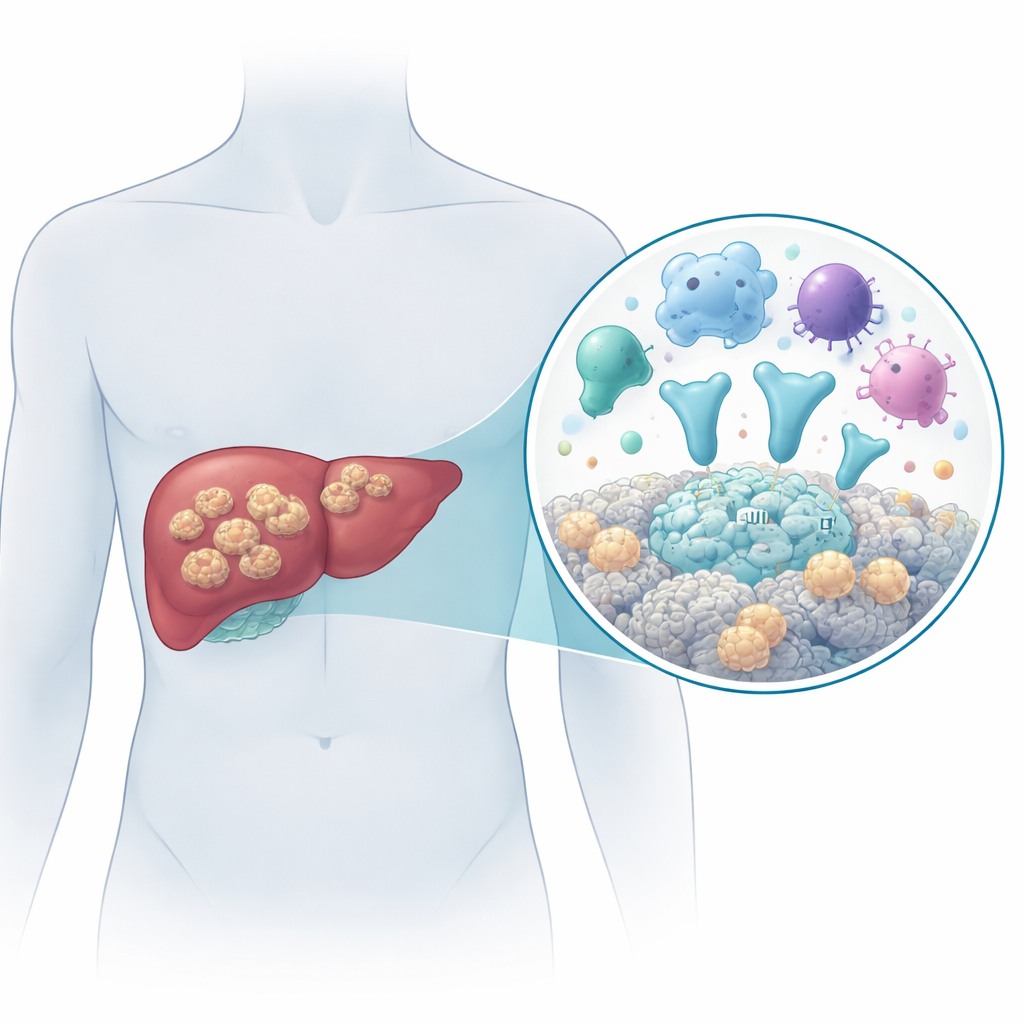
Een gevaarlijke lintworm die zich als een tumor uitbreidt
De ziekte wordt veroorzaakt door het larvale stadium van de lintworm Echinococcus multilocularis. Mensen raken geïnfecteerd door het per ongeluk inslikken van parasieteneieren, bijvoorbeeld via besmet voedsel of water. Eenmaal in het lichaam vestigen de larven zich vooral in de lever en groeien daar als vele kleine met vocht gevulde blaasjes die het omliggende weefsel infiltreren, zich verspreiden naar nabijgelegen organen zoals de milt en soms zelfs op afstand naar de longen of hersenen. Zonder effectieve behandeling sterven meer dan 9 op de 10 patiënten binnen 10 tot 15 jaar. Chirurgie gecombineerd met langdurige antiparasitaire medicijnen is momenteel de beste optie, maar vroege diagnose is moeilijk en de medicijnen genezen de infectie niet altijd. Daarom is het cruciaal te begrijpen hoe de parasiet op moleculair niveau met het menselijk lichaam omgaat.
Een parasiet-eiwit dat knipenzymen uitschakelt
Veel dieren, waaronder mensen, maken een familie eiwitten die cystatines worden genoemd en fungeren als veiligheidsblokkades voor krachtige spijsverteringsenzymen die cysteïneproteasen heten. Deze enzymen kunnen andere eiwitten afbreken en zijn belangrijk voor processen zoals het opruimen van versleten celonderdelen en het activeren van immuunreacties. Parasieten hebben geleerd eigen cystatine-achtige eiwitten te maken om de enzymen en het immuunsysteem van de gastheer te verstoren. In dit werk identificeerden de onderzoekers een cystatine-achtig eiwit van E. multilocularis en noemden het EmCystatin-B. Ze vonden dat het gen voor EmCystatin-B veel actiever is in de rijpe larvale koppen (protoscoleces) van de parasiet dan in het omringende cysteuze weefsel, en dat het eiwit aanwezig is in het cytoplasma en de kern van de parasietcellen, vooral in delende, “stamcelachtige” germinatieve cellen. Laboratoriumtests toonden dat EmCystatin-B de activiteit van menselijke cathepsine B, een belangrijke cysteïneprotease betrokken bij immuniteit en weefselhermodellering, sterk kan blokkeren.
Een vertrouwde vorm met een onverwachte wending
Om precies te zien hoe EmCystatin-B is opgebouwd, kristalliseerde het team het gezuiverde eiwit en gebruikte röntgendiffractie om de driedimensionale structuur op bijna-atoomresolutie te bepalen. Net als andere leden van de cystatinefamilie heeft elk EmCystatin-B-molecuul een kenmerkende vorm: een centraal helixachtig segment ondersteund door meerdere platte, lintachtige strengen, die samen een wig vormen die normaal gesproken in het actieve centrum van een protease past. Op basis van de sequentie en het ontbreken van een duidelijk signaalpeptide voor secretie valt EmCystatin-B in de „stefine”-subgroep van cystatines, die doorgaans kleine intracellulaire eiwitten zijn zonder stabiliserende disulfidebruggen. Verrassend genoeg toonde de structuur aan dat hoewel elk EmCystatin-B-molecuul de verwachte vouwing heeft, de manier waarop deze eenheden met elkaar associëren ongewoon en soortspecifiek is vergeleken met het menselijke tegenhanger, cystatine B.
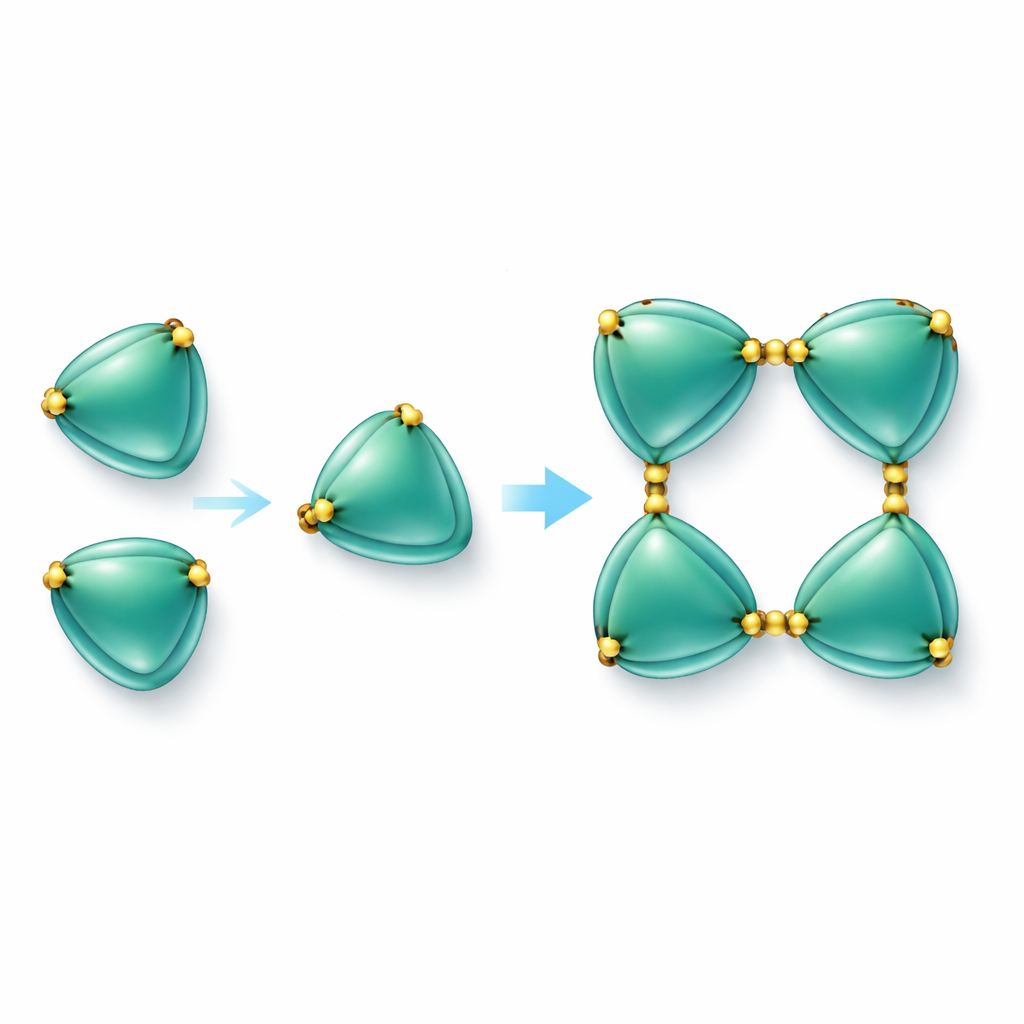
Eiwithaken bouwen met zwavelverbindingen
De opvallendste bevinding was dat EmCystatin-B-moleculen niet gewoon als losse eenheden in oplossing voorkomen. In plaats daarvan kunnen ze zich in stappen aan elkaar koppelen tot dimeren (paren) en daarna tetrameren (groepen van vier). Twee verschillende mechanismen dragen bij aan het vormen van de initiële dimeren. In het ene mechanisme zwaait een deel van het ene molecuul over naar en voltooit het de structuur van zijn buur, een fenomeen dat bekendstaat als domeinruil. In het andere worden paren van moleculen aan elkaar vastgezet door disulfidebruggen — sterke chemische verbindingen tussen zwavelhoudende aminozuren (cysteïnes). In EmCystatin-B vormt de cysteïne op positie 4 in het ene molecuul een binding met cysteïne op positie 76 in een partnermolecuul. Vier van zulke kruisverbindingen stabiliseren vervolgens het tetramer. Het gebruik van meerdere intermolculaire disulfidebruggen is volledig nieuw voor klassieke stefines, die doorgaans dergelijke bruggen missen. Toen de onderzoekers deze sleutelcysteïnes vervingen door een ander aminozuur, kon het eiwit niet langer efficiënt assembleren tot hogere-orde complexen en daalde zijn vermogen om cathepsine B te remmen sterk.
Wat dit betekent voor het bestrijden van de infectie
Voor niet-specialisten komt het erop neer dat de parasiet een speciaal bedraad variant van een veelvoorkomende eiwitfamilie heeft ontwikkeld en extra chemische “nagels” gebruikt om meerdere remmereenheden aan elkaar te vergrendelen. Deze oligomere vorm lijkt belangrijk om een gastheerenzym uit te schakelen dat anders zou helpen de infectie onder controle te houden. Door de precieze architectuur van EmCystatin-B en zijn unieke disulfide-gekoppelde assemblages bloot te leggen, vergroot de studie ons begrip van hoe cystatine-eiwitten tussen soorten kunnen worden afgestemd. Op de lange termijn zouden deze inzichten de ontwikkeling kunnen sturen van geneesmiddelen die ofwel het beschermende effect van EmCystatin-B op de parasiet blokkeren of zijn immuun-onderdrukkende eigenschappen nabootsen om ontstekingsziekten te behandelen.
Bronvermelding: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
Trefwoorden: alveolaire echinokokkose, Echinococcus multilocularis, cystatine B, eiwitstructuur, immuunmodulatie