Clear Sky Science · nl
Verstoring van NLRP3-inflammasoomassemblage via ligand-geïnduceerde herstructurering van pyrindomeininterfaces
Waarom het kalmeren van weglopende ontsteking belangrijk is
Veel chronische ziekten — van artritis en jicht tot hartaandoeningen en neurodegeneratie — worden aangejaagd door een overactief immuunalarmsysteem binnen onze cellen. Een sleutelcomponent van dit alarm, het NLRP3-inflammasoom, helpt ons bij het bestrijden van infecties maar kan ook schadelijke ontsteking aandrijven wanneer het verkeerd afgaat. Deze studie beschrijft een nieuw klein molecuul, E9 genaamd, dat een vroeg stadium van NLRP3-activatie aanpakt en daarmee een nieuwe invalshoek biedt voor het ontwerpen van geneesmiddelen die schadelijke ontsteking temperen zonder het immuunsysteem volledig uit te schakelen.
Een cellulair brandalarm met een donkere kant
Wanneer ons lichaam gevaar detecteert, zetten immuuncellen het NLRP3-inflammasoom in elkaar, een groot eiwitcomplex dat fungeert als een moleculair brandalarm. Zodra het gevormd is, activeert dit complex een enzym genaamd caspase-1, dat op zijn beurt krachtige ontstekingsboodschappers zoals de cytokines IL-1β en IL-18 activeert. Deze signalen zijn essentieel voor het bestrijden van infecties en het opruimen van beschadigd weefsel. Maar als het inflammasoom te lang aanstaat of onverenigbaar wordt geactiveerd, draagt het bij aan chronische ontstekingsziekten die de gewrichten, bloedvaten, hersenen en andere organen treffen. Daarom zoeken onderzoekers wereldwijd naar precieze manieren om NLRP3 te reguleren zonder de algemene immuniteit te onderdrukken.
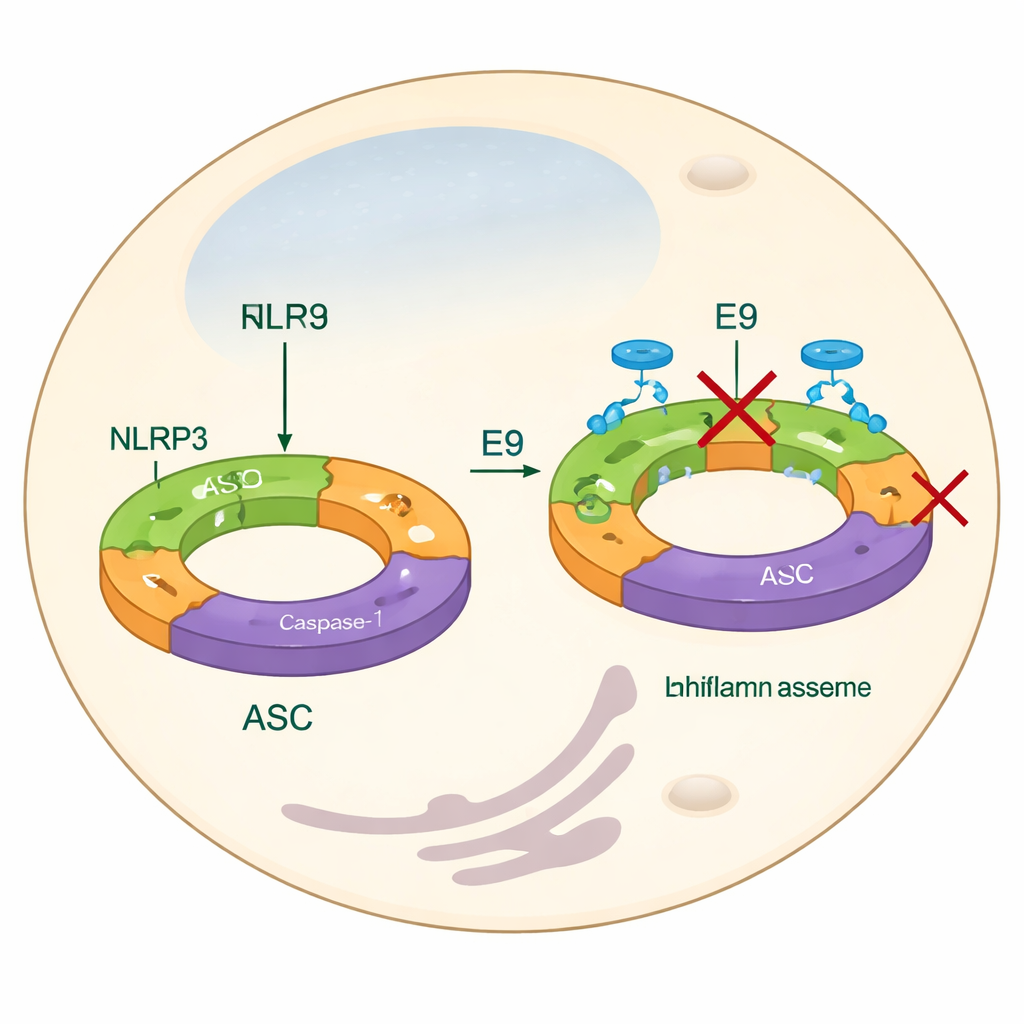
Voorbij de gebruikelijke medicijntargets kijken
De meeste huidige strategieën om NLRP3 te beteugelen richten zich op het blokkeren van de eindproducten — zoals IL-1β — of op het verstoren van een centraal, motorachtig domein dat energiebronnen zoals ATP gebruikt. Hoewel deze benaderingen effectief kunnen zijn, missen ze mogelijk de vroegste assemblagestappen en pakken ze niet volledig aan hoe NLRP3-eiwitten zich samenvoegen tot een functioneel apparaat. In dit werk richten de auteurs zich in plaats daarvan op het pyrindomein, een deel van NLRP3 dat helpt individuele units aaneen te koppelen tot lange filamenten. Deze filamenten rekruteren vervolgens een andere adaptor, ASC, die zich in heldere “specks” in cellen samenklontert — een visueel kenmerk van inflammasoomactivatie. Door chemicaliën te vinden die voorkomen dat pyrindomeinen goed in elkaar passen, wil het team voorkomen dat het inflammasoom zich in de eerste plaats vormt.
Een molecuul vinden dat de keten verbreekt
De onderzoekers screenden een bibliotheek van 1500 nieuw gesynthetiseerde kleine moleculen met een slimme lichtgebaseerde test. Ze fuseerden gespleten delen van een luciferase-enzym aan het NLRP3-pyrindomein; wanneer twee pyrindomeinen samenkwamen, assembleerden de enzymfragmenten opnieuw en produceerden licht. Verbindingen die pyrin–pyrin-contact blokkeerden deden het lichtsignaal zakken. Uit deze screen identificeerden ze vier veelbelovende kandidaten, waarvan één — E9 — opviel door sterke en consistente remming. Vervolgmetingen met microschaalthermophoresetechniek toonden aan dat E9 zich sterk aan het pyrindomein bond bij zeer lage (submicromolaire) concentraties, wat bevestigt dat het effect geen toevallig artefact was maar het resultaat van een specifieke interactie.
Het effect in levende cellen zien
Om te testen of E9 ook in een levend systeem werkt, gebruikten de onderzoekers menselijke immuunachtige cellen die waren aangepast om een fluorescerende versie van ASC te maken. Wanneer deze cellen worden gestimuleerd met bacteriële componenten en een tweede trigger, schakelt NLRP3 in en clusteren ASC-eiwitten tot heldere specks die onder de microscoop kunnen worden geteld. In aanwezigheid van E9 daalde het aantal van deze specks sterk, vergelijkbaar met of beter dan sommige bekende NLRP3-remmers. Dit toont aan dat het verstoren van pyrindomeincontacten voldoende is om de assemblage van het inflammasoom en de vroege stappen van ontstekingsgeleide celdood te verminderen, althans onder laboratoriumomstandigheden.
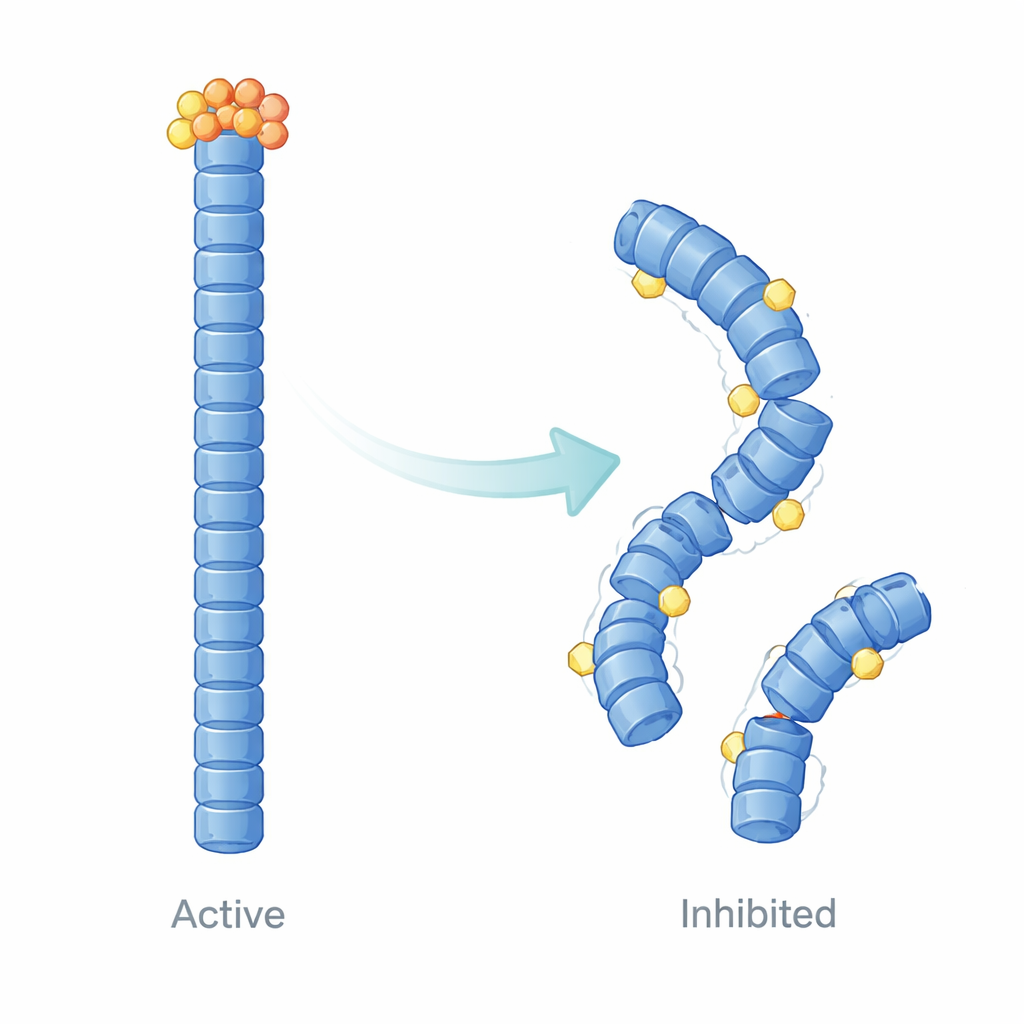
Hoe E9 het inflammasoomskelet hervormt
Buiten het louter meten van binding, gebruikten de auteurs computergestuurde structurele modellering en moleculaire dynamicasimulaties om te visualiseren hoe E9 het gedrag van NLRP3-filamenten in de tijd verandert. Hun berekeningen suggereren dat E9 zich nestelt op specifieke contactvlakken waar pyrindomeinen elkaar raken, en het filament subtiel losser en anders vormgeeft. In plaats van een uniform stabiele, coöperatieve structuur wordt het filament ongelijk: regio's nabij het gebonden E9 worden flexibeler en verliezen hun precieze uitlijning, terwijl andere delen dynamisch geïsoleerd raken. Deze verschuivingen dempen de grootschalige bewegingen en de strakke communicatie die nodig zijn voor efficiënte recrutering van ASC, wat een fysieke verklaring biedt voor de verminderde speckvorming in cellen.
Wat dit kan betekenen voor toekomstige therapieën
Samengevat positioneren de bevindingen E9 als een prototype voor een nieuwe klasse van inflammasoomgerichte geneesmiddelen die werken door de interfaces tussen NLRP3-bouwstenen te verstoren in plaats van door het blokkeren van zijn energiegebruik of eindproducten. Hoewel het huidige werk beperkt is tot proefbuisexperimenten, computersimulaties en gekweekte cellen — en verdere studies in dieren en mensen noodzakelijk zijn — toont het aan dat zorgvuldig ontworpen kleine moleculen het inflammasoomskelet zelf kunnen herschikken. Voor patiënten met ziekten die worden aangedreven door weglopende ontsteking, zouden dergelijke op interfaces gerichte geneesmiddelen ooit preciezere controle kunnen bieden, schadelijke immuunactivatie naar beneden bijstellen terwijl essentiële verdedigingen grotendeels behouden blijven.
Bronvermelding: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
Trefwoorden: NLRP3-inflammasoom, pyrindomein, klein-molecuulremmer, aangeboren immuniteit, pyroptose