Clear Sky Science · nl
TTF2 als potentiële biomarker en immunotherapie‑doelwit bij de diagnose en prognose van gliomen
Waarom deze hersenkankerstudie ertoe doet
Hersentumoren die gliomen worden genoemd behoren tot de dodelijkste vormen van kanker; de meeste patiënten leven slechts enkele jaren na de diagnose. Artsen hebben dringend betere middelen nodig om te voorspellen hoe de ziekte zich zal ontwikkelen en om nieuwe behandelingsdoelen te vinden, vooral voor moderne immuungerichte therapieën. Deze studie richt zich op een weinig bekend molecuul, TTF2, en stelt een eenvoudige vraag met grote gevolgen: kunnen TTF2‑niveaus in hersentumoren artsen helpen gliomen nauwkeuriger te diagnosticeren, de overleving te voorspellen en mogelijk toekomstige immunotherapie te sturen?
Een nieuw signaal verborgen in tumorgenen
Glioma is geen eenduidige ziekte maar een gemengd gezelschap van hersentumoren die verschillen in groeisnelheid en behandelrespons. De huidige instrumenten, zoals microscopisch onderzoek en een beperkt aantal genetische merkers, verklaren niet volledig waarom sommige patiënten goed reageren terwijl anderen snel achteruitgaan. De onderzoekers gebruikten grote openbare kanker‑genendatabases uit de Verenigde Staten en China om naar aanvullende moleculaire aanwijzingen te zoeken. Ze concentreerden zich op TTF2, een eiwit dat betrokken is bij het uitschakelen van genactiviteit, dat in verband is gebracht met meerdere andere kankers maar nog niet grondig in gliomen was bestudeerd.
Hoge TTF2, hoger risico
Door duizenden monsters te vergelijken, vonden de onderzoekers dat TTF2‑niveaus veel hoger zijn in gliomweefsel dan in normaal hersenweefsel. Binnen gliomen bleken tumoren met de hoogste TTF2‑niveaus doorgaans verder gevorderd, tot agressievere subtypes te behoren en bij oudere patiënten voor te komen. Bij follow‑up van de patiëntuitkomsten werd een duidelijk patroon zichtbaar: mensen van wie de tumoren meer TTF2 bevatten, hadden over het algemeen een kortere totale overleving en vaker ziekteprogressie. Zelfs na correctie voor sterke bestaande merkers zoals tumorgradatie, IDH‑mutatiestatus en een chromosomale verandering genaamd 1p/19q‑codeletie bleef TTF2 een onafhankelijke waarschuwingsfactor. Het team stelde een voorspellingsgrafiek op waarin TTF2 werd gecombineerd met deze standaardfactoren, en die goed de werkelijke overleving na één, drie en vijf jaar overeenkwam in twee afzonderlijke patiëntendatasets.
Aanwijzingen uit de buurt van de tumor
Om te begrijpen waarom TTF2 mogelijk aan slechte uitkomsten is gekoppeld, onderzochten de onderzoekers welke andere genen parallel aan TTF2 omhoog of omlaag gaan en welke biologische processen die genensets vertegenwoordigen. Tumoren met hoge TTF2 toonden sterkere activiteit in routes die te maken hebben met immuunsignaalgeving, antistofproductie en cel‑tot‑celcommunicatie, evenals in bekende kankerpaden zoals PI3K–AKT. Met behulp van computationele tools die de samenstelling van immuuncellen afleiden uit genpatronen, analyseerden ze vervolgens het tumor‑micro‑milieu. Gliomen met veel TTF2 waren ook rijk aan bepaalde immuuncellen — Th2‑helper T‑cellen, macrofagen en neutrofielen — die vaak met een verzwakte of onderdrukte antitumorrespons worden geassocieerd, en hadden minder plasmacytoïde dendritische cellen, die juist kunnen helpen sterkere immuniteit op te wekken.
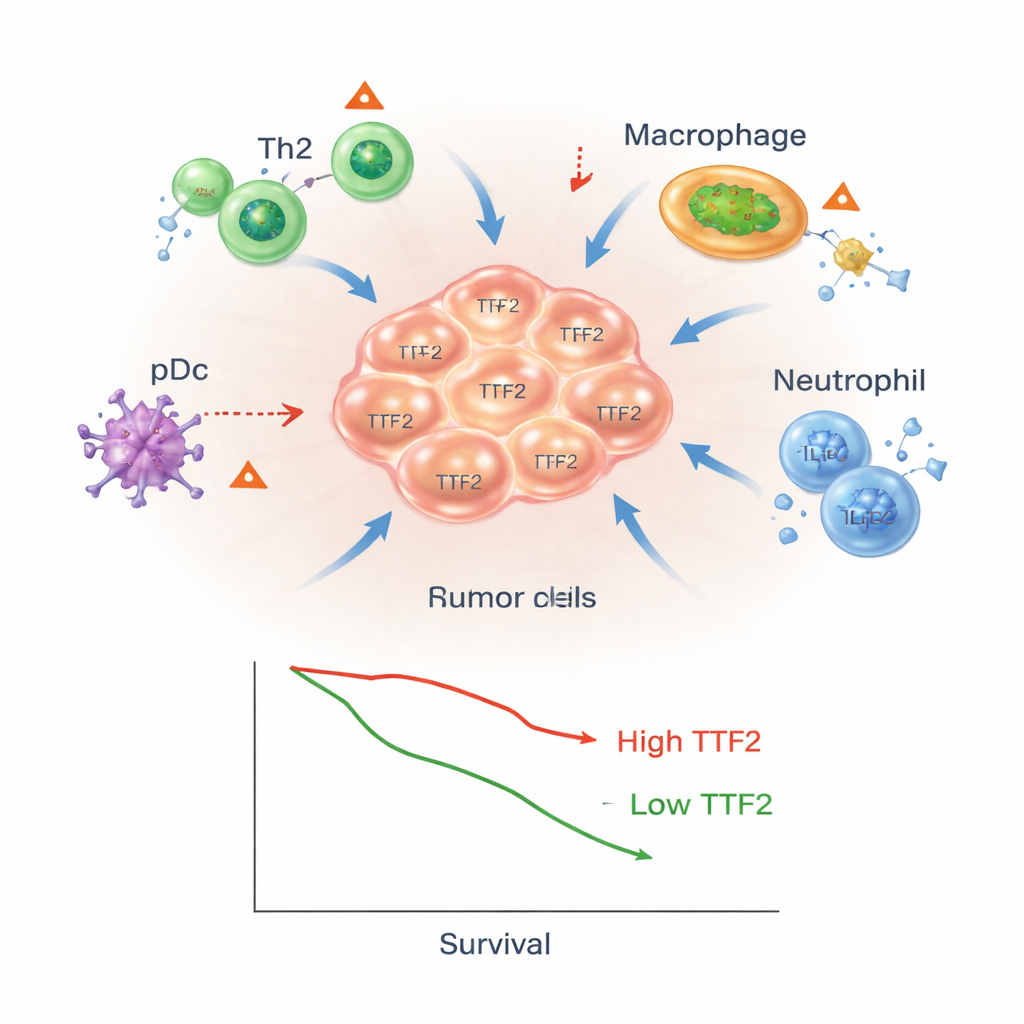
Hoe TTF2 tumoren zou kunnen helpen verbergen
Deze bevindingen suggereren dat TTF2 meer doet dan alleen gevaarlijke tumoren markeren; het kan actief meehelpen een beschermend schild rond tumoren te vormen. De auteurs stellen voor dat TTF2, door te beïnvloeden hoe genen worden uitgeschakeld, de niveaus van sleutelimmuunsignalen en chemokines kan veranderen — moleculen die immuuncellen aantrekken of afstoten. Daardoor zou de richting van T‑cellen kunnen verschuiven naar een Th2‑gedomineerde toestand die minder effectief is in het doden van kankercellen en de ophoping van tumor‑ondersteunende macrofagen en neutrofielen kunnen bevorderen. Hoewel deze ideeën voortkomen uit data‑analyse en niet uit directe laboratoriummanipulatie van TTF2, bieden ze een toetsbaar model voor hoe dit molecuul zowel tumorprogressie als immuunontsnapping zou kunnen bevorderen.
Wat dit betekent voor patiënten
De studie concludeert dat TTF2 sterk overgeproduceerd is in gliomen en dat hogere niveaus betrouwbaar geassocieerd zijn met slechtere overleving en agressievere ziektekenmerken. Voor patiënten schept dit twee hoopgevende mogelijkheden. Ten eerste zou het meten van TTF2 in tumormonsters artsen kunnen helpen de diagnose aan te scherpen en risicoschattingen te personaliseren, verder dan wat standaardtests tegenwoordig bieden. Ten tweede, als toekomstig laboratoriumonderzoek bevestigt dat TTF2 tumoren helpt het immuunsysteem te ontwijken, zouden geneesmiddelen die TTF2 of zijn downstreamroutes blokkeren of moduleren onderdeel kunnen worden van nieuwe combinatietherapieën die immunotherapie effectiever maken voor mensen met deze verwoestende hersenkanker.
Bronvermelding: Shi, D., Chen, F., Chen , Z. et al. TTF2 as a potential biomarker and immunotherapy target in glioma diagnosis and prognosis. Sci Rep 16, 7653 (2026). https://doi.org/10.1038/s41598-026-35049-9
Trefwoorden: glioma, TTF2, biomarker voor hersentumoren, tumor immuunmicro‑omgeving, doelwit voor immunotherapie