Clear Sky Science · nl
Moleculaire profilering van primaire versus gekoppelde asynchrone metastatische heldercelniercelcarcinoom onthult heterogeniteit in het tumor-immuummicro-omgeving
Waarom deze nierkankerstudie belangrijk is
Nierkanker zaait vaak uit naar andere delen van het lichaam, en moderne immunotherapieën werken niet voor iedere patiënt of ieder tumor even goed. Deze studie onderzoekt heldercelniercelcarcinoom — het meest voorkomende type nierkanker — om te zien hoe het immuunsysteem zich anders gedraagt in de oorspronkelijke nier-tumor vergeleken met latere metastasen. Inzicht in deze verschillen kan helpen verklaren waarom sommige tumoren beter op behandeling reageren dan andere en kan leiden tot nauwkeurigere, gepersonaliseerde zorg.
Een kijkje in primaire en metastatische tumoren
De onderzoekers concentreerden zich op 19 patiënten bij wie de nier-tumor (de primaire tumor) was verwijderd en die later metastasen ontwikkelden op locaties zoals long, bot, lever, bijnier, lymfeklieren of zacht weefsel. Van deze patiënten verzamelden ze 42 tumorexemplaren: 19 primaire tumoren en 23 niet-behandelde metastasen. Ze isoleerden RNA — een molecuul dat aangeeft welke genen actief zijn — uit dunne plakjes geconserveerd weefsel en gebruikten high-throughput sequencing om genexpressie over duizenden genen in elk monster vast te leggen. 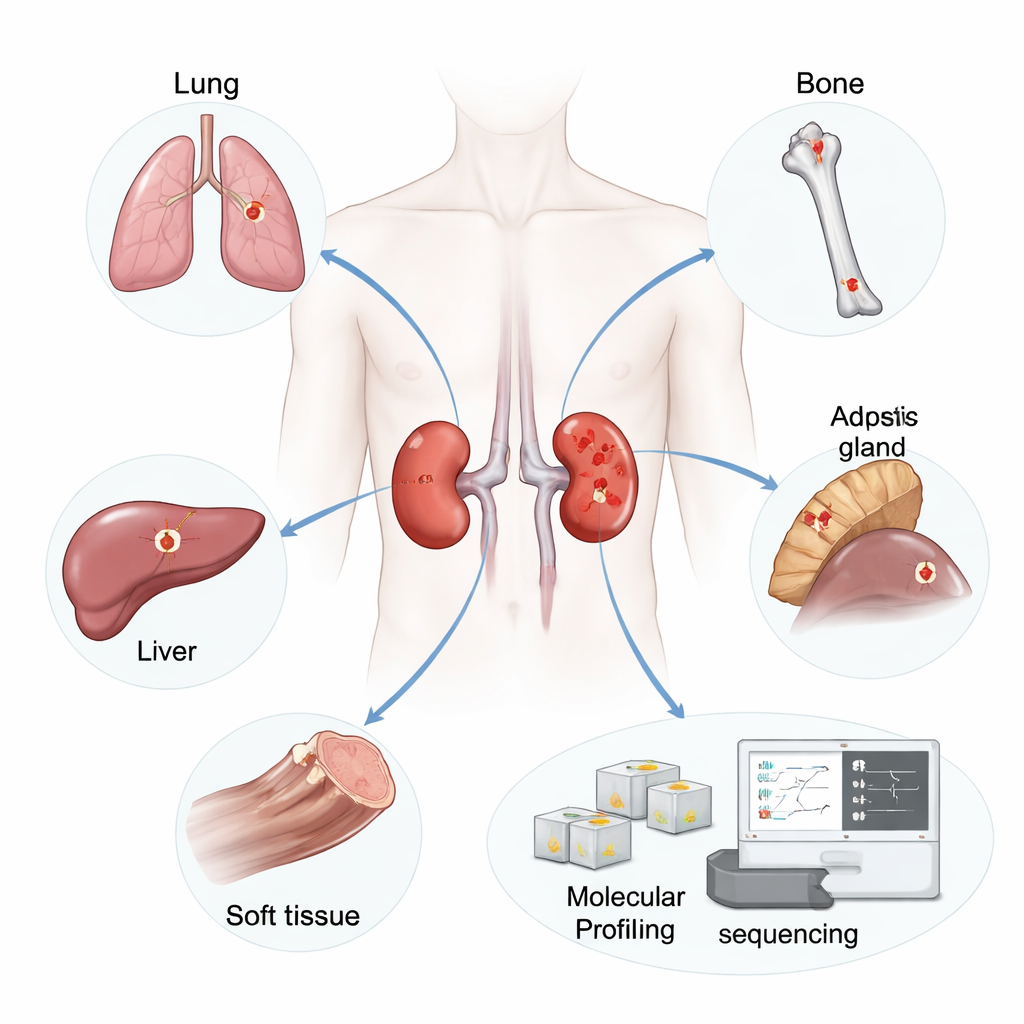
Primaire en metastatische tumoren zijn moleculair verschillend
Toen het team patronen van genactiviteit analyseerde, vonden ze dat primaire niertumoren de neiging hadden samen te clusteren en meer op elkaar leken dan op hun eigen metastasen. Met andere woorden: de metastase van een patiënt kon meer verschillen van de oorspronkelijke tumor van die patiënt dan van de metastase van een andere persoon. Duizenden genen waren hoger of lager actief in metastasen vergeleken met primairumoren. Metastatische tumoren toonden sterkere signalen van genprogramma’s die verbonden zijn aan snelle celdeling en agressief gedrag, inclusief paden betrokken bij celcycluscontrole en eiwitsynthese. Daarentegen waren primaire tumoren meer verrijkt voor stress- en signaleringsroutes zoals hypoxie (laag zuurstof) en ontstekingssignalen, wat wijst op andere biologische druk in de nier vergeleken met verre organen.
Het immuunlandschap verschuift naarmate kanker uitzaait
Naast ruwe genactiviteit schatten de wetenschappers welke typen immuuncellen in elk tumormonster aanwezig waren met een computationele methode die bulk-RNA gegevens ontleedt. Ze ontdekten een opvallend verschil: primaire niertumoren bevatten een significant hoger aandeel gereguleerde T-cellen (Tregs), een type immuuncel dat immuunreacties dempt en tumoren kan afschermen tegen aanvallen. Primairen hadden ook meer rustende dendritische cellen, monocyten, natural killer-cellen en CD8+ T-cellen. Daarentegen waren metastasen rijker aan zogenaamde M2-macrofagen — immuuncellen die vaak geassocieerd worden met wondheling en een tumorsupportieve in plaats van tumor-dodende omgeving — samen met meer plasmacellen en geactiveerde dendritische cellen. 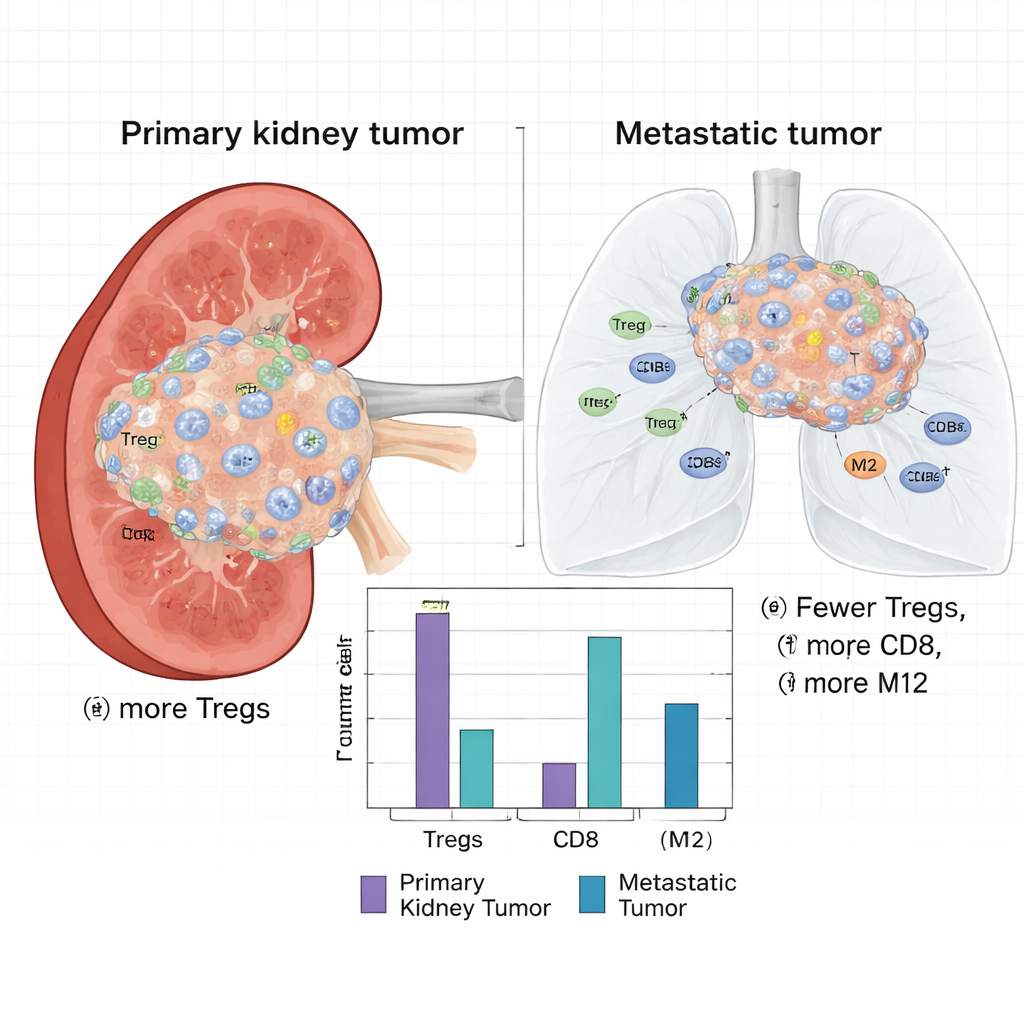
Long- en botmetastasen vertellen verschillende immuunverhalen
Toen de onderzoekers inzoemden op specifieke metastatische locaties, kwamen belangrijke nuances naar voren. Longmetastasen vertoonden verhoogde activiteit van gensets die verbonden zijn met celdelingscontrole (de G2M-checkpoint) en E2F-transcriptiefactoren, evenals hoge expressie van hornerine, een eiwit dat gekoppeld is aan bloedvatvorming in tumoren. Hun bijbehorende primaire niertumoren waren meer verrijkt voor hypoxie-gerelateerde genprogramma’s en bevatten opnieuw meer Tregs. Botmetastasen staken daarentegen uit door sterkere activering van epitheel–mesenchymale transitie, een proces dat kankercellen helpt mobieler en invasiever te worden. Deze botlaesies bevatten ook hogere niveaus M2-macrofagen, terwijl de primairen die hen voortbrachten verhoogde expressie van HHLA2 vertoonden, een recent erkend immuuncheckpointeiwit. Samen benadrukken deze bevindingen dat de immuun- en moleculaire omgevingen van metastasen niet alleen verschillen van primairen, maar ook van elkaar afhankelijk van de metastatische locatie.
Balans van immuuncellen en uitkomsten voor patiënten
Om te begrijpen wat deze immuunpatronen voor patiënten betekenen, raadpleegten de onderzoekers drie grote openbare datasets van heldercelniercelcarcinoom. Ze gebruikten dezelfde computationele methode om Treg- en CD8+ T-cel niveaus te schatten en koppelden deze vervolgens aan overlevingsuitkomsten. In de cohorts hadden mensen wiens tumoren een combinatie van lage CD8+ T-cellen (de belangrijkste tumor-dodende T-cellen) en hoge Tregs vertoonden, de neiging slechter te scoren wat betreft progressievrije of ziektespecifieke overleving, zelfs na correctie voor leeftijd, tumorgradatie en stadium. Hoewel het algemene stadium nog steeds sterk van invloed was op overleving, kwam de balans tussen onderdrukkende Tregs en aanvallende CD8+ cellen naar voren als een aanvullende risicomarker.
Wat dit betekent voor toekomstige nierkankerzorg
In toegankelijke bewoordingen laat deze studie zien dat de oorspronkelijke nier-tumor en zijn metastasen in verschillende immuun-"wijken" leven. De primaire tumor lijkt bijzonder goed in het aantrekken van vredehoudende cellen die het immuunsysteem kalmeren, wat deels kan verklaren waarom niertumoren in situ vaak minder goed op immunotherapie reageren dan metastatische afzettingen. Metastasen ontwikkelen ondertussen hun eigen lokale ondersteuningssystemen die per orgaan variëren. Deze inzichten suggereren dat artsen soms zowel de nier-tumor als metastasen moeten bemonsteren om de ziekte van een patiënt volledig te begrijpen, en dat behandelingen die immuuncheckpointremmers combineren met strategieën gericht op Tregs of M2-macrofagen de uitkomsten voor mensen met metastatisch heldercelniercelcarcinoom zouden kunnen verbeteren.
Bronvermelding: Cotta, B., Nallandhighal, S., Monda, S. et al. Molecular profiling of primary versus paired asynchronous metastatic clear cell renal cell carcinoma reveals heterogeneity in tumor immune microenvironment. Sci Rep 16, 5473 (2026). https://doi.org/10.1038/s41598-026-35021-7
Trefwoorden: nierkanker, tumormicro-omgeving, immunotherapie, metastase, regulerende T-cellen