Clear Sky Science · nl
Structurele basis voor diosgenine als inverse agonist van de retinoïnezuurreceptor-gerelateerde weesreceptor γ
Waarom een plantaire verbinding en een immuumschakelaar van belang zijn
Veel chronische aandoeningen — van auto-immuunziekten zoals multiple sclerose en psoriasis tot obesitas en type 2-diabetes — worden gedreven door overactieve immuunsignalen en verstoorde metabole signalen. Wetenschappers zoeken al lang naar veiligere middelen die deze signalen nauwkeurig kunnen bijstellen. Deze studie onderzoekt hoe diosgenine, een natuurlijke molecule die voorkomt in bepaalde geneeskrachtige planten en yams, zich vasthecht aan een immuunregulerend eiwit genaamd RORγ en het in een minder actieve toestand brengt. Inzicht in deze interactie op atomair niveau kan de deur openen naar zachtere, meer gerichte therapieën gebaseerd op een bekend planten-afgeleid bouwblok.
Een hoofdregelaar voor immuniteit en metabolisme
RORγ maakt deel uit van een grote familie van "nucleaire receptoren" — eiwitten in cellen die genen aan of uit zetten in reactie op kleine moleculen. Dit specifieke eiwit is een belangrijke regulator van een groep immuuncellen die bekendstaan als Th17-cellen; deze produceren het ontstekingssignaal IL-17A en worden in verband gebracht met auto-immuunziekten zoals multiple sclerose, psoriasis, reumatoïde artritis en de ziekte van Crohn. RORγ beïnvloedt ook hoe vetcellen zich ontwikkelen en hoe het lichaam reageert op insuline, waardoor het gelinkt is aan obesitas en diabetes. Vanwege dit brede bereik is RORγ een aantrekkelijk geneesmiddeldoelwit geworden, maar veel synthetische stoffen die eraan binden, stuiten op problemen met veiligheid, selectiviteit of werkzaamheid bij mensen.
Een traditioneel middel levert een veelbelovende lead op
Diosgenine is een steroid-achtig molecuul dat wordt gewonnen uit planten, waaronder soorten van Dioscorea (wilde yam) en verschillende traditionele medicinale kruiden. Het is bestudeerd op ontstekingsremmende, anti-kanker-, anti-diabetische en cardiovasculaire voordelen in cel- en diermodellen. Eerder onderzoek suggereerde dat diosgenine de RORα/γ-route kan beïnvloeden en schadelijke Th17-responsen kan onderdrukken, maar het was onduidelijk of het direct RORγ raakte en hoe het het gedrag van het eiwit zou veranderen. Om dat te achterhalen screenden de auteurs een bibliotheek van natuurlijke verbindingen met een gevoelige bindingsassay en identificeerden diosgenine als een sterke binder aan het ligandbindende gebied van RORγ.
Hoe diosgenine RORγ in omgekeerde stand zet
De onderzoekers onderzochten hoe diosgenine RORγ’s vermogen beïnvloedt om helper-eiwitten te recruteren die ofwel de genactiviteit versterken (coactivatoren) ofwel verzwakken (corepressoren). Verrassend genoeg moedigde diosgenine RORγ aan om beide typen partners te binden, een patroon dat verschilt van dat van een bekende natuurlijke antagonist, ursolzuur. In celgebaseerde reporter-assays die genregulatie volgen, verlaagde diosgenine consequent de RORγ-gedreven activiteit op een dosisafhankelijke manier, met potentie in het sub-micromolaire bereik. Dit gedrag past bij het profiel van een "inverse agonist": een verbinding die niet alleen de basale activiteit blokkeert maar ook actief de receptor in een uit-stand duwt, zelfs wanneer deze normaal gesproken aan zou staan.
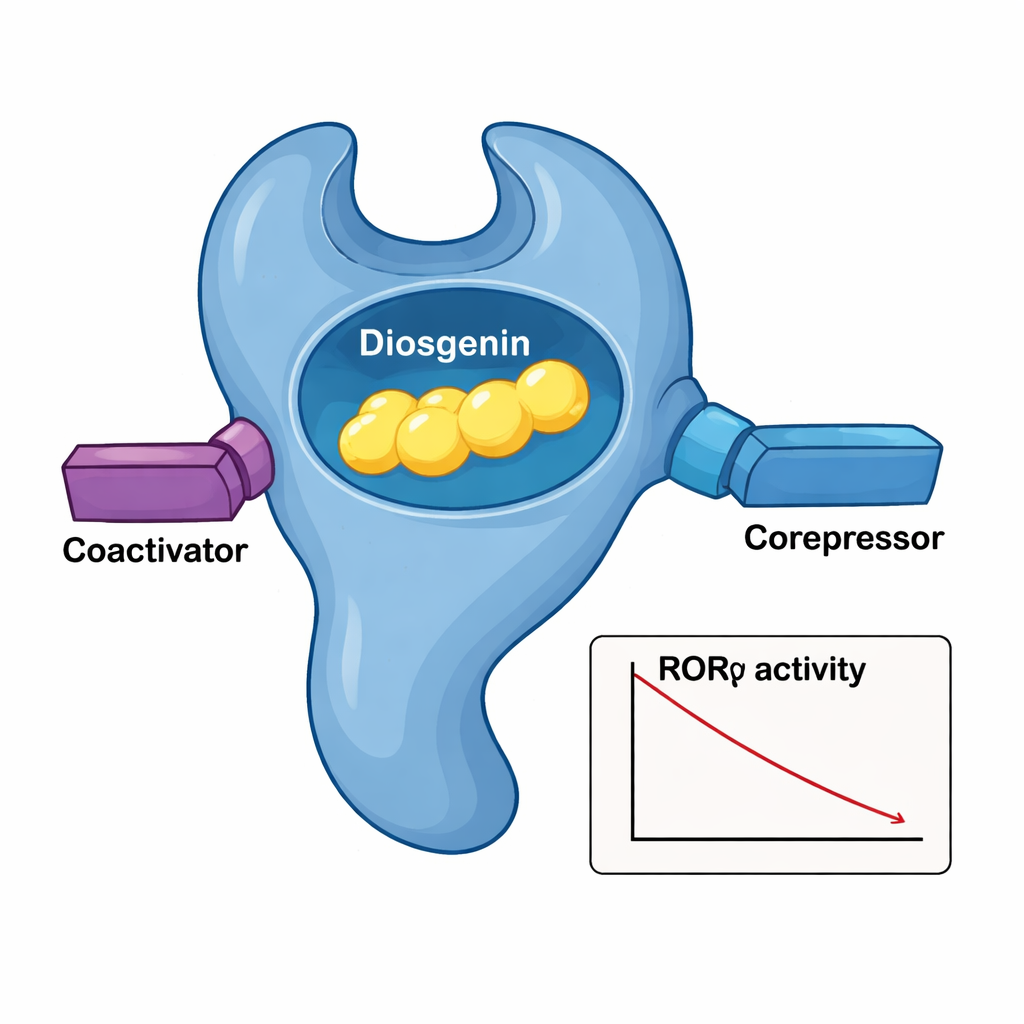
Een nadere blik op de moleculaire handdruk
Om precies te zien hoe diosgenine in RORγ past, loste het team de driedimensionale kristalstructuur op van het ligandbindende domein van het eiwit met diosgenine erin. De receptor vouwt zich tot een gelaagde bundel van helices en vormt een pocket die het steroid-achtige lichaam van diosgenine omsluit. Een netwerk van nauwe hydrofobe contacten van meerdere aminozuren werkt als een op maat gemaakte handschoen rond de rug van het molecuul, terwijl een kritische hydroxylgroep op diosgenine watergemedieerde waterstofbruggen vormt met twee arginine-residuen. Wanneer die pocketresiduen één voor één werden gewijzigd, daalde diosgenine’s vermogen om RORγ te onderdrukken, wat hun belang bevestigt. Structurele vergelijkingen met het RORγ–ursolzuurcomplex toonden aan dat diosgenine een sleutelhelix aan de staart (AF-2) in een "actief-achtige" positie houdt, terwijl het desondanks de algehele transcriptie naar beneden drijft, wat verklaart waarom het tegelijk zowel coactivatoren als corepressoren kan aantrekken.
Van kristalstructuur naar toekomstige medicijnen
Het gedetailleerde beeld van de diosgenine–RORγ-interactie benadrukt twee noemenswaardige voordelen voor geneesmiddeldesign. Ten eerste toont de pocket van de receptor voldoende flexibiliteit om verschillende ligandschikkingen te herkennen, wat betekent dat chemici diosgenine’s scaffold kunnen verfijnen om de selectiviteit voor RORγ te verbeteren en ongewenste binding aan andere nucleaire receptoren te verminderen. Ten tweede maken diosgenine’s natuurlijke oorsprong en de bekende lage inherente toxiciteit in preklinische modellen het een aantrekkelijk uitgangspunt vergeleken met sommige volledig synthetische verbindingen die in klinische proeven zijn vastgelopen. In eenvoudige bewoordingen laat dit werk zien hoe een plantaardig afgeleide molecule zich kan vastklampen aan een centrale immuun- en metabole schakelaar en deze in omgekeerde richting kan duwen, en levert het een structureel sjabloon voor het ontwikkelen van veiligere, effectievere behandelingen voor aandoeningen gerelateerd aan RORγ.
Bronvermelding: Chen, S., Tian, S., Liang, J. et al. Structural basis for diosgenin as an inverse agonist of retinoic acid receptor-related orphan receptor γ. Sci Rep 16, 4765 (2026). https://doi.org/10.1038/s41598-026-35006-6
Trefwoorden: ROR gamma, diosgenine, auto-immuunziekte, nucleaire receptor, inverse agonist