Clear Sky Science · nl
Transcriptomische karakterisering van afwijkende alternatieve spleising in skeletspieren van sarcopeniepatiënten
Waarom verouderende spieren kracht verliezen
Sarcopenie — het geleidelijke verlies van spiermassa en -kracht met de leeftijd — is een van de hoofdredenen dat ouderen moeite hebben met alledaagse taken, van traplopen tot boodschappen dragen. Deze studie duikt in verouderende spierweefsels op het niveau van RNA, de boodschappen die cellen vertellen welke eiwitten ze moeten maken. De auteurs tonen aan dat bij sarcopenie veel van deze RNA-boodschappen op abnormale manieren worden geknipt en aan elkaar gezet, wat mogelijk de energieproductie in de spier verstoort en wijst op nieuwe behandelroutes.
Spierverlies en het geniale “bewerkingssysteem” van het lichaam
Onze genen zijn geschreven in DNA, maar cellen werken met RNA-kopieën van die genen. Voordat een RNA-boodschap wordt gebruikt, trimmen en spleisen cellen die normaal gesproken — vergelijkbaar met het monteren van een film — zodat één gen meerdere varianten van een eiwit kan produceren. Dit proces, alternatieve spleising genoemd, is bijzonder actief in spierweefsel, dat nauwkeurig afgestemde eiwitten nodig heeft om samen te trekken, te herstellen en zich aan inspanning aan te passen. Wanneer spleising misgaat, kunnen verkeerde eiwitvarianten worden geproduceerd of belangrijke varianten verloren raken, wat bijdraagt aan ziekten zoals spierdystrofie en sommige hersenaandoeningen. De auteurs vermoeden dat een vergelijkbare, verborgen laag van RNA-misbewerking sarcopenie kan aandrijven.
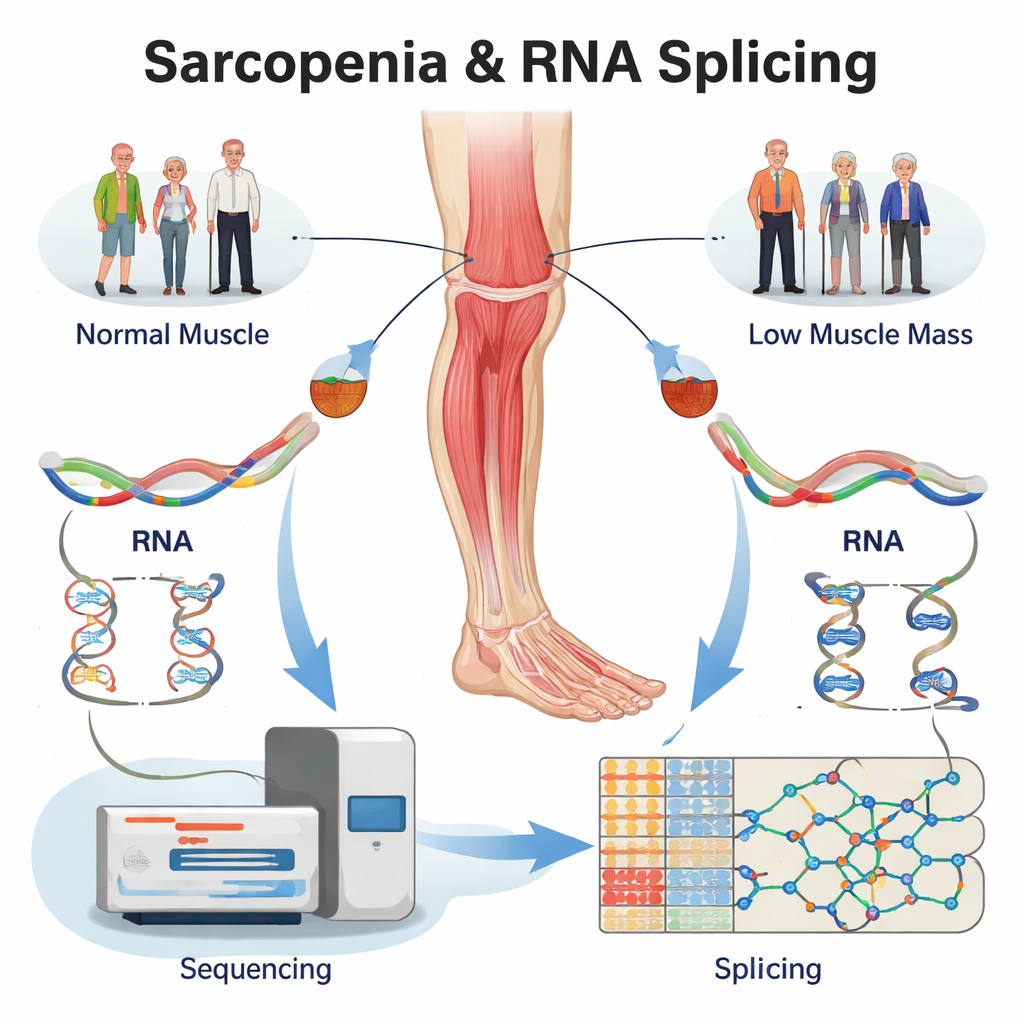
Hergebruik van bestaande data om verborgen RNA-fouten te vinden
In plaats van nieuwe vrijwilligers te werven, heranalyseerde het team een bestaande grote RNA-sequencingdataset van menselijke biopten uit de dijspier. De monsters kwamen uit vier groepen: ouderen met duidelijke sarcopenie, mensen met alleen een lage spiermassa, mensen met alleen lage spierkracht, en leeftijdsgematchte gezonde controles. Met gespecialiseerde software bevestigden ze eerst dat honderden genen in de zieke spieren omhoog- of omlaaggaan in expressie. Belangrijker nog, vervolgens onderzochten ze hoe het RNA van elk gen werd gespleisd en catalogueerden meer dan 5.000 spleiswijzigingen in de drie probleemgroepen vergeleken met gezond spierweefsel. Deze veranderingen concentreerden zich in een paar basispatronen — zoals het overslaan van een exon of het kiezen van een alternatieve knipplaats — patronen die bekendstaan om sterk de eiwitstructuur te veranderen.
Energiecentrales en cellulair “brandstofmeter”-routes zijn verstoord
De spleiswijzigingen kwamen voor in genen die centraal staan in de spierbiologie. Veel getroffen genen bouwen onderdelen van de mitochondriën, de kleine energiecentrales die spiercontractie aandrijven. In sarcopene spieren toonden 16 genen betrokken bij oxidatieve fosforylering — het proces dat voedingsstoffen omzet in bruikbare energie — gewijzigde spleising, vooral componenten van de mitochondriale complexen die elektronen transporteren en protonen pompen. Andere veranderingen verschenen in genen die NAD⁺ maken of gebruiken, een sleutelmolecuul voor cellulaire energie en herstel. In plaats van simpelweg meer of minder aanwezig te zijn, produceerden belangrijke enzymen zoals CD38, PARP2 en verschillende sirtuïnen verschillende RNA-varianten, wat suggereert dat de balans tussen NAD⁺-productie en -consumptie verstoord is op spleisingsniveau. De aangetaste genen clusterden ook in bekende signaalroutes in spieren, waaronder AMPK- en FoxO-pathways, die fungeren als cellulaire brandstofmeters en stressresponsoren.
Gedeelde patronen in verschillende stadia — en over soorten heen
Opvallend was dat veel van dezelfde genen spleiswijzigingen toonden niet alleen bij mensen met volledige sarcopenie, maar ook bij degenen met alleen lage spiermassa of alleen lage kracht. Dit suggereert dat abnormale spleising vroeg begint en de verschillende klinische verschijningsvormen van de ziekte overstijgt. Om te testen of deze veranderingen in een diermodel konden worden gereproduceerd, induceerden de onderzoekers spierafbraak bij muizen met het steroid dexamethason, een gebruikelijke manier om sommige kenmerken van sarcopenie na te bootsen. De muizen ontwikkelden een zwakkere grijpkracht en slechtere prestaties bij rennen en balanstests. Toen het team het muizenspier-RNA sekwenseerde, vonden ze opnieuw honderden genen met gewijzigde spleising. Ongeveer een vijfde daarvan overlapt met de menselijke sarcopeniegenen, en veel waren betrokken bij het regelen van transcriptie, chromatinestructuur en spleising zelf — hogere niveau schakelaars die het volledige eiwitproduct van een cel kunnen hervormen.
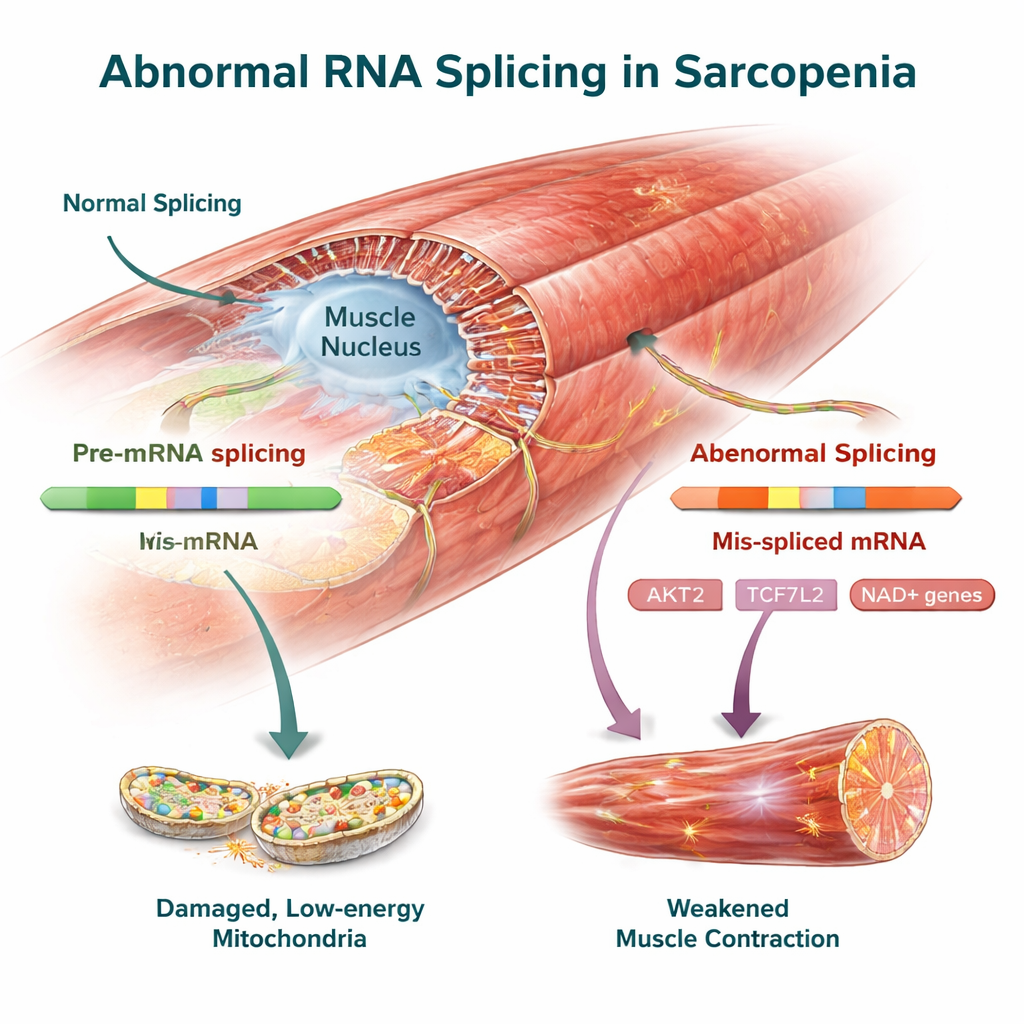
Belangrijke spiergecontrolegenen als potentiële behandeldoelen
Onder de soortoverschrijdende veranderingen zaten meerdere genen die al met spiergezondheid in verband zijn gebracht. AKT2, een centrale regulator van groei en eiwitopbouw in spier, toonde duidelijke spleisveranderingen bij zowel mensen als muizen die mogelijk zijn vermogen om spiermassa te behouden verminderen. TCF7L2, onderdeel van de Wnt-signaleringsroute, samen met FMNL2 en USP40, die helpen bij het organiseren van het interne geraamte van de spier en eiwitkwaliteitscontrole, droegen ook gewijzigde RNA-varianten. Het team bevestigde deze spleiswijzigingen experimenteel in muizenpieren, wat versterkt dat het echte kenmerken van de ziekte zijn en geen artefacten van data-analyse.
Wat dit betekent voor het voorkomen van kwetsbaarheid
Voor niet-specialisten is de boodschap dat sarcopenie niet alleen gaat over spieren die “verslijten” of genen die aan- of uitgaan. Het omvat ook een wijdverspreide misbewerking van RNA-boodschappen die sturen hoe spiercellen hun machinerie maken en onderhouden, vooral de systemen die energie genereren en stress waarnemen. Omdat spleising in principe te corrigeren is met nauwkeurig ontworpen RNA-gebaseerde geneesmiddelen, bieden de hier ontdekte geconserveerde spleisfouten — met name in genen zoals AKT2 en TCF7L2 — een nieuwe reeks aanknopingspunten voor therapieën om verouderende spieren langer sterker te houden.
Bronvermelding: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
Trefwoorden: sarcopenie, spierveroudering, RNA-spleising, mitochondriën, AKT2