Clear Sky Science · nl
Fenomenologisch model van stabilisatie van transthyretine
Waarom dit belangrijk is voor patiënten en families
Transthyretine-amyloïdose is een ernstige aandoening waarbij een normaal bloedproteïne, transthyretine (TTR), uiteenvalt en de fragmenten zich kunnen ophopen als schadelijke afzettingen in het hart en de zenuwen. Nieuwe medicijnen zoals tafamidis en acoramidis zijn ontworpen om dit eiwit in zijn veilige, viervoudige vorm te houden en hebben al de uitkomsten voor veel mensen verbeterd. Artsen zien echter een raadselachtig effect bij behandelde patiënten: de TTR-spiegels in het bloed stijgen met meer dan 30%, en het is niet duidelijk waarom. Dit artikel gebruikt een vereenvoudigd, wiskundig model om te onderzoeken wat er mogelijk in het lichaam gebeurt en wat dat betekent voor de manier waarop deze geneesmiddelen werkelijk werken. 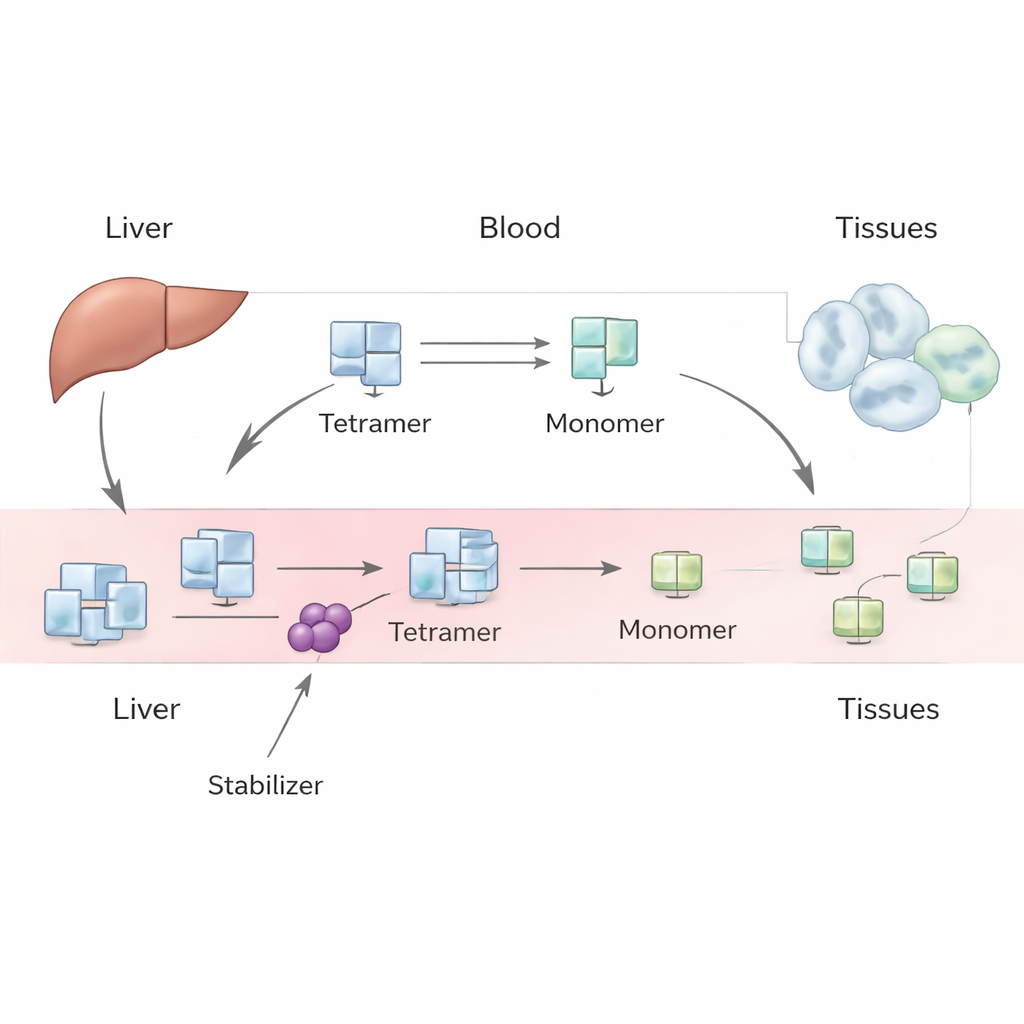
Een eiwit dat kan helpen of schaden
TTR wordt voornamelijk in de lever gemaakt en circuleert normaal in het bloed als een stabiele bundel van vier identieke subunits, een tetramer genaamd. Het vervoert schildklierhormoon en vitamine A. Onder bepaalde omstandigheden, waaronder veroudering of erfelijke genvarianten, kan dit tetramer uiteen vallen in losse subunits, of monomeren. Deze monomeren kunnen misvouwen en samenklonteren tot amyloïde fibrillen, die weefsels beschadigen en leiden tot transthyretine-amyloïdose van het hart (cardiomyopathie) of de zenuwen (neuropathie). Geneesmiddelen zoals tafamidis en acoramidis zijn ontworpen om aan het tetramer te binden en het moeilijker te maken voor het uiteen te vallen, waardoor de ziekteloop vertraagt. Wanneer patiënten echter met deze medicijnen beginnen, stijgen hun gemeten TTR-niveaus in het bloed voorspelbaar, en die toename is groter dan simpele laboratoriumexperimenten zouden suggereren.
Een eenvoudig beeld van een complex systeem bouwen
De auteurs pakken dit raadsel aan met een fenomenologisch model — een model dat zich richt op het algehele observeerbare gedrag in plaats van elk microscopisch detail. In hun raamwerk produceert de lever TTR-tetrameren met een constante snelheid, die vervolgens in de bloedbaan terechtkomen. Eenmaal in circulatie kunnen tetrameren dissociëren tot monomeren en weer assembleren, en zowel tetrameren als monomeren kunnen uit het bloed worden verwijderd door opname in weefsels en afbraak. Door een paar massabalansvergelijkingen voor tetrameren en monomeren op te stellen, verkent het team verschillende scenario’s: één waarin monomeren vooral weer tetrameren vormen, één waarin ze snel worden verwijderd, en een intermediair geval waarin beide processen belangrijk zijn. Ze gebruiken historische humane tracerstudies en moderne laboratoriumdata om sleutelvariabelen te schatten, zoals hoe snel tetrameren worden geklaard, hoe snel ze uiteen vallen en hoe sterk geneesmiddelen dit uiteenvallen vertragen.
Waarom alleen tetramerstabilisatie niet genoeg is
Gewapend met deze schattingen stellen de onderzoekers een gerichte vraag: als een geneesmiddel perfect zou voorkomen dat tetrameren uiteen vallen, hoeveel zou het TTR-gehalte in het bloed dan stijgen? In alle plausibele regimes is het antwoord beperkt — in de orde van 15% hoogstens voor typische parameterwaarden, en vaak minder, afhankelijk van hoe monomeren worden verwerkt. Dit blijft ver onder de >30% stijging die bij behandelde patiënten wordt waargenomen. De discrepantie blijft zelfs als men ruime onzekerheid in de bekende parameters toelaat. Het model suggereert daarom dat het simpelweg vertragen van tetramer-uiteenvallen op zichzelf niet het volledige klinische effect kan verklaren. Andere processen die bepalen hoe snel TTR wordt gemaakt, opgenomen door cellen of afgebroken, moeten ook veranderen wanneer stabiliserende geneesmiddelen aanwezig zijn. 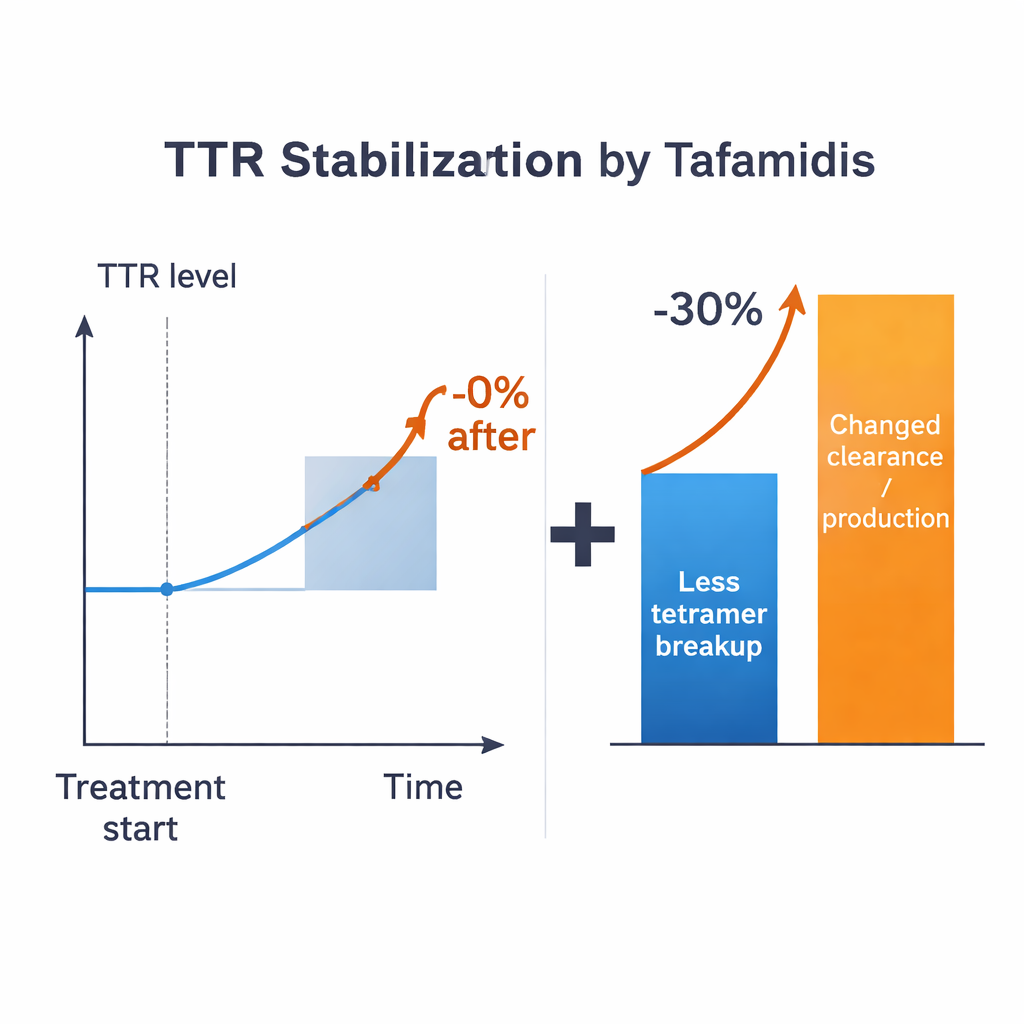
Aanwijzingen uit medicijnspiegels en slimme experimenten
Om de blootstelling aan het geneesmiddel te koppelen aan TTR-gedrag combineren de auteurs een basis farmacokinetisch model van tafamidis (hoe het medicijn zich in de tijd door het lichaam gedraagt) met gespecialiseerde “subunit-uitwisselings” assays. In deze experimenten worden gelabelde en ongelabelde TTR-tetrameren gemengd in menselijk plasma, en de geleidelijke uitwisseling van subunits onthult hoe vaak tetrameren uiteen vallen. Het meten van dit proces bij verschillende medicijnconcentraties levert een directe, op data gebaseerde koppeling tussen het tafamidisniveau en de effectieve tetramerstabiliteit, zonder te hoeven weten hoeveel medicijn aan albumine of schildklierhormoon gebonden is. Deze fenomenologische koppeling voedt het model en omzeilt op elegante wijze veel biochemische onbekenden. Toch beperken de berekeningen zelfs met dit voordeel de verwachte stijging van TTR tot ongeveer de helft van de klinisch waargenomen toename, wat het idee bestendigt dat veranderingen in klaring, internalisatie, afbraak of zelfs synthese deel van het verhaal moeten uitmaken.
Wat dit betekent voor de toekomst
Voor niet-specialisten is de kernboodschap dat deze stabiliserende geneesmiddelen waarschijnlijk meer doen dan alleen TTR-tetrameren “aan elkaar plakken”. Ze beïnvloeden waarschijnlijk ook hoe het lichaam het eiwit produceert, verwijdert of recyclet. De auteurs betogen dat eenvoudige, transparante modellen zoals het hunne krachtig zijn omdat ze zulke hiaten in ons begrip blootleggen en wijzen op concrete experimenten — bijvoorbeeld het direct meten van hoe snel monomeren worden geklaard, hoe snel verschillende vormen van TTR door cellen worden opgenomen, of of medicijngebonden TTR anders wordt behandeld dan niet-gebonden eiwit. Beter inzicht in deze vragen zou niet alleen de behandeling van transthyretine-amyloïdose verfijnen, maar mogelijk ook algemene principes onthullen over andere ziekten waarbij normale eiwitten veranderen in schadelijke aggregaten.
Bronvermelding: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
Trefwoorden: transthyretine-amyloïdose, eiwitstabilisatie, tafamidis, farmacokinetisch modelleren, amyloïde ziekten