Clear Sky Science · nl
Gerichte stabilisatie van hypoxie-induceerbare factor 1-alfa (HIF1A) tijdens in vitro rijping van boviene cumulus-oöcytcomplexen verhoogt blastocystenpercentages
Waarom het aanpassen van zuurstofsensatie in eicellen ertoe doet
Moderne veeteelt is sterk afhankelijk van in het laboratorium gemaakte embryo’s, maar succes is verre van gegarandeerd: slechts ongeveer een derde van de oöcyten bereikt het cruciale blastocyststadium, wanneer ze klaar zijn om in een koe te worden ingebracht. Deze studie stelt een schijnbaar eenvoudige vraag met brede betekenis voor dierenfokkerij en geassisteerde voortplanting: als we de lage-zuurstofcondities die eicellen natuurlijk in de eierstok ervaren beter nabootsen—door voorzichtig een belangrijk zuurstofsensor-eiwit te versterken—kunnen we dan meer embryo’s succesvol laten ontwikkelen?
Het leven begint in een laagzuurstofniche
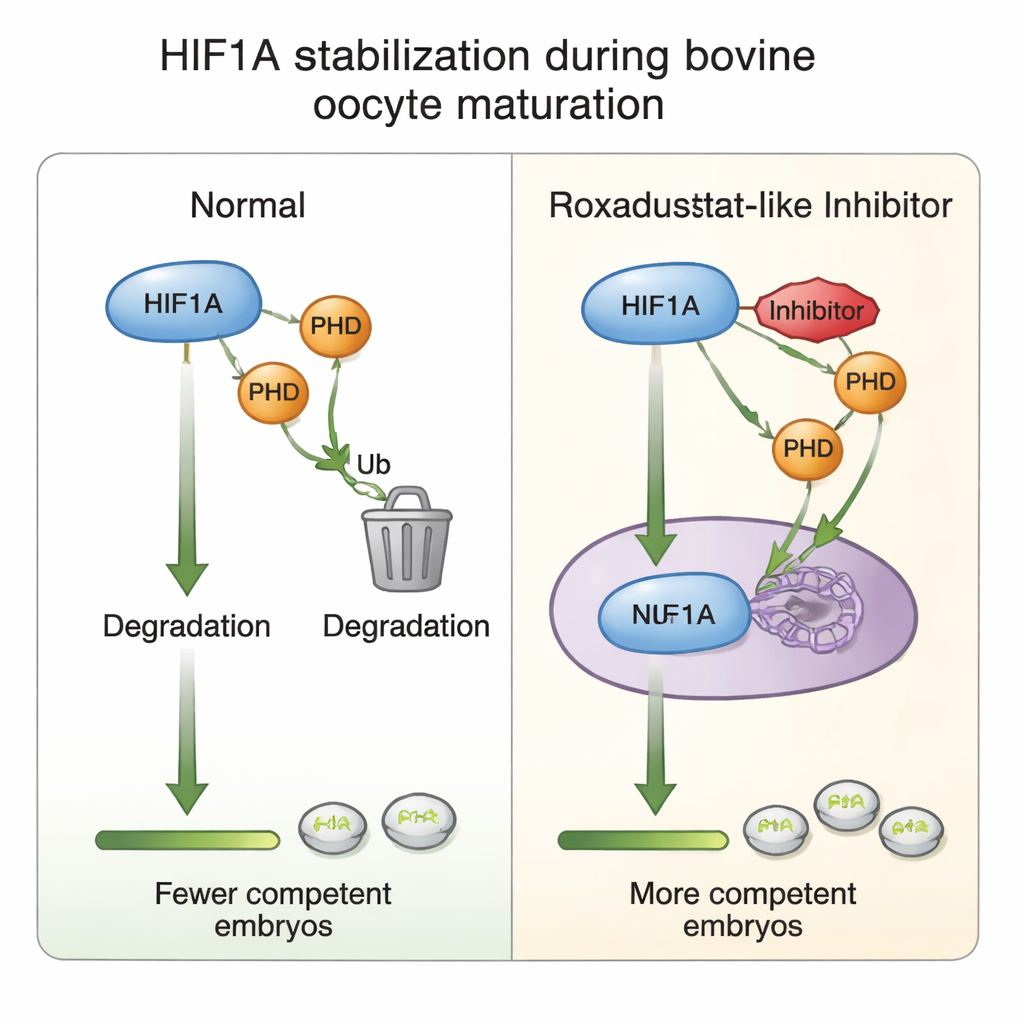
In de eierstok wordt iedere zich ontwikkelende eicel omgeven door een ondersteunende cluster van cellen, de cumulus, samen vormend een cumulus–oöcytcomplex. Hoewel de eierstok beter van bloed wordt voorzien naarmate follikels groeien, reiken bloedvaten niet tot in de directe omgeving van de eicel. Zuurstof moet diffunderen, waardoor er een licht laagzuurstof- of hypoxisch milieu rond de rijpende eicel ontstaat. In deze niche helpt een intracellulaire sensor, HIF1A, cellen zich aan te passen door metabolisme en hormoonproductie bij te sturen. Eerder werk toonde dat het blokkeren van HIF1A de oöcytrijping schaadt en de embryovorming drastisch vermindert, wat dit eiwit aanwijst als een centrale coördinator van eicelkvaliteit—het vermogen van een eicel om bevrucht te worden en zich tot een gezond embryo te ontwikkelen.
Een medicijn gebruiken om de zuurstofsensor van de eicel fijn af te stellen
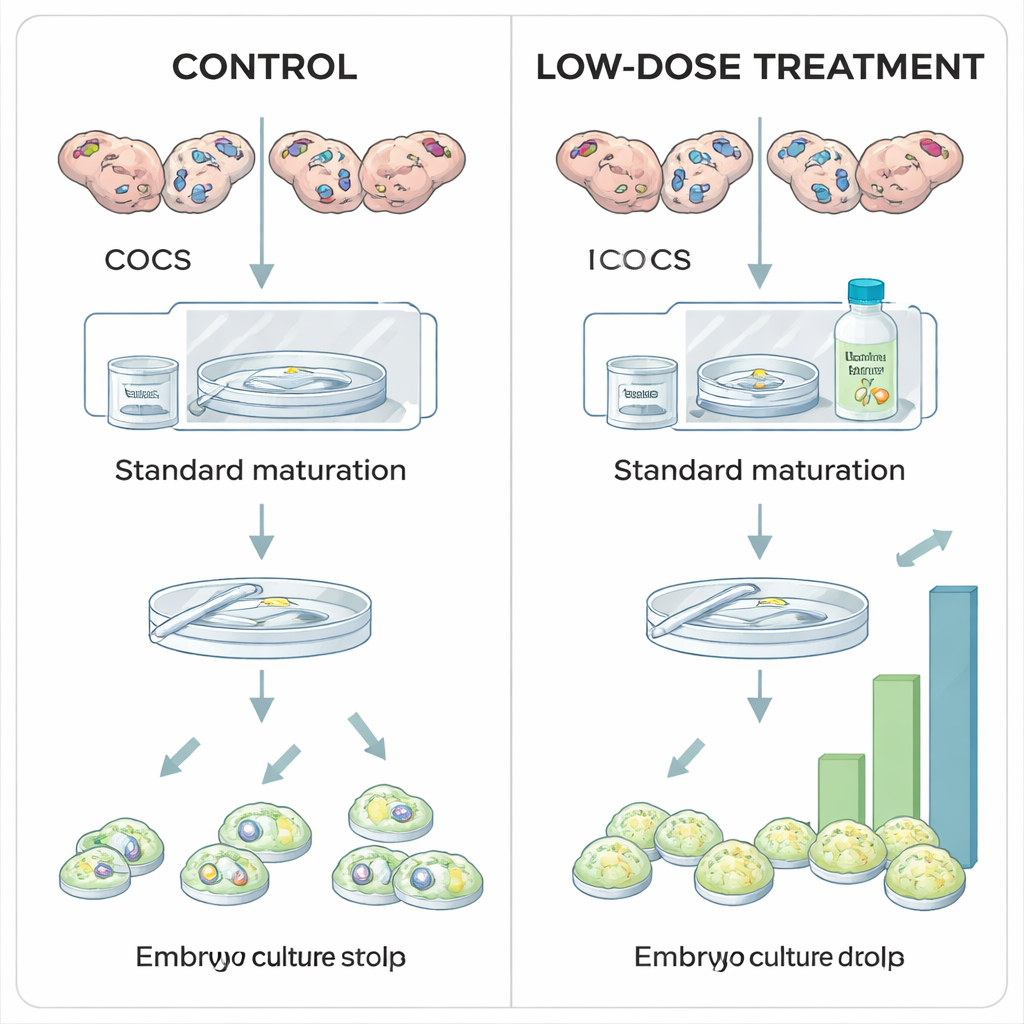
De onderzoekers onderzochten of het matig stabiliseren van HIF1A tijdens laboratoriumrijping van boviene eicellen de embryo-opbrengst kan verhogen. In standaard in vitro-protocollen worden cumulus–oöcytcomplexen gerijpt onder normale luchtzuurstofniveaus, grotendeels om praktische redenen in plaats van biologische. In deze studie werden eicellen, verzameld uit slachthuisovaria, verdeeld in groepen en tijdens hun 24 uur durende rijpingsperiode blootgesteld aan verschillende doses Roxadustat, een geneesmiddel dat al in de menselijke geneeskunde wordt gebruikt tegen bloedarmoede. Roxadustat werkt door een familie enzymen, prolyl-hydroxylasen (PHDs), te remmen; deze enzymen markeren HIF1A normaal gesproken voor afbraak wanneer zuurstof ruim aanwezig is. Door PHDs te remmen kan HIF1A-eiwit zich ophopen, zelfs bij hogere zuurstofniveaus, en wordt het hypoxiesignaal gereconstrueerd dat de eicel in vivo zou ervaren.
Meer blastocysten bij de juiste dosis, schadelijk bij hogere niveaus
Toen het team onderzocht hoe eicellen en embryo’s er na behandeling voorstonden, verscheen een duidelijk patroon. Een lage dosis Roxadustat (25 micromolair) veranderde niet hoeveel eicellen de rijping voltooiden of hoeveel bevruchte eicellen begonnen te delen, maar verhoogde wel significant het aandeel dat het blastocyststadium bereikte. Met andere woorden: vroege stappen bleven onaangetast, maar meer embryo’s voltooiden succesvol de veeleisende weg naar blastocystvorming—wat erop wijst dat bescheiden HIF1A-stabilisatie de intrinsieke kwaliteit van de eicel verbetert. Daarentegen verlaagde de hoogste dosis (100 micromolair) het percentage eicellen dat überhaupt rijpte, en wanneer dezelfde remmer later werd toegepast, tijdens de acht dagen durende embryo-kweekperiode, verminderden hoge doses scherp de blastocystvorming zonder de vroege celdelingen te veranderen. Deze bevindingen geven aan dat "precies genoeg" HIF1A-activiteit tijdens rijping gunstig is, terwijl te veel of te langdurige activatie schadelijk is.
Wat er gebeurt in de ondersteunende cellen van de eicel
Om te begrijpen hoe deze chemische afstelling werkt, onderzochten de auteurs de cumuluscellen die elke eicel omringen. Ze vonden dat rijping in het algemeen de HIF1A-genactiviteit verhoogt, maar dat toevoeging van Roxadustat paradoxaal genoeg HIF1A-messenger RNA verlaagde terwijl de HIF1A-eiwitniveaus onveranderd bleven—een aanwijzing dat cellen de genuitvoer kunnen dempen zodra het eiwit voldoende gestabiliseerd is, een soort ingebouwde rem tegen overactivering. De niveaus van PHD2, het meest zuurstofgevoelige van de PHD-enzymen, stegen als reactie op het middel, wat zijn rol als onderdeel van de zuurstof-sensorlus versterkt. Bij hogere medicatiedoses waren marker voor celproliferatie en voor de kleverige matrix die helpt dat cumuluscellen rond de eicel uitbreiden gereduceerd, in lijn met de waargenomen afname in rijping en embryovorming. Dit alles ondersteunt het idee dat zorgvuldig gebalanceerde HIF1A-activiteit de dialoog tussen eicel en cumuluscellen fijn afstemt en zo de latere ontwikkelingssucces beïnvloedt.
Implicaties voor veeteelt en daarbuiten
Dit werk laat zien dat het zacht stabiliseren van de zuurstofsensor van de eicel tijdens het korte venster van in vitro-rijping blastocystopbrengsten bij runderen zinvol kan verhogen en stabiliseren, zonder bevruchting of vroege klieving te veranderen. In praktische termen zou dat kunnen leiden tot betrouwbaardere embryo-productie voor fokprogramma’s, met gebruik van een gericht geneesmiddel in plaats van grove aanpassingen van zuurstofniveaus of giftigere chemicaliën. De studie benadrukt ook een bredere les relevant voor menselijke vruchtbaarheidsbehandelingen: het nabootsen van de genuanceerde, laagzuurstofomgeving van de eierstok is niet louter een kwestie van zuurstof omhoog of omlaag zetten, maar van het respecteren van de fragiele balans van signaalmoleculen zoals HIF1A. Het fijnafstellen van die balans, in plaats van het tot het uiterste te pushen, kan een belangrijke route naar gezondere embryo’s zijn.
Bronvermelding: Gübeli, M., Bleul, U. & Kowalewski, M.P. Targeted hypoxia-inducible factor 1-alpha (HIF1A) stabilization during in vitro maturation of bovine cumulus-oocyte complexes increases blastocyst rates. Sci Rep 16, 7554 (2026). https://doi.org/10.1038/s41598-025-33894-8
Trefwoorden: in vitro embryo-productie, oöcytrijping, hypoxiesignalering, HIF1A-stabilisatie, rundveereproductie