Clear Sky Science · nl
Computerondersteunde diagnose van neonatale acute bilirubine-encefalopathie met multimodale MRI-beelden en convolutionele neurale netwerken
Waarom dit ertoe doet voor pasgeborenen en hun gezinnen
Geelzucht komt veel voor bij pasgeborenen en is meestal onschuldig, maar bij sommige zuigelingen kan een ophoping van het gele pigment bilirubine de hersenen onopgemerkt beschadigen. Artsen vinden het moeilijk om alleen op scans en bloedtests te bepalen welke geelzuchtige baby’s echt gevaar lopen. Deze studie onderzoekt of slimme computertools hersenscans nauwkeuriger kunnen interpreteren dan het menselijk oog, zodat artsen baby’s kunnen beschermen tegen blijvende beperkingen en tegelijkertijd onnodige ongerustheid en behandeling kunnen vermijden.
Het verborgen gevaar achter pasgeboren geelzucht
De meeste baby’s ontwikkelen enige mate van geelzucht terwijl hun onrijpe lever leert bilirubine uit het bloed te verwijderen. Wanneer bilirubinespiegels zeer hoog worden, kan het pigment in gevoelige diepe structuren van de hersenen terechtkomen en een aandoening veroorzaken die acute bilirubine-encefalopathie heet, wat kan leiden tot blijvende problemen met beweging, gehoor en leren als het niet tijdig wordt behandeld. Het probleem is dat vroege hersenschade subtiel en omkeerbaar kan zijn, en dat huidige bed-side scores en bloedtesten onvolmaakt zijn. Magnetic resonance imaging (MRI) biedt een niet-invasief venster op de pasgeboren hersenen, maar zelfs specialisten vinden vaak dat aangedane en niet-aangedane baby’s verrassend vergelijkbaar lijken op standaardbeelden.
De hersenen bekijken met meer dan één bril
Traditionele MRI voor deze baby’s richt zich vooral op één type beeld, bekend als T1-gewogen beelden, waar de globus pallidus — een kleine, diepe regio die betrokken is bij beweging — ongewoon helder kan lijken wanneer deze door bilirubine is aangetast. Eerder werk toonde aan dat alleen deze beelden lezen, zelfs met eenvoudige computermetingen of oudere deep-learningmodellen, ruimte voor fouten liet. De auteurs stelden dat andere MRI-“smaken”, zoals T2-gewogen beelden en diffusie-gebaseerde kaarten die volgen hoe water zich door hersenweefsel beweegt, extra aanwijzingen zouden kunnen bevatten. In plaats van artsen handmatig specifieke regio’s te laten meten, wilden ze de volledige rijkdom van deze drie beeldtypen invoeren in moderne beeldherkenningsalgoritmen.
Computers leren vroege hersenschade te herkennen
Het onderzoeksteam verzamelde hersenscans van 150 pasgeborenen met hoge bilirubinespiegels: de helft had tekenen van acute hersenbetrokkenheid en de andere helft niet. Voor elke baby werden drie MRI-series verkregen — T1, T2 en een diffusie-gebaseerde kaart genaamd apparent diffusion coefficient (ADC). Eerst werden de beelden zorgvuldig uitgelijnd en bijgesneden zodat alleen de hersenen overbleven, vervolgens van formaat veranderd en helderheid-genormaliseerd zodat ze door standaard beeldanalyse-software verwerkt konden worden. De wetenschappers probeerden twee brede strategieën. De ene steunde op een klassiek machine-learningmethode genaamd support vector machine, met eenvoudige handmatige helderheidsverhoudingen tussen een kwetsbare diepe structuur (de globus pallidus) en het nabijgelegen witte stof. De andere gebruikte krachtige deep-learningmodellen, InceptionV3 en EfficientNetB0, die hun eigen visuele kenmerken rechtstreeks uit de ruwe beelden leren.
Het combineren van scantypen geeft het duidelijkste beeld
Toen het team de methoden vergeleek, verbeterde de eenvoudigere, handmatig gemeten aanpak enigszins wanneer meerdere scantypen werden gecombineerd, maar de beste prestaties bleven achter bij wat comfortabel zou zijn voor klinische besluitvorming. Daarentegen verbeterden de deep-learningmodellen dramatisch naarmate meer MRI-typen werden samengevoegd. Door T1-, T2- en ADC-beelden samen te stapelen als drie kleurkanalen in een foto, onderscheidde het best presterende netwerk (InceptionV3) aangedane van niet-aangedane baby’s correct in meer dan 96% van de gevallen, met een vrijwel perfecte maat voor de algehele discriminerende kracht. Visuele kaarten van welke regio’s het netwerk gebruikte lieten zien dat het zich concentreerde op dezelfde diepe hersengebieden — globus pallidus, nucleus subthalamicus en hippocampus — die menselijke experts als het meest kwetsbaar voor bilirubineschade beschouwen, wat suggereert dat de computer klinisch betekenisvolle patronen leerde in plaats van willekeurige eigenaardigheden.
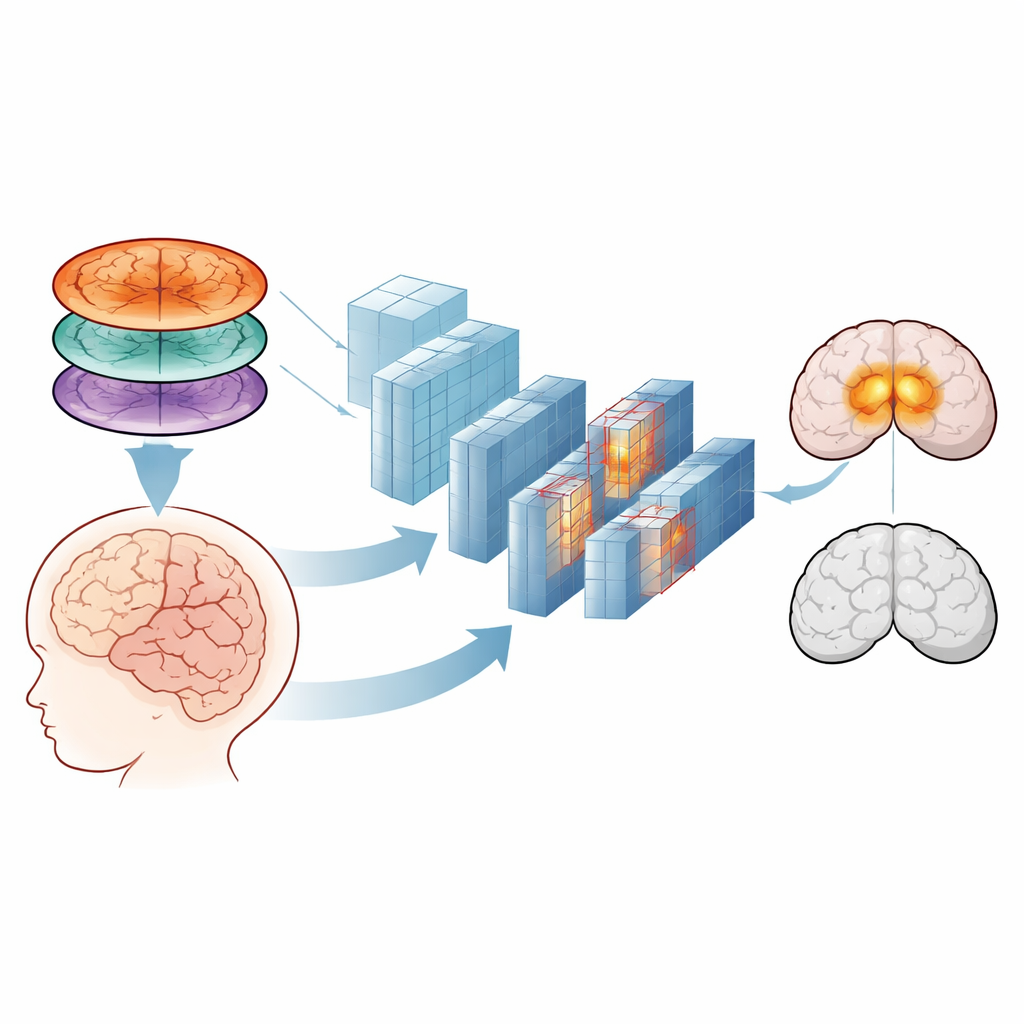
Van onderzoeksgereedschap naar hulp aan het bed
De studie concludeert dat een zorgvuldig getraind computerondersteund diagnosesysteem, gevoed met meerdere complementaire typen MRI in plaats van één scan, vroege bilirubine-gerelateerde hersenschade bij pasgeborenen met indrukwekkende nauwkeurigheid kan signaleren. Hoewel het werk in één ziekenhuis is uitgevoerd en nog hindernissen kent zoals overfitting en de noodzaak om te testen op grotere, meer diverse groepen baby’s, wijst het op een toekomst waarin geavanceerde beeldleesalgoritmen fungeren als een tweede paar ogen voor kinderartsen en radiologen. Op verstandige wijze gebruikt, kunnen dergelijke hulpmiddelen helpen bepalen welke geelzuchtige zuigelingen het meest dringend behandeling nodig hebben — en minstens zo belangrijk, geruststelling bieden aan gezinnen wanneer de hersenen van een baby waarschijnlijk veilig zijn.
Bronvermelding: Wu, M., Liu, Q. Computer-aided diagnosis of neonatal acute bilirubin encephalopathy with multi-modal MRI images and convolutional neural networks. Sci Rep 16, 9611 (2026). https://doi.org/10.1038/s41598-025-33337-4
Trefwoorden: neonatale geelzucht, bilirubine-encefalopathie, hersenen MRI, diep leren, computerondersteunde diagnose