Clear Sky Science · nl
CMAF-Net: cross-modale aandachtfusie met informatie-theoretische regularisatie voor ongebalanceerde histopathologie van borstkanker
Waarom dit onderzoek van belang is voor borstkankerzorg
Pathologen stellen de diagnose borstkanker door dunne weefsellagen onder een microscoop te bestuderen, maar het scheiden van zeldzame kwaadaardige plekjes uit een zee van gezonde cellen is veeleisend en onvolmaakt werk. Deze studie introduceert CMAF-Net, een nieuw type computersysteem dat is ontworpen om meer kankergevallen in deze beelden te detecteren terwijl valse alarmsignalen laag blijven, zelfs wanneer maligne voorbeelden sterk in de minderheid zijn. De vooruitgang kan automatische screening betrouwbaarder maken, overbelaste clinici ondersteunen en een blauwdruk bieden voor het opsporen van veel andere zeldzame aandoeningen.
Een naald vinden in een hooiberg van weefselbeelden
In echte ziekenhuisgegevens zijn de meeste borstweefselmonsters onschadelijk en bevat slechts een minderheid invasieve ductale carcinomen, de meest voorkomende vorm van borstkanker. Deze ongelijkheid zorgt ervoor dat veel AI-systemen stilletjes "leren" dat het voorspellen van gezond weefsel bijna altijd veilig is, waardoor gevaarlijke tumoren gemist worden. Tegelijkertijd doen aanwijzingen voor maligniteit zich voor op zeer verschillende zoomniveaus, van vervormde kernen in enkele cellen tot verstoorde structuren over een groter weefselgebied. Traditionele beeldanalyzenetwerken zijn goed in óf kleine details óf grote patronen, maar ze combineren zelden beide op een manier die de zeldzame, levensbedreigende gevallen naar voren brengt.
Details van dichtbij mengen met het grotere geheel
Om deze dubbele problemen aan te pakken, ontwierpen de auteurs CMAF-Net met twee complementaire "ogen" op elk beeld. De ene tak werkt als een klassiek patroonherkenningssysteem dat gespecialiseerd is in fijne texturen, zoals de vormen en ordening van cellen. De tweede tak gedraagt zich meer als een globale kaartlezer en legt bredere weefselorganisatie vast met een modern transformer-ontwerp. In plaats van deze twee weergaven simpelweg op elkaar te stapelen, laat het systeem ze passeren door een speciale fusieblok dat de takken toestaat informatie uit te wisselen via meerdere aandachtkanalen. Dit blok behoudt selectief kenmerken die nieuwe inzichten toevoegen en onderdrukt gedupliceerde of afleidende signalen, zodat de uiteindelijke gecombineerde representatie zowel rijk als compact blijft. 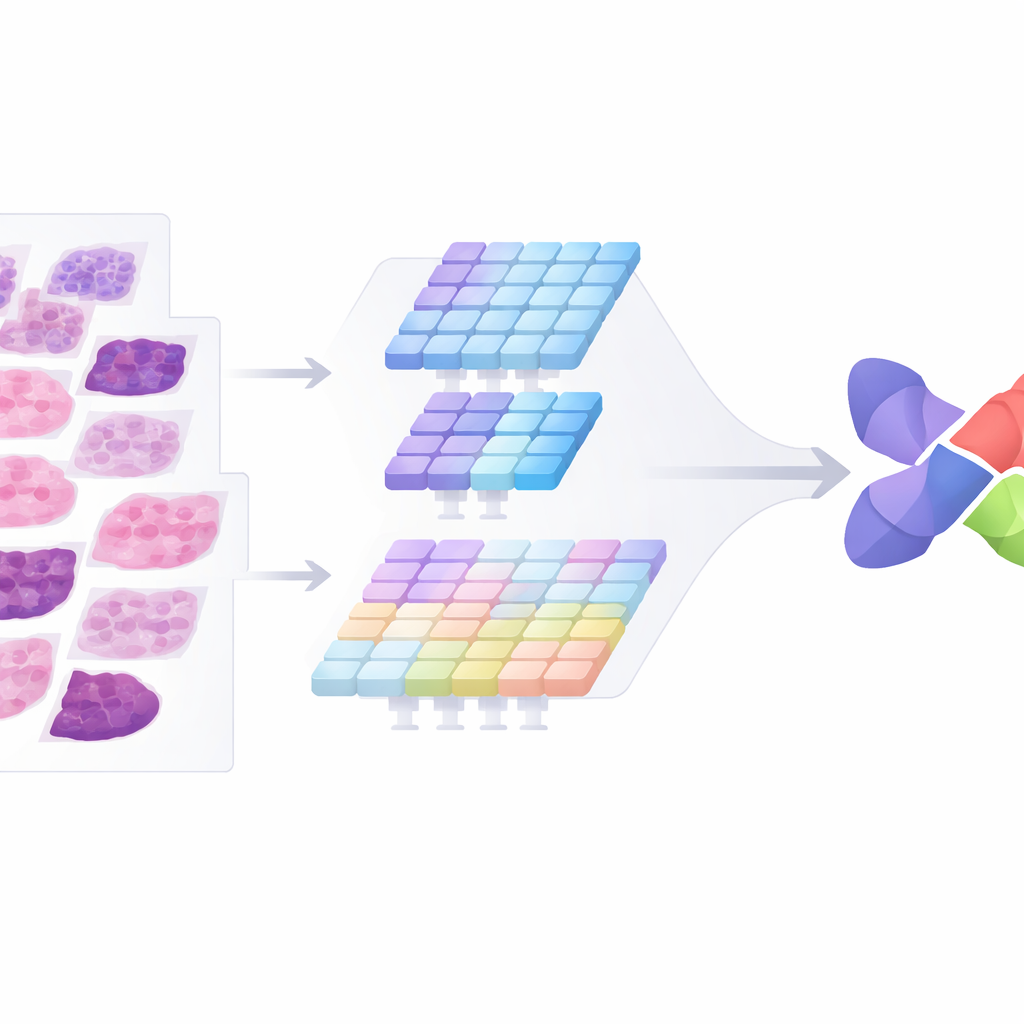
Het systeem leren om zeldzame kankers belangrijk te vinden
Zelfs een slimme architectuur kan nog steeds de voorkeur geven aan de meerderheidsklasse, dus herontwierpen de onderzoekers de manier waarop het systeem leert van zijn fouten. Gebaseerd op ideeën uit de informatietheorie en margin-based learning, ontwikkelden ze een trainingsregel die het model er expliciet toe aanzet bredere "veiligheidsmarges" rond de minderheidskankergevallen uit te kerven. Praktisch gezien wordt CMAF-Net zwaarder gestraft voor het missen van een maligne patch dan voor het verkeerd classificeren van een goedaardige, en deze straf wordt na verloop van tijd aangepast naarmate de features-ruimte zich ontwikkelt. Het aandachtmechanisme zelf wordt ook afgestemd via een soort "temperatuur"-regeling: scherpere aandacht behoudt meer informatie wanneer dat nodig is, terwijl zachtere aandacht ruis wegfiltert, waardoor het model een principiële manier krijgt om data te comprimeren zonder de signalen te verliezen die kanker van niet-kanker scheiden. 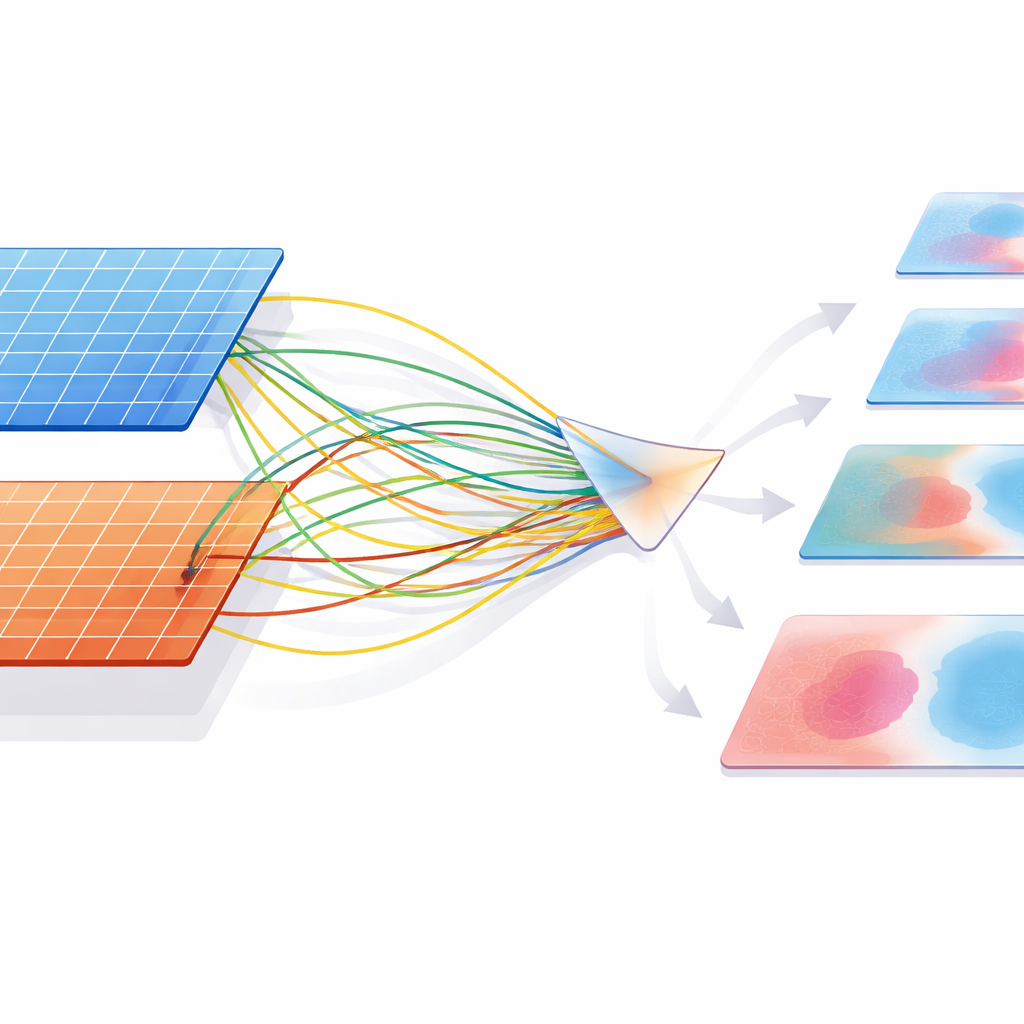
De methode op de proef stellen
Het team evalueerde CMAF-Net op een grote, natuurlijk ongebalanceerde dataset van borstweefselpatches, waarbij ongeveer driekwart goedaardig was en de rest kwaadaardig. Vergeleken met een reeks sterke baseline-systemen — waaronder diepe convolutionele netwerken, vision transformers en eerdere fusie-modellen afgestemd op ongelijkheid — stak de nieuwe methode eruit. Het identificeerde correct ruwweg 95% van de maligne voorbeelden terwijl de specificiteit vergelijkbaar hoog bleef, en deed dit met minder parameters dan veel concurrerende fusienetwerken. Toen de auteurs de data nog schever maakten, tot slechts één kankerpakket per negenennegentig goedaardige, daalde de prestatie van CMAF-Net geleidelijk maar bleef klinisch bruikbaar. Andere methoden daarentegen verloren het grootste deel van hun vermogen om kanker te herkennen onder deze extreme condities.
Generaliseren over microscopen en tumortypes
Om te onderzoeken of CMAF-Net slechts één dataset uit het hoofd leerde of meer universele ziektepatronen oppikte, testten de auteurs het op een aparte verzameling borsttumorafbeeldingen gemaakt van verschillende patiënten en op vier verschillende vergrotingsniveaus. Zonder enige hertraining behield het model een hoge sensitiviteit over alle zoomniveaus en overtrof het eerdere benaderingen zowel op eenvoudige goedaardig-tegen-malignant taken als op een zwaardere acht-klassenprobleem dat meerdere tumorsubtypes beslaat. Opmerkelijk is dat CMAF-Net de grootste winst liet zien bij zeldzame tumorcategorieën, wat suggereert dat de focus op informatie-efficiënte fusie en klasse-bewust leren helpt subtiele, ongewone patronen te onderscheiden in plaats van alleen de meest typische gevallen.
Wat dit betekent voor de toekomst
Voor niet-specialisten is de belangrijkste boodschap dat CMAF-Net een slimmere manier biedt voor computers om pathologiedia's te lezen: het kijkt nauwkeurig en globaal tegelijk, leert extra aandacht te geven aan zeldzame maar gevaarlijke tekenen van kanker, en blijft werken zelfs wanneer maligne voorbeelden schaars zijn. Buiten borstkanker kunnen dezelfde ontwerpprincipes hulpmiddelen leiden voor het opsporen van zeldzame aandoeningen in vele soorten medische beelden, waardoor artsen een betrouwbaardere second opinion krijgen en mogelijk eerdere, nauwkeurigere diagnoses mogelijk worden voor patiënten die ze het meest nodig hebben.
Bronvermelding: Ativi, W.X., Chen, W., Kwao, L. et al. CMAF-Net: cross-modal attention fusion with information-theoretic regularization for imbalanced breast cancer histopathology. Sci Rep 16, 9607 (2026). https://doi.org/10.1038/s41598-025-32794-1
Trefwoorden: borstkanker, histopathologie AI, klasse-ongelijkheid, deep learning, medische beeldanalyse