Clear Sky Science · nl
Incrementele leeraanpak voor semantische segmentatie van huidhistologiebeelden
Waarom het belangrijk is computers huidmonsters te leren lezen
Huidkanker is een van de meest voorkomende vormen van kanker wereldwijd, en artsen baseren hun beslissingen vaak op dunne weefselplakjes die onder een microscoop worden bekeken om te bepalen hoe ernstig een tumor is en hoe die behandeld moet worden. Het lezen van deze preparaten is een langzaam, veeleisend werk dat per expert kan verschillen. Deze studie onderzoekt hoe computersystemen kunnen worden gebouwd die leren verschillende huidweefsels en kankers in deze microscoopbeelden te herkennen en — belangrijk — hoe ze na verloop van tijd kunnen blijven verbeteren als nieuwe typen beelden worden toegevoegd, vergelijkbaar met een menselijke leerling die gedurende zijn carrière blijft bijleren.
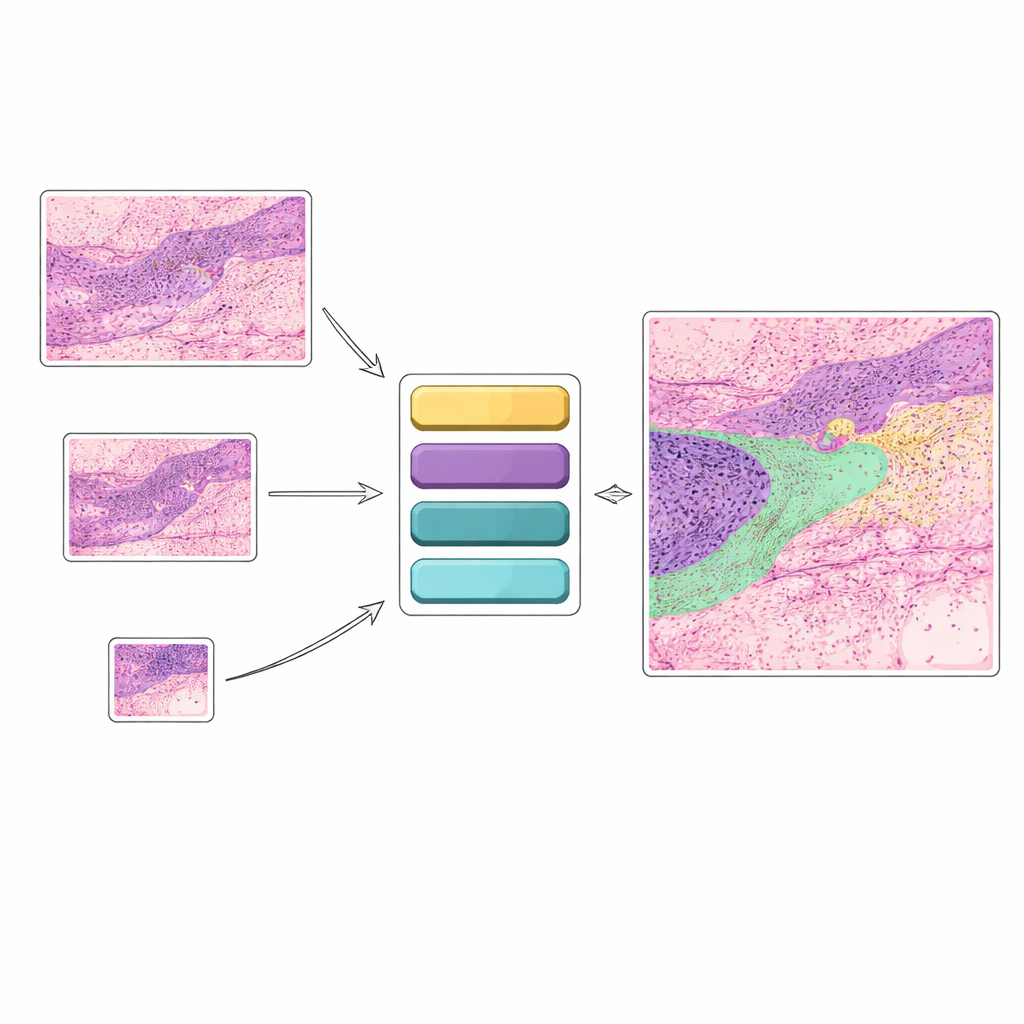
Van eenvoudige ja/nee-antwoorden naar gedetailleerde weefselkaarten
Veel bestaande kunstmatige-intelligentietools voor huidkanker bekijken een beeld en geven een beperkte ja/nee-uitkomst zoals “kanker” of “geen kanker.” Hoewel nuttig, vangt dit soort beslissing niet de rijke details die pathologen zien. In de praktijk kijken artsen tegelijk naar vele structuren: verschillende kankertypen, gezonde huidlagen, haarzakjes, klieren, ontstoken gebieden en meer. Deze studie richt zich op “semantische segmentatie”, waarbij elke pixel in een histologiebeeld wordt toegewezen aan een van de twaalf weefselcategorieën. Dat levert een kleurgecodeerde kaart op die precies laat zien waar verschillende kankers en normale weefsels liggen, en biedt duidelijkere aanwijzingen voor diagnose en behandelplanning.
Waarom huidige slimme systemen moeite hebben zich aan te passen
De krachtige deep-learningmodellen van vandaag veronderstellen meestal dat alle trainingsdata in één keer beschikbaar zijn. Eenmaal getraind neigen ze ertoe hun kennis te "vergrendelen". Als later nieuwe data met andere eigenschappen worden toegevoegd — bijvoorbeeld beelden met een andere vergroting — is de veiligste optie vaak het hele model opnieuw vanaf nul te trainen. Dat is kostbaar en traag, en erger nog, het toevoegen van nieuwe informatie kan "catastrofaal vergeten" veroorzaken, waarbij de prestaties op eerdere taken geleidelijk verslechteren. In de klinische praktijk veranderen gegevens echter continu wanneer scanners worden geüpdatet, beeldinstellingen variëren en ziekenhuizen nieuwe typen monsters verzamelen. Een AI-hulpmiddel dat zulke veranderingen niet soepel kan opnemen, is moeilijk betrouwbaar in het dagelijks gebruik.
Een stapsgewijze leerstrategie geïnspireerd op hoe mensen leren
De auteurs bouwen voort op een moderne vision-transformerarchitectuur genaamd SegFormer en zetten die om in een "incrementeel leer"-systeem voor niet-melanoom huidkanker. In plaats van alle data in één keer te zien, wordt het model in fasen getraind met histologiedia’s uit een openbare dataset van de Queensland University. Eerst leert het van hoge vergroting (10×) beelden, waarin fijne details duidelijk zijn. Later worden beelden op 5× en vervolgens 2× vergroting toegevoegd, terwijl een deel van de eerdere gegevens met hoge detailgraad in de mix blijft. Speciale verliesfuncties helpen de nieuwe versie van het model te behouden wat het eerder wist over weefselpatronen, zelfs terwijl het zich aanpast aan grovere, meer uitgezoomde beelden. Dit "leren zonder te vergeten" wordt gestuurd door een techniek genaamd knowledge distillation, waarbij een eerder model als leraar fungeert voor de nieuwere, en door een wederzijdse distillatie-term die zowel oude als nieuwe representaties aanmoedigt in harmonie te blijven.
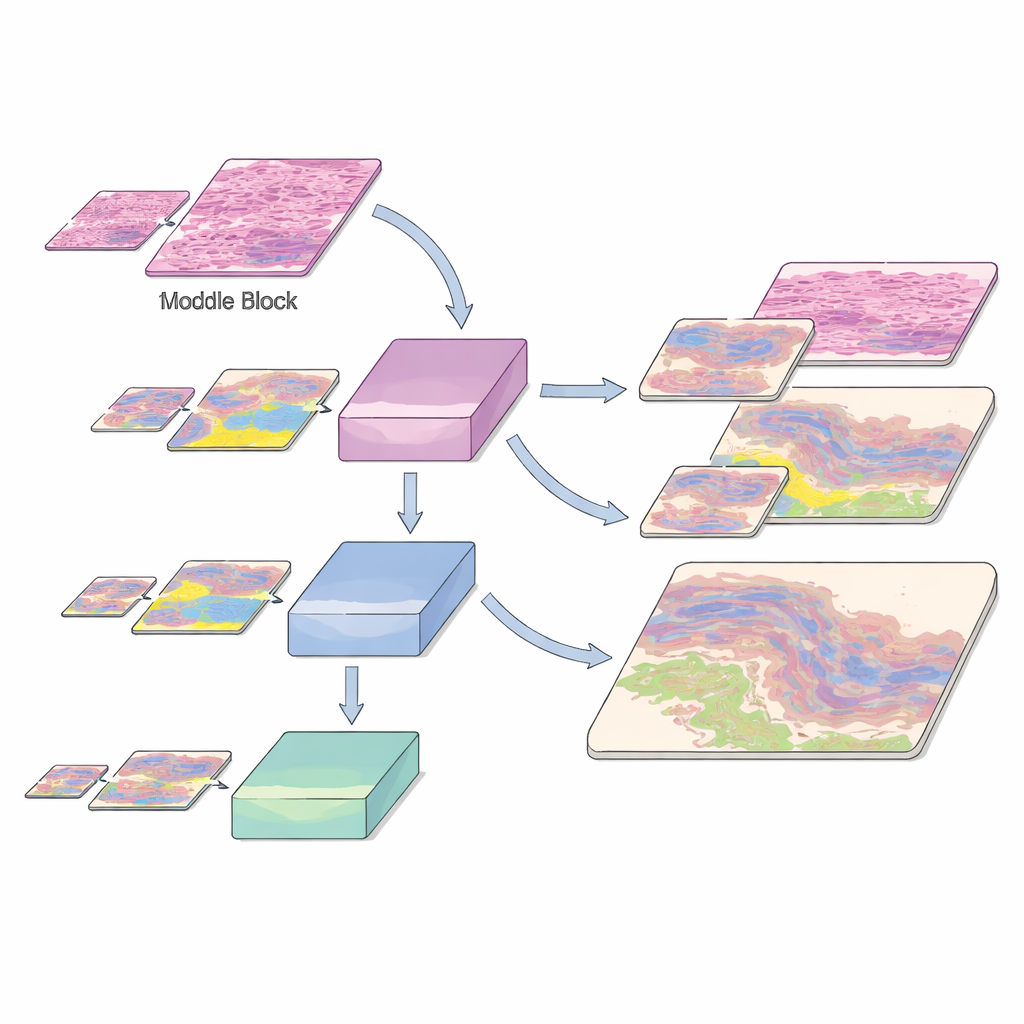
Leren over zoomniveaus en zeldzame weefseltypen
Histologiebeelden zijn uitdagend, niet alleen omdat er veel weefseltypen zijn, maar ook omdat sommige belangrijke structuren zeldzaam zijn. De dataset bevat veelvoorkomende kankers zoals basaalcelcarcinoom en plaveiselcelcarcinoom, evenals normale en ontstoken huidlagen, elk op pixelniveau geannoteerd door experts — een arbeidsintensief proces van vele honderden uren. De auteurs snijden deze grote dia’s in kleine patches en trainen hun model met een zorgvuldig verdeelde set voor training, validatie en test, waarbij de samenstelling van weefselklassen bij elke vergroting behouden blijft. Om het systeem te helpen schaarse maar klinisch cruciale regio’s te herkennen, vergroten ze ondervertegenwoordigde klassen door patches te roteren en door het model deze weefsels op meerdere zoomniveaus te laten zien. Deze blootstelling aan meerdere resoluties helpt de AI dezelfde biologische structuur te herkennen, of deze nu als een scherpe close-up of als een zachtere, uitgezoomde vorm verschijnt.
Wat het model bereikt vergeleken met eerdere tools
Op zichzelf presteren SegFormer-modellen die afzonderlijk op elke vergroting zijn getraind al beter dan eerdere convolutionele ontwerpen zoals U-Net voor veel weefselcategorieën. Maar wanneer de incrementele leermethode wordt toegepast — eerst trainen op 10×, vervolgens op 10× plus 5× en ten slotte op 10×, 5× en 2× samen — worden de verbeteringen opvallend. De algehele nauwkeurigheid stijgt van ongeveer 89% met alleen 10× beelden naar meer dan 95% nadat alle drie de vergrotingen zijn opgenomen. Maatstaven van overlap tussen voorspelde en werkelijke regio’s verbeteren ook gestaag, en de prestaties op kankers zoals basaalcel- en plaveiselcelcarcinoom, evenals op belangrijke normale lagen zoals de epidermis en papillaire dermis, overtreffen die van concurrerende methoden. Belangrijk is dat het model, naarmate elk nieuw zoomniveau wordt toegevoegd, niet vergeet wat het eerder heeft geleerd; in plaats daarvan wordt zijn begrip van weefselstructuur robuuster en algemener.
Hoe dit werk AI-ondersteunde diagnose dichter bij de kliniek brengt
Voor niet-specialisten is de kernboodschap dat de auteurs een huidweefsel-"kaartmaker" hebben ontwikkeld die nieuwe soorten beelden kan blijven bestuderen zonder zijn eerdere vaardigheden te verliezen. Door zorgvuldig vorm te geven hoe het model in fasen leert en hoe het zijn eigen verleden hergebruikt, laten ze zien dat het mogelijk is AI-hulpmiddelen te bouwen die zich aanpassen naarmate medische beeldvorming evolueert. Hoewel meer validatie over ziekenhuizen en ziektetypen nodig is, wijst deze incrementele, transformer-gebaseerde aanpak in de richting van AI-systemen die up-to-date kunnen blijven met veranderende data, gedetailleerde visuele verklaringen geven waar kankers zich bevinden, en uiteindelijk pathologen ondersteunen bij het nemen van zekerder en consistenter behandelbeslissingen.
Bronvermelding: Fatima, S., Salam, A.A., Akram, M.U. et al. Incremental learning approach for semantic segmentation of skin histology images. Sci Rep 16, 9593 (2026). https://doi.org/10.1038/s41598-025-31553-6
Trefwoorden: huidkanker, histologiebeelden, semantische segmentatie, incrementeel leren, deep learning-transformers