Clear Sky Science · nl
In vivo visualisatie van extracellulaire adenosinedynamiek in het hart en de farmacologische modulatie ervan in zebravis-hartfalenmodellen
Waarom dit verhaal over het vishart telt
Hartfalen blijft een van de belangrijkste doodsoorzaken wereldwijd, en veel patiënten verslechteren nog steeds ondanks de beste beschikbare medicijnen. Wetenschappers weten dat gestreste hartcellen chemische "noodsignalen" in hun omgeving vrijgeven, maar het is moeilijk geweest om deze signalen in actie te bekijken in een kloppend hart. Deze studie gebruikt transparante zebravissen, waarvan de kleine harten belangrijke kenmerken van menselijke harten nabootsen, om die gevaarsignalen in realtime te volgen en een nieuwe manier te testen om ze te dempen.
Signalen van een worstelend hart
Wanneer hartcellen beschadigd raken, geven ze energierijke moleculen zoals ATP en het afbraakproduct adenosine vrij in de extracellulaire ruimte. Buiten de cel fungeren deze moleculen niet meer als brandstof maar als dringende boodschappen die ontsteking kunnen aanwakkeren. Bij chronisch hartfalen kan die ontstekingsreactie overactief worden en het hart verder beschadigen. Tot nu toe hadden onderzoekers echter geen directe, in vivo bewijsvoering van hoe deze moleculen zich in de tijd gedragen in een falend hart.
Zebravissen ombouwen tot levende chemische camera's
Het team bouwde zebravissen die op het oppervlak van hun hartcellen een speciaal fluorescerend sensors-eiwit genaamd GRABAdo produceren. Wanneer adenosine buiten de cellen ophoopt, gaat deze sensor helderder groen oplichten, waardoor elk klein hartje als het ware een eigen levende chemische camera wordt. De onderzoekers veroorzaakten vervolgens hartfalen in zebravissen met terfenadine, een geneesmiddel dat bekendstaat om hartritmestoornissen te veroorzaken en de pompfunctie te verzwakken. Naarmate de vissen duidelijke tekenen van hartfalen ontwikkelden — langzamere hartslagen, vergrote en zwakkere ventrikels, vochtophoping rond het hart en slechtere zwemprestaties — lichtten hun hartsensoren op en toonden een duidelijke stijging van extracellulair adenosine. Chemische metingen van hele larven bevestigden dat de totale adenosinespiegels hoger waren in de falende harten.
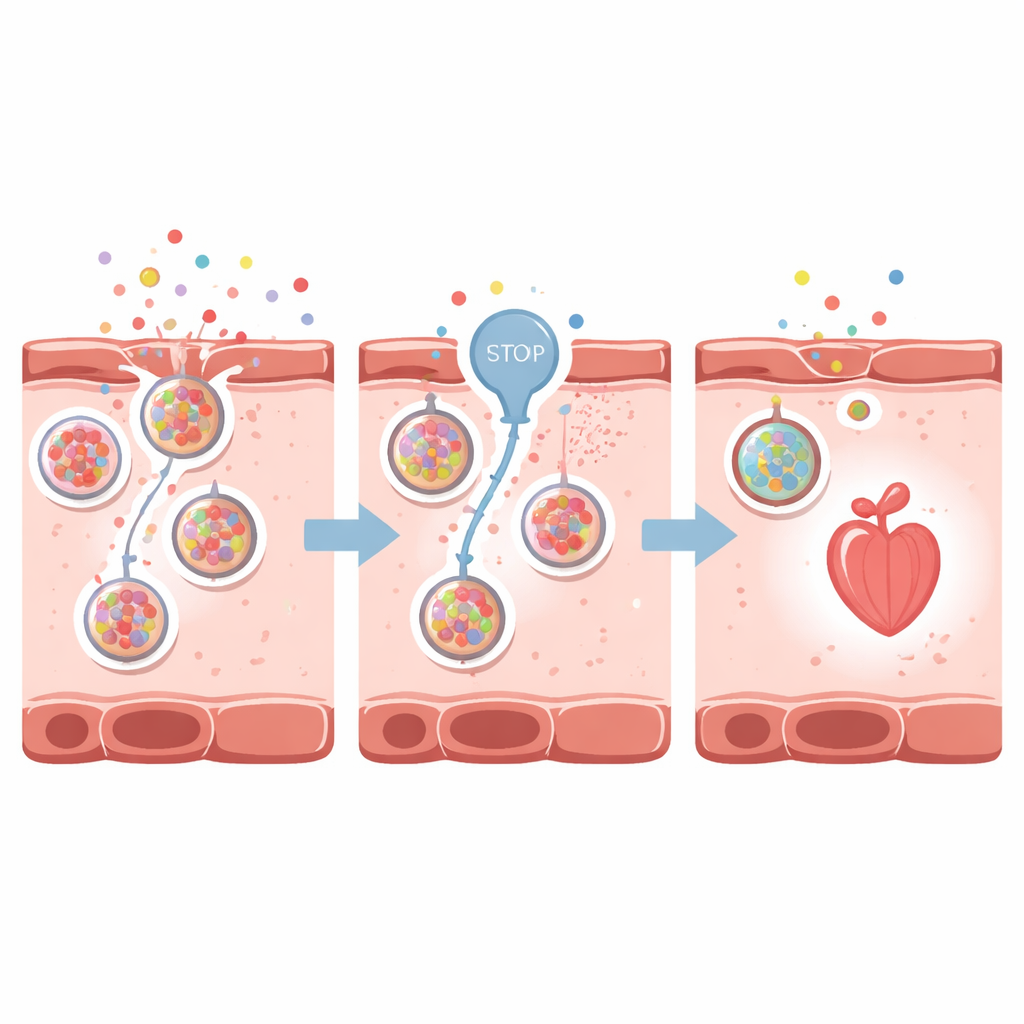
De uitlaatklep afsluiten
De wetenschappers vroegen zich vervolgens af of het dempen van deze noodsignalen het hart kon beschermen. Ze richtten zich op VNUT, een transporter die ATP laadt in kleine cellulaire blaasjes (vesikels) voor afgifte buiten de cel. Met clodronaat, een middel dat VNUT blokkeert, verminderden ze de ATP-afgifte en indirect de ophoping van adenosine rond hartcellen. Bij zebravissen met geneesmiddel-geïnduceerd hartfalen hield VNUT-remming de hartvorm beter in stand, verminderde kameruitzetting, verbeterde de hartslag en pompkracht en handhaafde een betere bloedstroom. De oplichtende adenosinesensor dimde, wat aangaf dat er minder van het noodsignaal buiten de cellen aanwezig was. Vergelijkbare beschermende effecten werden gezien bij volwassen zebravissen met een acute, snel optredende vorm van hartfalen.
Meerdere beschermende hendels die samenwerken
Hartfalen omvat meer dan één pad, dus testten de onderzoekers hoe VNUT-blokkade samenwerkt met andere bekende spelers. Middelen die bepaalde adenosinereceptoren en ATP-receptoren blokkeren, evenals een verbinding die passief ATP-lek door membraankanalen beperkt, hielpen elk op zichzelf de zebravissenharten. In combinatie met VNUT-remming leverden veel van deze behandelingen additieve voordelen op, wat suggereert dat het terugschakelen van purinesignalering op meerdere niveaus bijzonder krachtig kan zijn. VNUT-remming hielp ook het calciumbalans in hartcellen te herstellen, essentieel voor normaal kloppen, en verminderde zowel celdood als de activiteit van genen die met ontsteking samenhangen. Gezamenlijk schetsen deze resultaten VNUT als een centraal schakelpunt dat ATP-afgifte, ontsteking, verstoorde calciumhuishouding en progressieve hartschade verbindt.
Van vissenbakken naar toekomstige therapieën
Voor niet-specialisten is de kernboodschap dat de studie direct een chemisch stresssignaal laat zien dat toeneemt in falende harten en aantoont dat het blokkeren van de afgifte daarvan de hartfunctie in een levend dier kan beschermen. Hoewel zebravissenharten eenvoudiger zijn dan menselijke harten, delen ze genoeg biologie om een krachtig testplatform voor nieuwe ideeën te bieden. Door VNUT bloot te leggen als een veelbelovend target op het snijvlak van ontsteking en elektrische instabiliteit, suggereert dit werk dat toekomstige hartfalentherapieën meer kunnen doen dan alleen de bloedstroom ondersteunen — ze kunnen ook actief schadelijke cellulaire communicatie kalmeren die het hart richting falen duwt.
Bronvermelding: Phurpa, P., Apolinario, M.E.C., Umeda, R. et al. In vivo visualization of cardiac extracellular adenosine dynamics and its pharmacological modulation in zebrafish heart failure models. Sci Rep 16, 8220 (2026). https://doi.org/10.1038/s41598-025-30303-y
Trefwoorden: hartfalen, adenosinesignalering, zebravissenmodel, ontsteking, cardiale bescherming