Clear Sky Science · nl
Telomerische G-quadruplex‑intermediairen onthuld door complexe Markov-netwerkanalyse
Verborgen knopen aan de uiteinden van ons DNA
Aan de uiteinden van onze chromosomen bevinden zich beschermende doppen die telomeren worden genoemd, vaak vergeleken met de plastic uiteinden van veters. In deze regio’s kan het DNA zichzelf in ongewone vierstrengige knopen vouwen, bekend als G-quadruplexen. Deze kleine structuren kunnen beïnvloeden hoe onze genen werken en hoe cellen verouderen of kwaadaardig worden. Deze studie werpt een blik achter de schermen van hoe één zo’n knoop geleidelijk losraakt, waarbij gedetailleerde computersimulaties en geavanceerde data-analyse vluchtige vormen blootleggen die in experimenten bijna niet te vangen zijn.
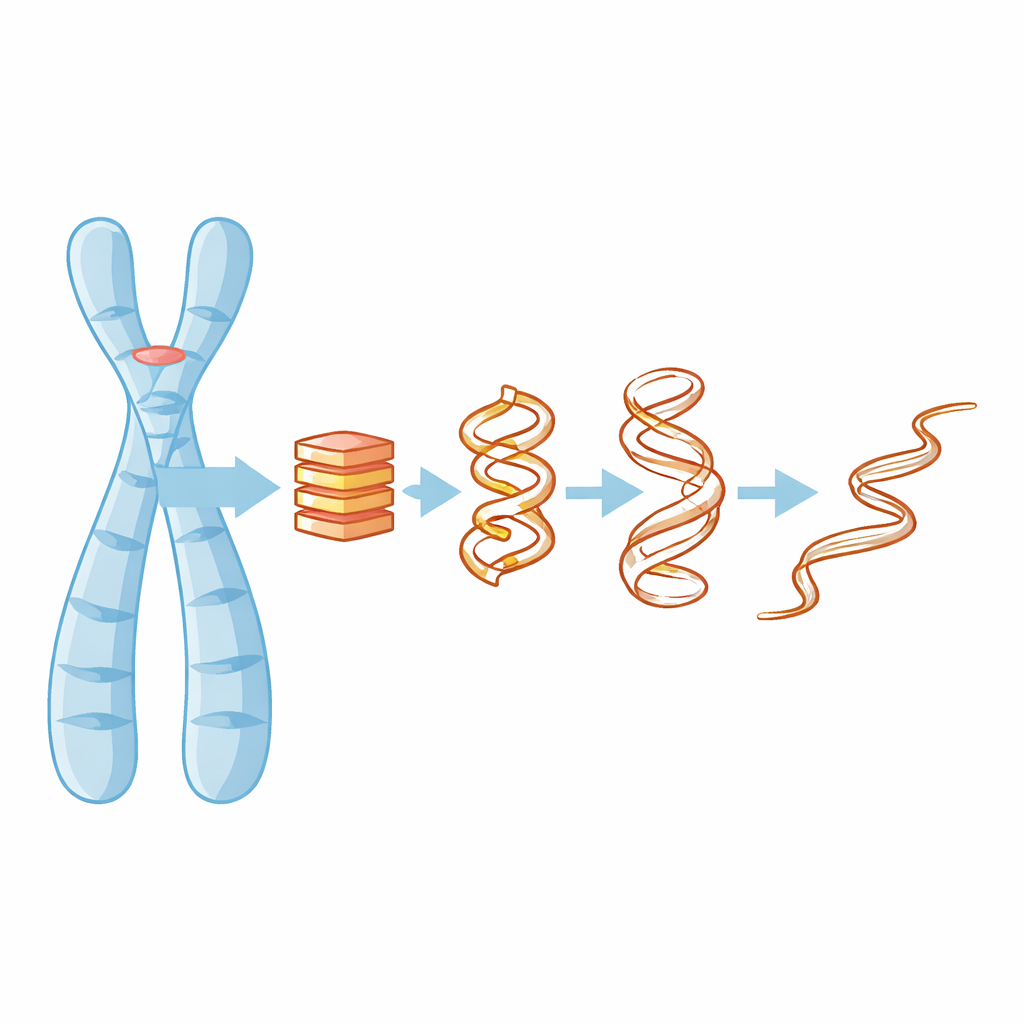
Waarom vierstrengige DNA‑knopen ertoe doen
De meesten van ons leren dat DNA een dubbele helix is, maar in guanine‑rijke stukken—zoals die in telomeren—kan het molecuul vouwen tot compacte vierstrengige stapels die G-quadruplexen worden genoemd. Deze stapels worden bijeengehouden door platte lagen guaninebasen en kleine positief geladen ionen, zoals kalium, die in het midden zitten en alles samenlijmen. Wanneer een G-quadruplex zich vormt of uit elkaar valt, kan dat delen van het genoom blokkeren of blootleggen, wat invloed heeft op genexpressie, DNA‑replicatie en zelfs hoe kankercellen hun telomeren onderhouden. Begrijpen hoe deze structuren hun vorm verliezen is daarom cruciaal om ze met medicijnen te kunnen richten of te voorspellen wanneer ze hun functie verliezen.
Een moleculaire knoop zien loskomen
De onderzoekers richtten zich op een menselijke telomerische G-quadruplex waarin vier segmenten van één DNA‑streng parallel naast elkaar liggen en stapelen tot een compacte kolom. Ze gebruikten all‑atom moleculaire dynamicasimulaties—virtuele experimenten die de beweging van elk atoom volgen—om acht kopieën van deze structuur op te warmen tot temperaturen dicht bij het smeltpunt. Om het systeem verschillende vormen te laten verkennen, pasten ze replica‑exchange toe, waarbij simulaties bij verschillende temperaturen af en toe configuraties uitwisselen. In zeven van de acht gevallen bleef de G-quadruplex intact; in één geval vouwde hij volledig uit. Die zeldzame uitvouwing werd een gedetailleerde casestudy, die niet alleen het voor en na liet zien, maar een hele reeks tussenliggende vormen onderweg.
De cruciale rol van kleine ionen
Een centrale bevinding is dat de kleine ionen binnenin de G-quadruplex als spilpunten fungeren. Zolang ten minste één ion genesteld blijft tussen de guaninelagen, blijft de structuur grotendeels intact—misschien iets losser maar nog herkenbaar. Wanneer beide ionen uiteindelijk het centrale kanaal verlaten, destabiliseert de stapel echter snel. De guaninelagen vervormen en afzonderlijke strengen pellen weg, en het totale DNA wordt meer uitgerekt en flexibel. Andere gesimuleerde moleculen die slechts één ion verloren, kwamen in wiebelige maar nog deels geordende toestanden terecht, wat suggereert dat volledige uitvouwing het verlies van beide stabiliserende ionen vereist—een aanwijzing waarom sommige G-quadruplexen in de cel zo hardnekkig stabiel zijn.
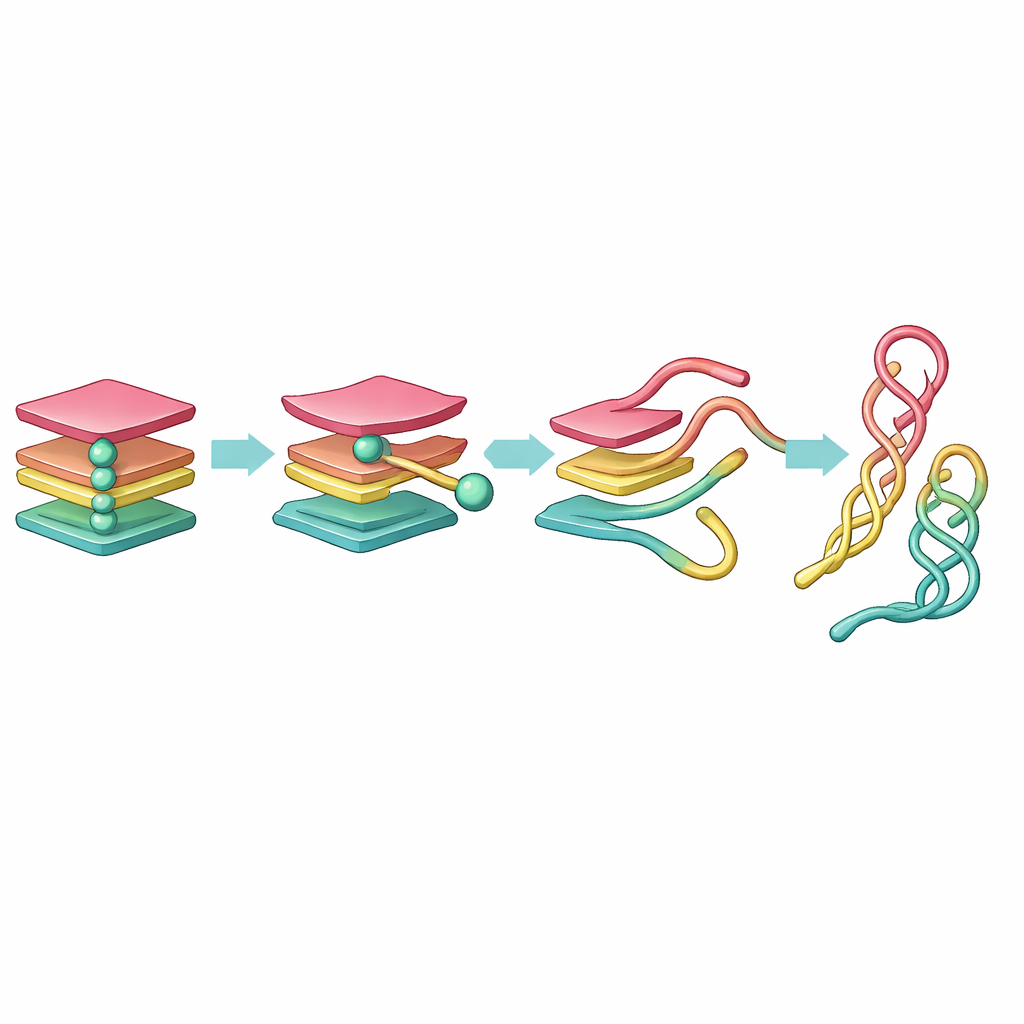
Verborgen tussenstops in de route ontdekken
De ruwe simulatie leverde een enorme hoeveelheid data op, veel te complex om met het blote oog te interpreteren. Om dit te beteugelen vereenvoudigde het team eerst het DNA door elke base te representeren als één bolletje, en gebruikte vervolgens wiskundige hulpmiddelen om de beweging terug te brengen tot slechts een paar sleutelcoördinaten. Ze pasten twee methoden toe: Principal Component Analysis (PCA), die de richtingen van grootste beweging benadrukt, en time‑independent Component Analysis (tICA), die de langzame, duurzaam blijvende veranderingen filtert die echte structurele verschuivingen markeren. Vanuit deze gereduceerde coördinaten bouwden ze zogenaamde conformationele Markov‑netwerken, waarin elke knoop een typisch DNA‑vorm is en verbindingen tonen hoe het molecuul van de ene vorm naar de andere springt.
Een geprefereerde route van knoop naar losse streng
Deze netwerkvisie onthulde een duidelijke uitvouwingsroute. Beginnend bij een volledig gevouwen G-quadruplex raakt eerst één streng los en vormt een driestrengige "triplex"‑toestand. Die triplex reorganiseert vervolgens in een tweestrengige "hairpin" en een reeks daaraan verwante losse strengen. De hairpin en een verwante "cross‑hairpin"‑configuratie blijken verrassend langlevend en fungeren als stabiele tussenstops op de weg van een strakke knoop naar een meer ontspannen DNA‑configuratie. Terwijl PCA deze progressie splitste in vele vergelijkbaar uitziende toestanden, destilleerde tICA het tot een klein aantal onderscheiden, kinetisch betekenisvolle stappen, en toonde dat triplex‑achtige vormen kortstondig zijn, terwijl hairpin‑achtige vormen veel langer aanhouden.
Wat dit betekent voor biologie en geneeskunde
Voor niet‑specialisten is de hoofdboodschap dat telomerische G-quadruplexen niet eenvoudigweg knappen van gevouwen naar uitgevouwen. In plaats daarvan smelten ze door een reeks kortstondige en langer durende vormen, waarbij kleine ionen als poortwachters van stabiliteit optreden. De simulaties suggereren dat driestrengige intermediairen vluchtig zijn, terwijl tweestrengige hairpins en kruisvormige vormen stabielere rustpunten vormen. Omdat deze tussenstaten mogelijk ook in de omgekeerde vouwrichting voorkomen, zijn ze waarschijnlijk cruciaal voor hoe G‑quadruplexen zich vormen, veranderen en omgaan met potentiële geneesmiddelen. Het in kaart brengen van dit verborgen landschap van vormen brengt wetenschappers een stap dichter bij het ontwerpen van moleculen die selectief deze DNA‑knopen kunnen stabiliseren of destabiliseren in de strijd tegen kanker en andere ziekten.
Bronvermelding: Sáinz-Agost, A., Falo, F. & Fiasconaro, A. Telomeric G-quadruplex intermediates unveiled by complex Markov network analysis. Sci Rep 16, 8308 (2026). https://doi.org/10.1038/s41598-025-29993-1
Trefwoorden: G-quadruplex, telomeer-DNA, moleculaire dynamica, eiwitvrije DNA‑vouwing, kankergeneesmiddelen