Clear Sky Science · nl
Identificatie en evaluatie van tumorpyroptose-geassocieerde antigenen voor het ontwerpen van een vaccinkandidaat tegen longkanker
Waarom dit onderzoek belangrijk is voor mensen met longkanker
Longkanker blijft de dodelijkste kanker wereldwijd, en de huidige behandelingen — chirurgie, chemotherapie, bestraling en immunotherapie — laten nog veel patiënten zonder langetermijnopties. Deze studie onderzoekt een heel ander idee: een therapeutisch vaccin dat niet bedoeld is om infecties te voorkomen, maar om het immuunsysteem beter te trainen longtumoren te herkennen en aan te vallen. Met geavanceerde computer‑modellering bouwen en testen de auteurs geheel in silico een eiwitgebaseerd vaccin dat zich richt op moleculen die betrokken zijn bij een vuurkrachtige vorm van celdood, pyroptose, en opent daarmee een nieuwe weg naar meer precieze en duurzame behandeling van longkanker.
Een celdoodschakelaar veranderen in een kankerdoelwit
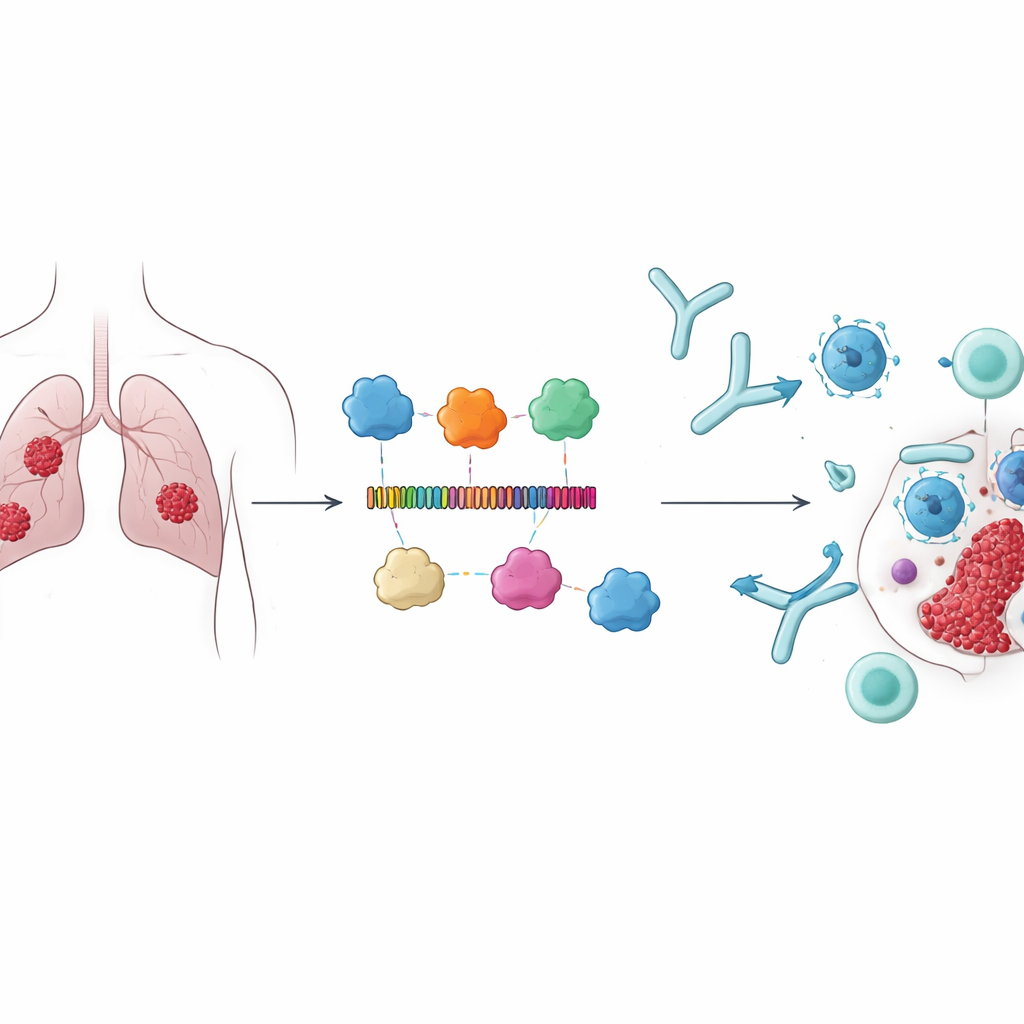
In plaats van zich te concentreren op klassieke kankermarkers kozen de onderzoekers vier eiwitten — CARD8, NAIP, NLRP1 en NLRP3 — die betrokken zijn bij pyroptose, een explosieve vorm van geprogrammeerde celdood die het immuunsysteem kan alarmeren. Deze eiwitten spelen een rol in immuunregulatie en zijn geassocieerd met betere overleving bij longadenocarcinoom, wat ze aantrekkelijke doelwitten maakt. Het team redeneerde dat als het immuunsysteem nauwkeurig getraind kan worden om kleine segmenten van deze eiwitten op tumorcellen te herkennen, dat niet alleen kankercellen direct kan helpen vernietigen, maar ook bredere immuunreacties tegen de tumor kan versterken.
Een op maat gemaakt vaccin stukje bij beetje opbouwen
Met behulp van immunoinformatica-tools doorzochten de auteurs de vier eiwitten om korte reeksen, of epitopen, te identificeren die naar verwachting door zowel T‑cellen als B‑cellen worden herkend. Uit honderden kandidaten selecteerden ze 15 epitopen die hoog scoorden voor herkenbaarheid door immuuncellen, en die bovendien als niet‑toxisch en niet‑allergeen werden voorspeld. Deze stukjes werden vervolgens aaneengeschakeld tot één lang eiwit, verbonden door zorgvuldig gekozen moleculaire "spacers" zodat elk epitoop toegankelijk zou blijven. Om de immuunrespons te versterken voegden ze drie bekende immuunstimulerende componenten uit bacteriële eiwitten als adjuvanten toe. Het resulterende construct, 678 bouwstenen (aminozuren) lang, werd voorspeld stabiel, oplosbaar en sterk antigenisch te zijn — eigenschappen die belangrijk zijn voor een vaccin in de praktijk.
Vorm en stevigheid van het ontwerp testen op de computer
Omdat de effectiviteit van een vaccin sterk afhangt van zijn driedimensionale vorm, bouwde het team 3D‑modellen van het nieuwe eiwit met verschillende geavanceerde structuurpredictieprogramma's. Ze verfijnden deze modellen herhaaldelijk en controleerden hun kwaliteit met standaard structurele maatstaven, en kozen een definitieve versie die voldeed aan strikte criteria voor realistische eiwitgeometrie en stabiliteit. Ze brachten ook in kaart welke oppervlakteregio's het gemakkelijkst door antilichamen vastgepakt zouden kunnen worden en ontwierpen nieuwe interne "bruggen" genaamd disulfidebindingen, die naar verwachting het eiwit verder zouden verstevigen en stabiliseren. Om na te bootsen hoe het vaccin zich in de waterige omgeving van het lichaam zou gedragen, voerden ze gedetailleerde moleculaire dynamicasimulaties uit van 100 miljardsten van een seconde in tien onafhankelijke runs. Gedurende deze simulaties bleef het model‑eiwit compact en structureel stabiel, wat suggereert dat het zijn beoogde vorm onder reële omstandigheden zou kunnen behouden.
Simuleren hoe het immuunsysteem reageert
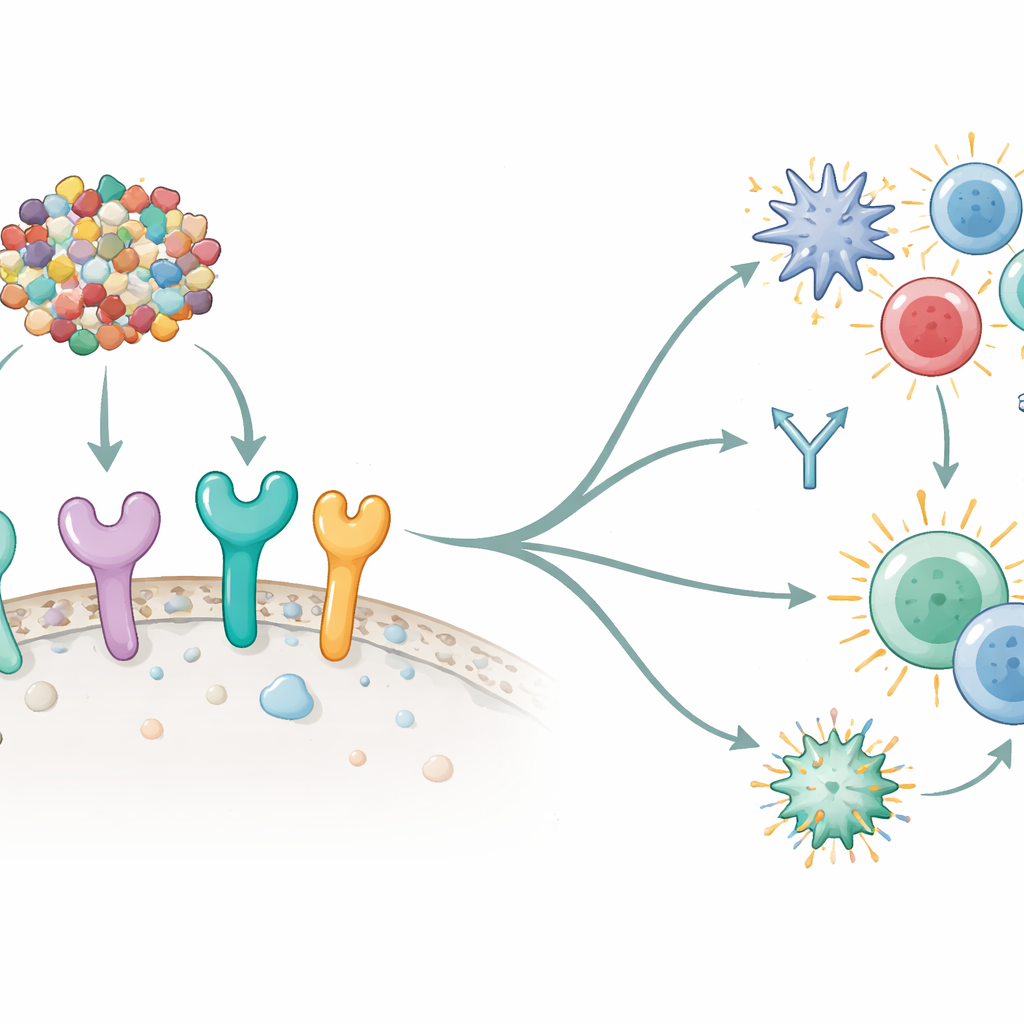
De onderzoekers vroegen zich vervolgens af of hun vaccin in principe met de belangrijkste "alarmsensoren" van het immuunsysteem kon communiceren — Toll‑achtige receptoren (TLR's) die op of in immuuncellen zitten. Computer dockingexperimenten toonden sterke, stabiele interacties tussen het vaccin en zes verschillende menselijke TLR's, met name TLR5 en TLR8, die bekendstaan om het op gang brengen van krachtige immuuncascade. Ze simulateerden daarna een volledig vaccinatieschema met immuunsysteem‑modelleringsoftware. In deze virtuele experimenten leidden drie doses van het vaccin tot snelle klaring van het gesimuleerde antigeen, sterke golven van antilichamen (vooral IgM en IgG1), en een toename van langlevende geheugen B‑cellen en T‑helpercellen. Belangrijke signaalmoleculen zoals interferon‑gamma en interleukines stegen ook, wat wijst op activatie van zowel de aangeboren als de verworven immuniteit — precies het evenwichtige antwoord dat gewenst is voor antitumorbescherming.
Voorbereiden op productie in de echte wereld
Om van concept naar laboratoriumtesten te gaan controleerde het team of het vaccin efficiënt geproduceerd kon worden in een veelgebruikte bacteriële werkpaard, Escherichia coli. Door de genetische code van het vaccin aan te passen zonder het eiwit zelf te veranderen, bereikten ze een optimaal patroon voor bacteriële eiwitproductie en een gebalanceerde chemische samenstelling van het DNA. Vervolgens voerden ze een virtuele kloonstap uit, waarbij ze het geoptimaliseerde gen in een standaard laboratoriumplasmide voor eiwitexpressie invoegden. Deze stappen suggereren dat, indien in het laboratorium opgepakt, het vaccin waarschijnlijk op schaal geproduceerd kan worden voor experimentele studies.
Wat dit kan betekenen voor toekomstige kankerzorg
Simpel gezegd levert dit werk een grondig computergetest blauwdruk voor een longkankervaccin dat eiwitten target die verbonden zijn met een bijzonder inflammatoire vorm van tumorceldood. Het ontwerp lijkt veilig, stabiel en in simulaties in staat om immuunverdediging sterk te activeren, met brede voorspelde dekking over menselijke populaties. Hoewel het nog een digitaal prototype is en moet worden gevalideerd in cellen, dieren en uiteindelijk mensen, illustreert de studie hoe moderne computationele tools jaren van trial‑and‑error kunnen samendrukken tot één geïntegreerd ontwerp. Als toekomstige experimenten deze voorspellingen bevestigen, zou zo’n vaccin op een dag bestaande behandelingen kunnen aanvullen en de eigen immuunrespons van patiënten betrouwbaarder kunnen helpen longtumoren herkennen en aanvallen.
Bronvermelding: Nguyen, T.L., Kim, H. Identification and evaluation of tumor pyroptosis-associated antigens for design a vaccine candidate against lung cancer. Sci Rep 16, 9559 (2026). https://doi.org/10.1038/s41598-024-84792-4
Trefwoorden: longkankervaccin, pyroptose, multi-epitoop immunotherapie, computationeel vaccindesign, tumorimmuunrespons