Clear Sky Science · nl
Een verenigde dataset voor het ontwerpen van antilichamen en nanobodies met sequentie-, structuur- en bindingsaffiniteitsgegevens
Waarom kleine immuungereedschappen en big data ertoe doen
Antilichamen en hun kleinere neven, nanobodies, zijn het lichaam’s precisiegeleide projectielen tegen infecties en kanker. Medicijnontwikkelaars proberen deze moleculen tegenwoordig op computers te ontwerpen, vergelijkbaar met hoe ingenieurs vliegtuigen ontwerpen. Maar tot voor kort was het ruwe materiaal voor dergelijke kunstmatige-intelligentiedesigns — betrouwbare gegevens over antilichaamcomponenten, vormen en hoe sterk ze aan hun doelen binden — verspreid over veel incompatibele databanken. Dit artikel introduceert de Antibody and Nanobody Design Dataset (ANDD), een verenigde, publieke hulpbron die onderzoekers voorziet van de schone, uitgebreide data die nodig zijn om de volgende generatie gerichte therapieën te ontwerpen.
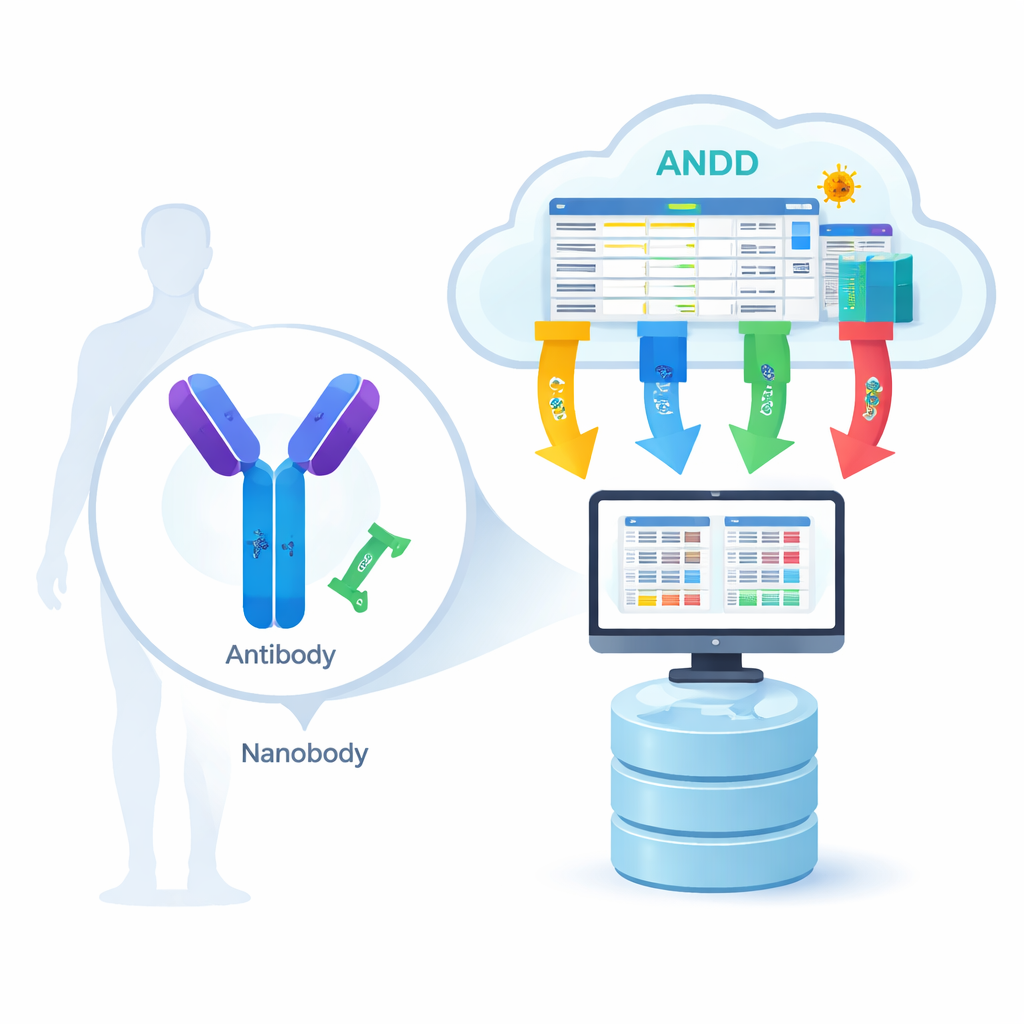
Van biologisch slot-en-sleutelprincipe naar digitale blauwdruk
Antilichamen zijn grote Y‑vormige eiwitten, terwijl nanobodies veel kleinere enkelvoudige versies zijn die voorkomen bij dieren zoals lama’s en alpaca’s. Beide herkennen specifieke “sloten” op virussen, kankercellen of andere ziektegerelateerde eiwitten. Voor computermodellen om te leren hoe deze herkenning werkt, hebben ze vier soorten informatie nodig voor veel verschillende voorbeelden: de aminozuursequentie (de onderdelenlijst), de 3D-structuur (de vorm), het antigeen (het doel) en de bindingssterkte (hoe strak de twee aan elkaar zitten). Tot nu toe bevatten de meeste bronnen slechts één of twee van deze onderdelen tegelijk, waardoor wetenschappers tussen databanken moesten schakelen en handmatig gegevens moesten samenvoegen, wat vooruitgang vertraagde en fouten introduceerde.
Verspreide gegevens samenbrengen in één georganiseerde bibliotheek
Het ANDD-team verzamelde gegevens uit 15 belangrijke bronnen, waaronder speciale antilichaam- en nanobody-databanken, algemene eiwitrepositoria en zelfs octroondocumenten. Deze ruwe input werd vervolgens door een zorgvuldig gescripte pijplijn gehaald: downloaden, herformatteren naar een gedeeld schema, kruiscontrole van identificatoren, verwijderen van duplicaten en harmoniseren van naamgevingsregels. Wanneer verschillende databanken het oneens waren, kregen gecureerde bronnen en directe experimenten prioriteit. Het eindresultaat is één tabel plus een set structuurbestanden die sequentie, structuur, doel en bindingsinformatie op een consistente manier verbinden, waarbij elk record is gemarkeerd zodat gebruikers precies kunnen nagaan waar het vandaan komt en hoe het is verwerkt.
Gelaagde detaillering voor verschillende onderzoeksbehoeften
Niet elke invoer in ANDD is even rijk aan informatie, daarom organiseerden de auteurs de collectie in lagen met toenemende detaillering. Op het breedste niveau zijn er 48.683 antilichaam- en nanobody-invoeren met sequentie-informatie. Een grote subset voegt 3D-structuren toe, en een kleinere subset bevat daarnaast sequenties van de doelproteïnen. De meest gedetailleerde laag — duizenden invoeren — voegt gemeten of voorspelde bindingssterkte toe. Voor antilichamen hebben bijvoorbeeld 18.464 invoeren sequenties, hetzelfde aantal combineert sequentie en structuur, meer dan 8.000 bevatten ook antigeensequenties, en 7.737 hebben volledige sequentie-, structuur-, antigeen- en affiniteitsgegevens. Een parallelle hiërarchie bestaat voor nanobodies, waardoor zowel experimenteerders als modelbouwers flexibiliteit hebben: zij kunnen kiezen voor grote, eenvoudige datasets of kleinere, informatie-rijkere subsets.
De hiaten in bindingssterkte opvullen
Bindingssterkte is cruciaal voor geneesmiddelontwerp, maar experimentele waarden zijn schaars en ongelijk gerapporteerd. Om dit gat te dichten zonder de grens tussen data en voorspelling te vervagen, gebruikten de auteurs een gespecialiseerd deep-learninginstrument, ANTIPASTI, om bindingssterktes te schatten uitsluitend voor invoeren die wel structuren hadden maar geen metingen. Deze 2.271 voorspelde waarden zijn duidelijk gelabeld en apart gehouden van de ongeveer 7.000 experimenteel gemeten waarden. Het team controleerde vervolgens de algehele consistentie met een ander model, AlphaBind, en door wiskundig gerelateerde maatstaven van binding te vergelijken. Sterke correlaties en lage fouten suggereren dat de gecureerde experimentele waarden betrouwbaar zijn en dat de voorspelde waarden zinvolle trends volgen zonder als absolute waarheid te gelden.
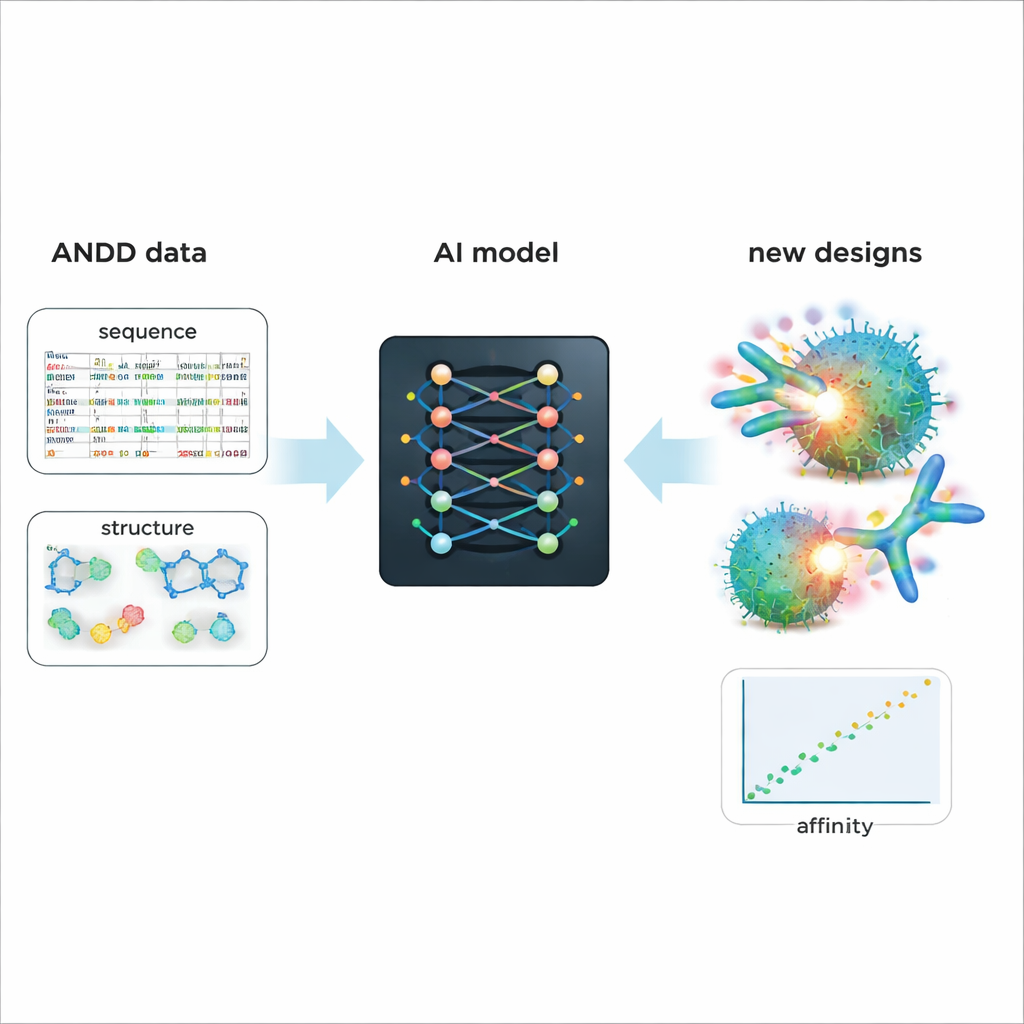
De basis voor slimmer ontwerp van toekomstige medicijnen
Om de praktische waarde van ANDD aan te tonen, verfijnden de auteurs een bestaand generatief AI-model dat antilichamen en nanobodies ontwerpt. Training op ANDD’s gecombineerde sequentie-, structuur-, doel- en affiniteitsinformatie leidde tot gegenereerde moleculen met betere voorspelde binding en realistischere vormen dan een basismodel dat op oudere, eenvoudigere data was getraind. Naast deze casestudy is ANDD openlijk beschikbaar onder een permissieve licentie, wordt geleverd met volledige documentatie en een reproduceerbare bouwpijplijn, en is het ontworpen om regelmatig te worden bijgewerkt. Voor niet‑specialisten is de kernboodschap dat ANDD een rommelig lappendeken van antilichaamgegevens omzet in een coherent, betrouwbaar naslagwerk — waardoor AI-tools een veel betere uitgangspositie krijgen om nauwkeurige, effectievere biologische geneesmiddelen te ontwerpen.
Bronvermelding: Wu, Y., Liu, X., Hrovatin, K. et al. A Unified Dataset for Antibody and Nanobody Design Including Sequence, Structure, and Binding Affinity Data. Sci Data 13, 295 (2026). https://doi.org/10.1038/s41597-026-06878-0
Trefwoorden: ontwerp van antilichamen, nanobodies, bindingsaffiniteit, biologische therapieën, AI-medicijnontdekking