Clear Sky Science · nl
Een single-cell transcriptomische dataset die traumatisch hersenletsel en NeuroD1-gebaseerde gentherapie bij muizen in kaart brengt
Waarom hersenletsels ons allemaal aangaan
Jaarlijks krijgen miljoenen mensen een klap tegen het hoofd door vallen, ongelukken, contactsporten of gevechten. Deze traumatische hersenletsels kunnen blijvende problemen veroorzaken met geheugen, beweging en stemming, en de huidige behandelingen richten zich meestal op symptoombeheer in plaats van op daadwerkelijke herstel van de hersenen. Deze studie onderzoekt een veelbelovende gengebaseerde aanpak bij muizen die niet alleen schade wil beperken, maar ook de hersenen van binnenuit wil helpen herbouwen. De veranderingen worden cel voor cel in kaart gebracht en beschikbaar gesteld als een publieke bron voor toekomstige therapieën.
Inzicht in het beschadigde brein
Wanneer de hersenen gewond raken, blauwe plekken ontstaan er niet zomaar zoals in een spier. Er ontvouwt zich een complexe ketenreactie: zenuwcellen sterven af, de bloedtoevoer raakt verstoord en ondersteunende cellen zoals astrocyten en immuuncellen rukken op. Astrocyten voeden normaal gesproken neuronen en houden de signaaloverdracht in balans, maar na een trauma kunnen ze een dichte littekenmassa vormen en langdurige ontsteking aanwakkeren. De auteurs gebruikten een gecontroleerde prikwond in de cortex van muizen om bepaalde vormen van penetrerend hersenletsel na te bootsen en onderzochten vervolgens hoe elk belangrijk celtype in het getroffen weefsel in de loop van de tijd reageerde. Ze pasten een techniek toe die single-cell RNA-sequencing heet, waarmee wordt gelezen welke genen in tienduizenden individuele cellen actief zijn, waardoor een gedetailleerde telling ontstaat van hoe de cellulaire samenstelling van de hersenen na letsel verandert.
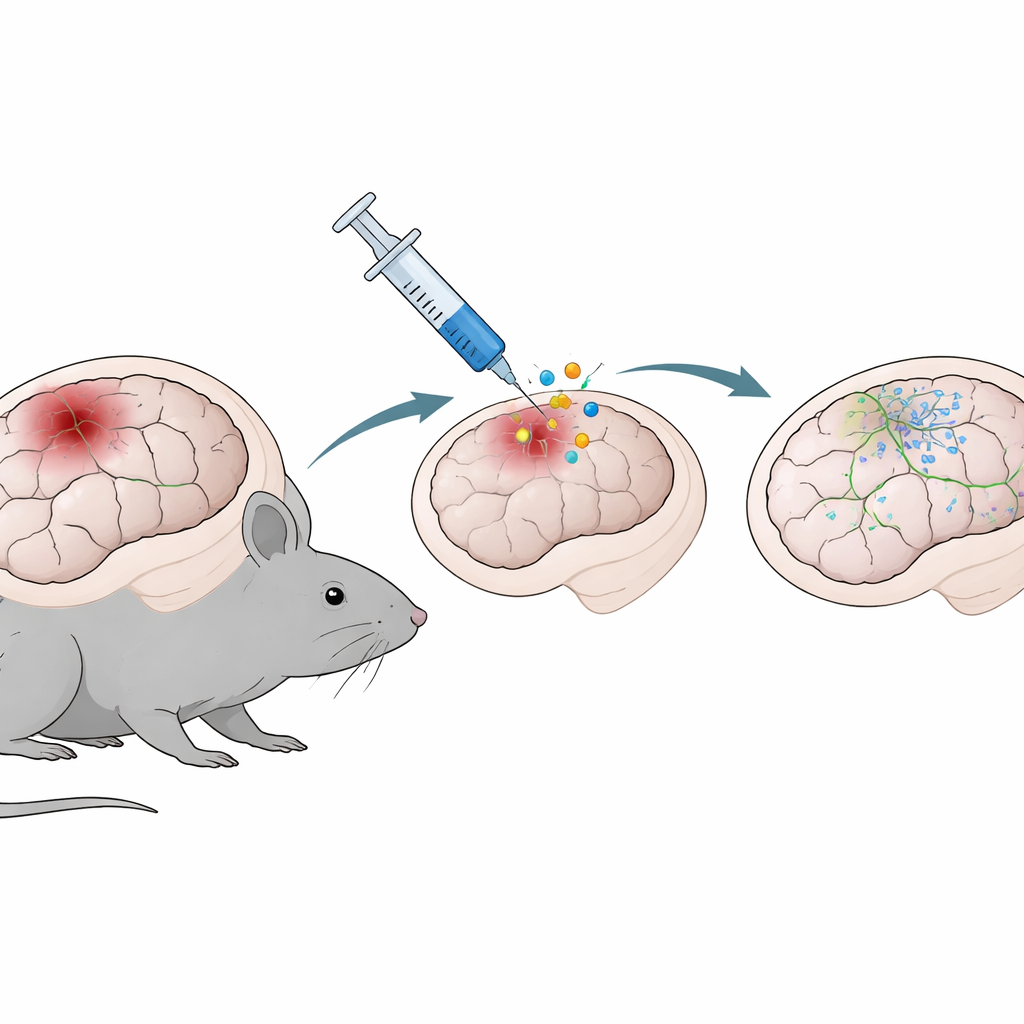
Een gentherapie die ondersteunende hersencellen inzet
Aangezien astrocyten overvloedig aanwezig zijn en zich precies op de plaats van het letsel bevinden, vormen ze aantrekkelijke doelwitten voor herstelstrategieën. Het team testte een gentherapie gebaseerd op NeuroD1, een gen dat bekendstaat om cellen in de richting van een neuronachtig stadium te duwen. Met een onschadelijke virale drager geïnjecteerd in het beschadigde corticale gebied drie dagen na het letsel leverden ze ofwel een neutrale marker (GFP) of NeuroD1 af in astrocyten. Bij onderzoek van de hersenen één en twee weken later hadden muizen die NeuroD1 kregen kleinere weefselholtes op de plek van het letsel en minder geactiveerde immuuncellen, microglia genaamd, rond de laesie. Met andere woorden, de therapie verminderde niet alleen zichtbare structurele schade maar kalmeerde ook de lokale ontstekingsreactie.
Celtellingen één voor één
Om te begrijpen wat ten grondslag lag aan deze verbeteringen, vergeleken de onderzoekers drie groepen corticale monsters: gezonde muizen, gewonde muizen die het controlevirus kregen, en gewonde muizen die het NeuroD1-virus kregen. Ze sequentieerden in totaal meer dan 97.000 individuele cellen en groepeerden die op basis van hun genactiviteitspatronen in bekende hersenbewoners, waaronder neuronen, astrocyten, oligodendrocyten (die zenuwvezels isoleren), microglia en cellen die bloedvaten en hersenkamers bekleden. Letsel alleen verschuift deze balans naar meer astrocyten en microglia en minder neuronen en myeline-vormende cellen, wat littekenvorming en ontsteking weerspiegelt. Met NeuroD1-behandeling begon deze scheve verdeling zich te herstellen: het aandeel neuronen, oligodendrocyten en choroïd plexus epitheelcellen nam toe, terwijl astrocyten en microglia minder dominant werden in de beschadigde zone.
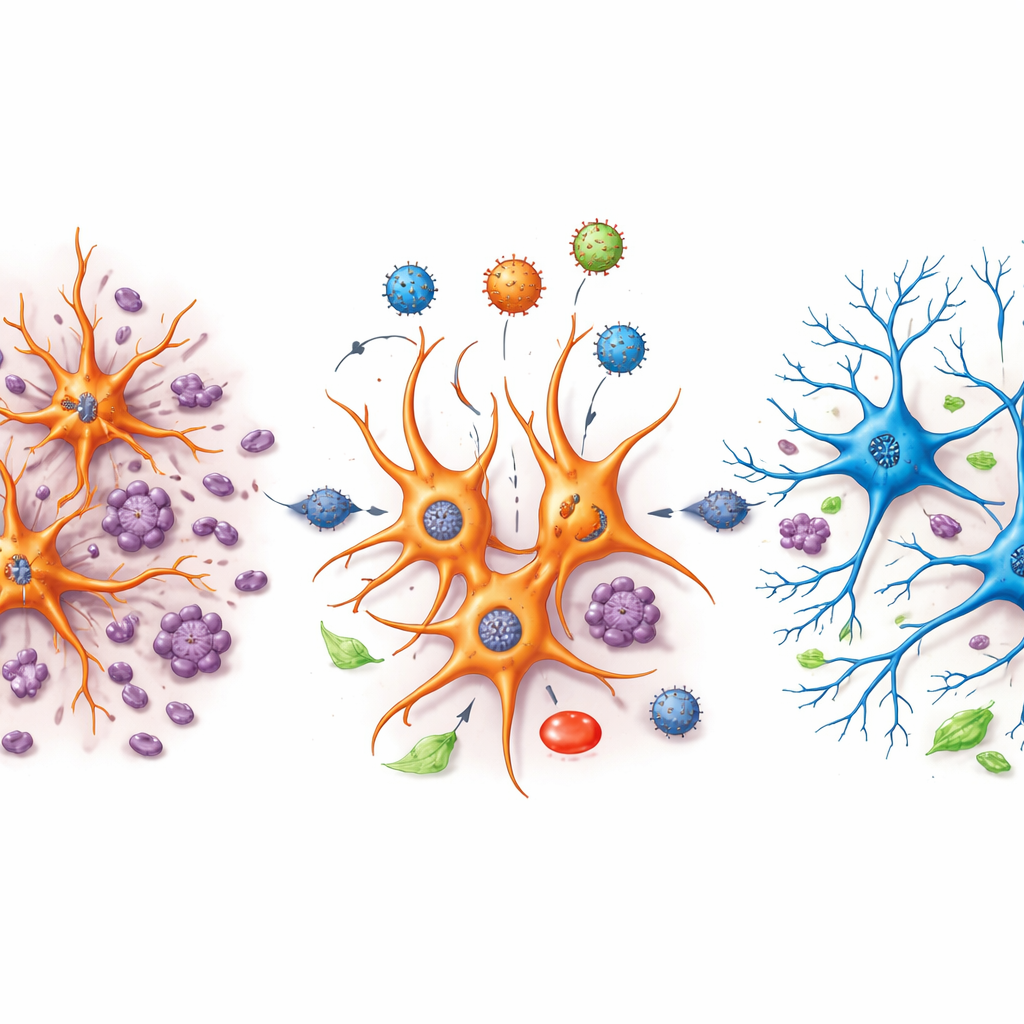
Het verborgen werk van astrocyt-subtypen
Astrocyten bleken geen uniforme populatie te zijn. Door ze afzonderlijk opnieuw te analyseren, identificeerde het team zeven verschillende astrocyt-subclusters, elk met een eigen gensignatuur en gedrag in de drie condities. Sommige subclusters waren veelvoorkomend in gezond weefsel maar verdwenen bijna na letsel, terwijl andere pas na trauma verschenen. In beschadigde hersenen behandeld met het controlevirus activeerden meerdere astrocytgroepen programma’s die betrokken zijn bij het bouwen en herschikken van synapsen—de verbindingen waarlangs neuronen communiceren—terwijl genen die gekoppeld zijn aan energieproductie in mitochondriën werden teruggeschroefd. Dit patroon suggereert dat astrocyten na letsel abnormale herbedradingsprocessen stimuleren terwijl hun metabolische capaciteit is verminderd.
Hoe NeuroD1 celenergie en bedrading in balans brengt
NeuroD1-behandeling vormde deze astrocyt-subclusters in een andere richting. In meerdere letselgerelateerde astrocytgroepen werden genen die horen bij mitochondriale activiteit, cellulaire ademhaling en algemene energiemetabolisme weer versterkt, terwijl genen die samenhangen met overmatige synapsopbouw en myelineherschikking werden afgezwakt. Met andere woorden, NeuroD1 leek de energiecentrales van deze cellen te herstellen en uit de hand lopende pogingen tot herbedrading te temperen die anders tot disfunctie kunnen bijdragen. Sommige astrocyt-subtypen die sterk waren toegenomen na letsel, krompen in aanwezigheid van NeuroD1, terwijl anderen die met gezondere functies geassocieerd worden toenamen. Deze fijne verschuivingen geven aanwijzingen welke astrocyt-staten schadelijk zijn en welke herstel kunnen ondersteunen.
Wat dit betekent voor toekomstig hersenherstel
Dit werk biedt nog geen kant-en-klare remedie voor menselijk hersenletsel, maar het levert twee belangrijke vooruitgangen. Ten eerste toont het aan in een levend zoogdierbrein dat een gerichte gentherapie weefselverlies en ontsteking kan verminderen terwijl populaties cellen en energiegebruik weer in een gezondere richting worden geduwd. Ten tweede stelt het een rijke, publieke single-cell dataset beschikbaar die andere wetenschappers kunnen benutten om specifieke celtypen, genen en paden te vinden die schade of herstel na trauma aansturen. Voor lezers buiten het lab is de kernboodschap dat de ondersteunende cellen van het brein mogelijk kunnen worden gerekruteerd en herprogrammeerd om beschadigde circuits te helpen herbouwen, waarmee we een stap dichter bij behandelingen komen die functioneren herstellen in plaats van alleen stabiliseren na een traumatische klap.
Bronvermelding: Chen, R., Zhang, S., Liu, S. et al. A single-cell transcriptomic dataset profiling traumatic brain injury and NeuroD1-based gene therapy in mice. Sci Data 13, 406 (2026). https://doi.org/10.1038/s41597-026-06788-1
Trefwoorden: traumatisch hersenletsel, gentherapie, astrocyten, single-cell sequencing, NeuroD1