Clear Sky Science · nl
HMI-LUSC: Een histologische hyperspectrale beeldgegevenenset voor plaveiselcelcarcinoom van de long
Kanker in nieuwe kleuren zien
Longkanker blijft een van de dodelijkste ziektes ter wereld, deels omdat het opsporen van elke laatste kankercel op een microscoopglasplaatje moeilijk en tijdrovend is. Pathologen vertrouwen doorgaans op roze‑ en paarstkleurig gekleurd weefsel onder de microscoop, een methode die structuur vastlegt maar subtiele chemische aanwijzingen mist. Dit artikel introduceert HMI‑LUSC, de eerste vrij toegankelijke verzameling microscoopbeelden van longplaveiselcelcarcinoom die niet slechts in drie kleuren, maar in tientallen smalle kleurbanden zijn vastgelegd, waardoor computers en clinici een veel rijker beeld krijgen van wat tumorcellen onderscheidt van hun gezonde buren.
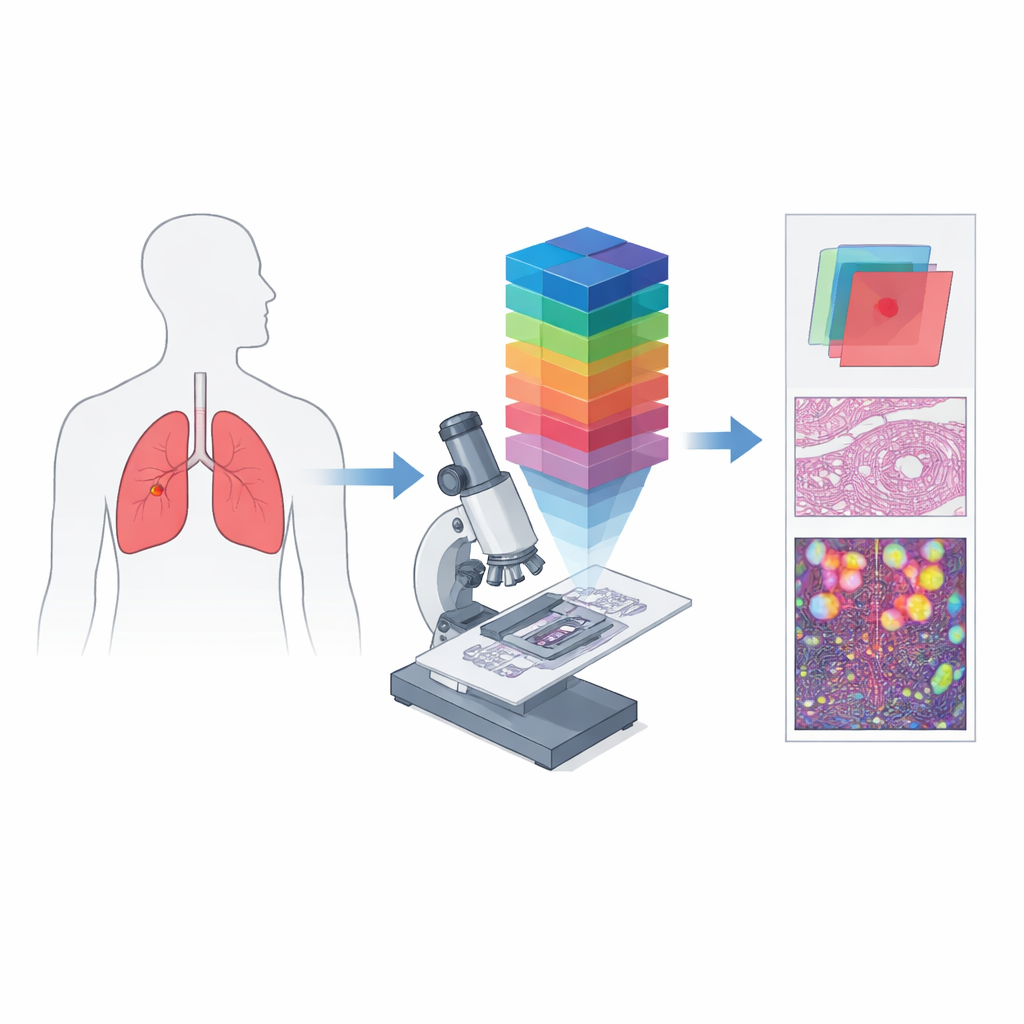
Van eenvoudige kleurenfoto’s naar spectrale vingerafdrukken
Conventionele digitale pathologie werkt veelal als een telefooncamera: ze registreert rood, groen en blauw om een benadering van wat het oog ziet vast te leggen. Hyperspectrale beeldvorming gaat een stap verder door licht op te splitsen in vele dicht opeenvolgende golflengten, waardoor een driedimensionale “datakubus” ontstaat waarin elk klein stukje weefsel zijn eigen gedetailleerde kleurspectrum heeft. Gecombineerd met een microscoop wordt dit hyperspectrale microscopische beeldvorming, in staat om zowel fijne structuur als rijke spectrale informatie op celniveau vast te leggen. Dergelijke gegevens kunnen verschillen onthullen in hoe weefsels licht absorberen en reflecteren die in standaardbeelden onzichtbaar zijn, waardoor unieke spectrale “handtekeningen” voor kankerachtige en niet‑kankerachtige gebieden ontstaan.
Een nieuwe bibliotheek voor longkankeronderzoek opbouwen
De auteurs creëerden HMI‑LUSC om een duidelijke leemte te vullen: vóór dit werk bestond er geen openbare hyperspectrale dataset voor longweefsel, wat het moeilijk maakte computergestuurde diagnostische methoden te testen en te vergelijken. Ze verzamelden weefsel van tien patiënten die een longtumoroperatie ondergingen, maakten standaard hematoxyline‑en‑eosine‑preparaten en scanden deze op hoge resolutie. Ervaren pathologen markeerden tumor‑ en normale gebieden, en representatieve regio’s werden opnieuw gefotografeerd met een speciaal gebouwde hyperspectrale microscoop. Elk resulterend beeld bestrijkt een klein weefselvlak maar omvat 61 golflengten tussen 450 en 750 nanometer, met een resolutie van 3088 bij 2064 pixels. Voor elke regio bevat de dataset de ruwe spectrale kubus, een conventionele RGB‑weergave en maskers die aangeven waar tumorgeleid aanwezig is.
Van grove omtrekken naar kaartjes op celniveau
Hoewel aanduidingen op glazenniveau nuttig zijn, vereist het trainen van moderne algoritmen vaak informatie op het niveau van individuele cellen. Het handmatig traceren van elke cel is onpraktisch, dus ontwierp het team een semi‑automatische workflow. Eerst groepeerden ze pixels in clusters op basis van hun spectrale gelijkenis met een standaard computer‑visiemethode. Vervolgens inspecteerden pathologen deze clusters als overlay op het weefselbeeld en verdeelden ze in vier categorieën: tumorcellen, niet‑tumorcellen, niet‑cellig weefsel zoals stroma of bloed, en lege achtergrond. Een tweede patholoog controleerde en paste deze resultaten aan, waarbij meningsverschillen door consensus werden opgelost. Het resultaat is een set gedetailleerde pixel‑gewijze maskers die subtiele mengsels van celtypen en verwarrende grenszones vastleggen, en daarmee veel rijker lesmateriaal bieden voor machine‑learningsystemen.
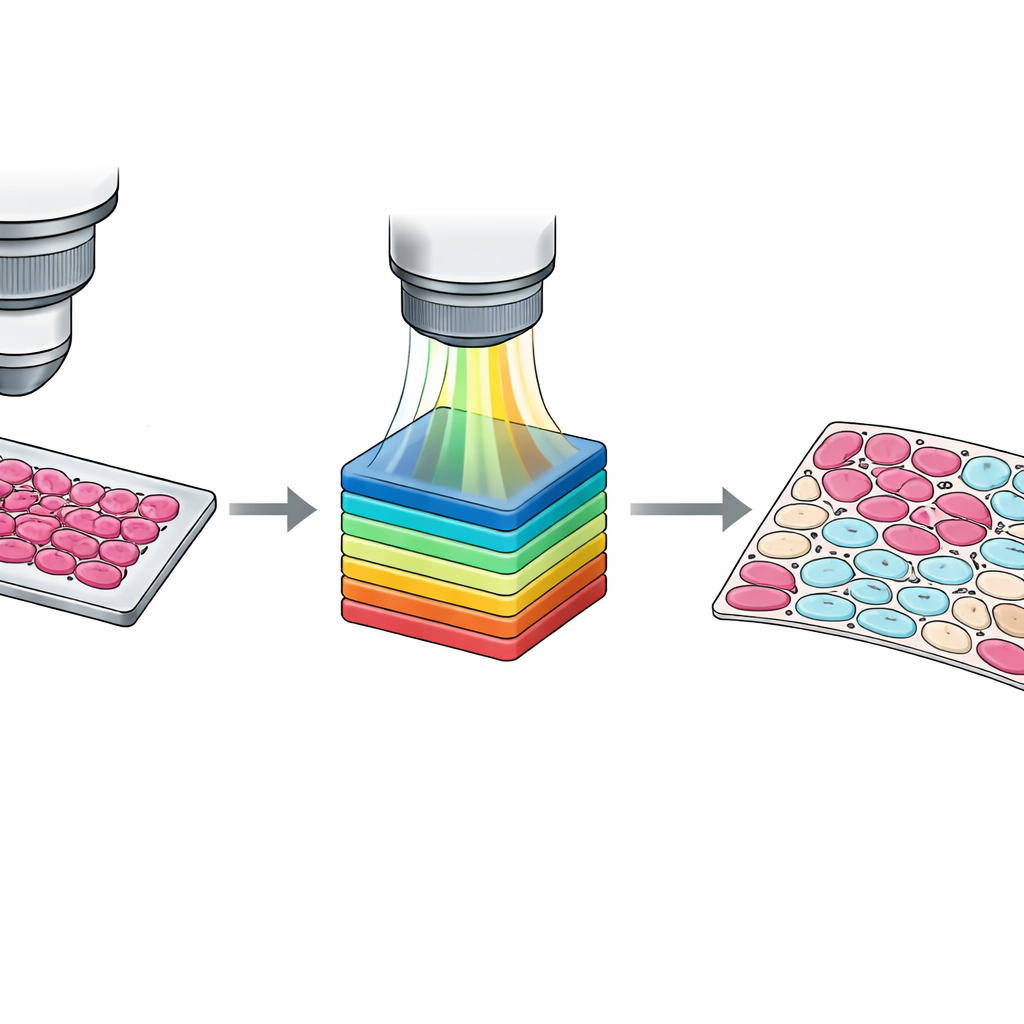
Zorgdragen voor scherpe en betrouwbare data
Om de dataset betrouwbaar te maken, hebben de auteurs hun beeldvormingssysteem grondig getest. Ze verifieerden dat de microscoop fijne patronen tot ongeveer één micron kan oplossen—klein genoeg om individuele cellen te onderscheiden—en dat ruis in de meeste golflengten laag is. Ze vergeleken ook het gemeten spectrum van een standaardlichtbron met referentiecurves en met een commercieel hyperspectraal camera, en vonden uitstekende overeenstemming. Ten slotte toonden ze hoe de gegevens kunnen worden gebruikt door basismodellen uit te voeren, van klassieke machine‑learningmethoden tot eenvoudige deep‑learningnetwerken, voor het segmenteren van tumorgebieden. Zelfs zonder sterke optimalisatie behaalden deze modellen degelijke nauwkeurigheid, wat aantoont dat de dataset geschikt is als referentie voor toekomstige methoden.
Wat dit betekent voor toekomstige zorg bij longkanker
HMI‑LUSC vervangt geen grote verzamelingen standaardpreparaten, en is op zichzelf nog geen klinisch hulpmiddel. Het biedt onderzoekers echter een zorgvuldig samengestelde inkijk in hoe longtumorcellen verschillen van nabijgelegen weefsel over veel golflengten van licht. Door deze gegevens, labels en code openlijk beschikbaar te maken, bieden de auteurs een gemeenschappelijke testomgeving voor het ontwikkelen en vergelijken van algoritmen die spectrale informatie gebruiken, van eenvoudige classifiers tot geavanceerde neurale netwerken. Op de lange termijn kan dergelijk werk computers helpen pathologen te assisteren bij het nauwkeuriger en sneller opsporen van tumoren, en mogelijk spectrale patronen blootleggen die samenhangen met tumortype of behandelreactie die gewone beelden niet kunnen tonen.
Bronvermelding: Yan, Z., Huang, H., Guo, Y. et al. HMI-LUSC: A Histological Hyperspectral Imaging Dataset for Lung Squamous Cell Carcinoma. Sci Data 13, 415 (2026). https://doi.org/10.1038/s41597-026-06766-7
Trefwoorden: hyperspectrale beeldvorming, longkanker, digitale pathologie, tumorsegmentatie, medische beeldgegevenenset