Clear Sky Science · nl
Groot histologisch beeldendatabestand met metadata voor het micro-omgeving van colorectaalkanker
Waarom het in kaart brengen van de verborgen omgeving van kanker ertoe doet
Wanneer artsen een colontumor onder de microscoop bekijken, zien ze niet alleen kankercellen; ze zien een drukke omgeving van vet, immuuncellen, bindweefsel en meer. Deze mix van celtypen, de tumor-micro-omgeving genoemd, beïnvloedt sterk hoe een patiënt op behandeling reageert en hoe lang hij of zij leeft. Computers die artsen zouden kunnen helpen deze complexe scènes te doorgronden, werden echter belemmerd door een eenvoudig probleem: er waren niet genoeg zorgvuldig gelabelde beelden om van te leren. Deze studie introduceert een van de grootste en meest zorgvuldig geannoteerde beeldverzamelingen van colorectale kankergewebe ooit samengesteld, speciaal ontworpen om moderne kunstmatige-intelligentiesystemen te trainen en te testen.
Een enorme beeldbibliotheek van darmtumoren opbouwen
De onderzoekers creëerden een bron die ze HMU-CRC-Hist550K noemen, opgebouwd uit weefselmonsters van 500 patiënten behandeld voor colorectale kanker in een groot kankerziekenhuis in China. De tumor van elke patiënt werd geconserveerd, volgens de standaardmethoden in pathologielaboratoria gekleurd en gescand tot een digitale dia met hoge resolutie. Uit deze dia’s sneed het team automatisch kleine vierkante beeldtegels, elk ongeveer zo groot als wat een patholoog in één keer door een microscoop zou kunnen zien. In totaal produceerden ze ongeveer 550.000 zulke tegels, waarmee kunstmatige-intelligentie-modellen een enorme en gevarieerde reeks voorbeelden kregen om te leren hoe verschillende weefsels eruitzien.
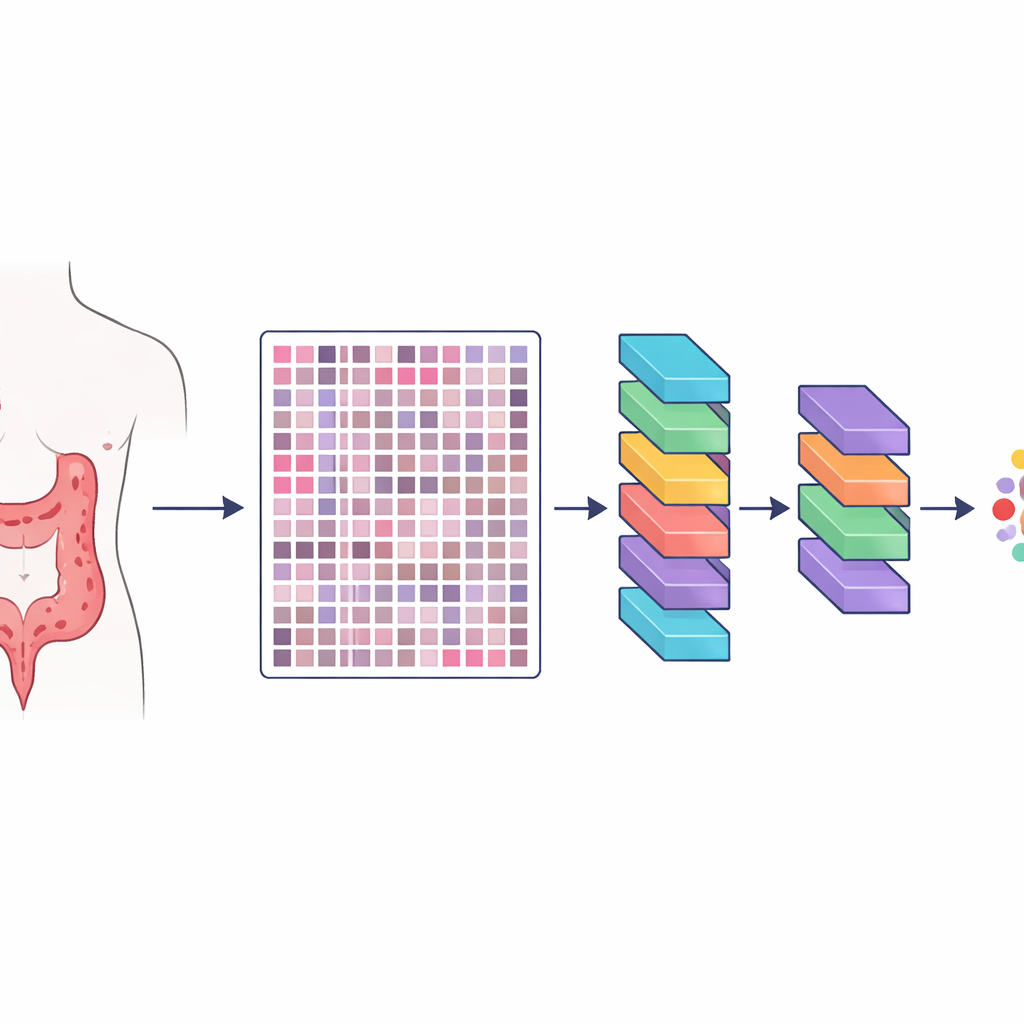
Zorgvuldige menselijke labeling van het kankerlanschap
Een grote beeldbibliotheek maken is niet genoeg; de beelden moeten ook nauwkeurig gelabeld worden. Drie ervaren pathologen werkten samen via een driestappenproces om acht belangrijke componenten van de tumoromgeving aan te geven: vetweefsel, cellulaire resten, immuuncellen genaamd lymfocyten, slijm, glad spierweefsel, normaal colonepitheel, ondersteunend bindweefsel rond de tumor, en de kankercellen zelf. Twee pathologen tekenden eerst onafhankelijk regio’s op de grote dia’s en controleerden vervolgens elkaars werk. Een senior specialist voerde een laatste beoordeling uit, loste meningsverschillen op en sloot onduidelijke gebieden uit. Deze kruiscontrole verminderde persoonlijke bias sterk en leverde zeer consistente labels op in fijn detail, zodat elke tegel gekoppeld is aan een specifiek weefseltype binnen de tumoromgeving.
Microscoopbeelden koppelen aan patiëntverhalen
Wat deze dataset bijzonder krachtig maakt, is dat de beelden gekoppeld zijn aan rijke klinische informatie per patiënt. Voor elk geval verzamelde het team basisgegevens zoals leeftijd en geslacht, evenals tumorrisico, de locatie van de tumor langs colon en rectum, hoe afwijkend de kankercellen eruitzagen, of zenuwen of lymfeklieren waren aangedaan, en hoe lang de patiënt na behandeling overleefde. Ze noteerden ook resultaten van veelvoorkomende laboratoriumtests die het genetische en eiwitprofiel van de tumor weerspiegelen. Alle persoonlijke identificerende gegevens werden verwijderd zodat patiënten niet te herkennen zijn. Door weefselpatronen met deze klinische kenmerken te combineren, kunnen onderzoekers onderzoeken hoe specifieke micro-omgevingsindelingen samenhangen met reële uitkomsten, zoals welke patiënten het beter of slechter doen.
AI op de proef stellen met de nieuwe dataset
Om te laten zien dat de dataset echt nuttig is, trainden de wetenschappers drie verschillende diep-lerende modellen — moderne patroonherkenningssystemen die uitblinken in beeldtaken — om de acht weefseltypen in de tegels te herkennen. Ze gebruikten strikte regels om patiënten tussen trainings- en testgroepen te verdelen, zodat de modellen beoordeeld werden aan de hand van patiënten die ze nog nooit eerder hadden gezien. De modellen, waaronder zowel klassieke beeldnetwerken als een nieuwere “vision transformer”-architectuur, behaalden allemaal zeer hoge nauwkeurigheid, met prestatiescores die op meerdere testsets dicht bij perfectie lagen. Het team vergeleek de resultaten ook met andere geavanceerde beeldsegmentatiemethoden en vond vergelijkbaar sterke prestaties. Visuele hulpmiddelen werden gebruikt om te benadrukken op welke delen van het weefsel de modellen zich baseerden, waarmee werd bevestigd dat ze zich richtten op medisch betekenisvolle regio’s in plaats van willekeurige patronen.
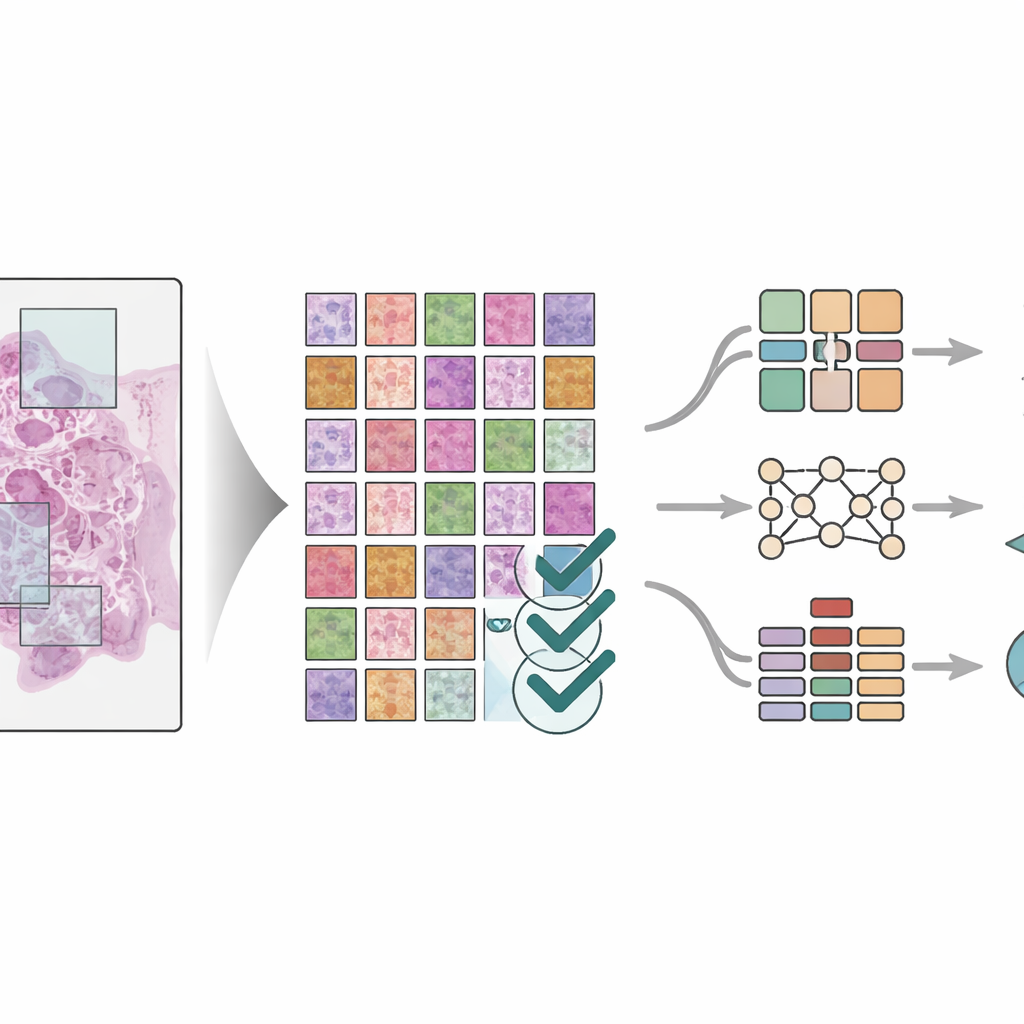
Wat dit betekent voor toekomstige kankerzorg
Voor niet-specialisten is de kernboodschap dat dit werk geen nieuwe behandeling introduceert, maar eerder een krachtige basis voor slimmer diagnostiek en prognose legt. Door een grote, goed georganiseerde en openlijk beschikbare beeldbibliotheek te delen die gekoppeld is aan gedetailleerde patiëntgegevens, stellen de auteurs onderzoekers wereldwijd in staat AI-hulpmiddelen op dezelfde stevige grond te bouwen en te vergelijken. Zulke hulpmiddelen zouden uiteindelijk pathologen kunnen helpen de tumoromgeving sneller en consistenter in kaart te brengen, voorspellen welke patiënten een hoger risico lopen en meer gepersonaliseerde behandelstrategieën suggereren. Hoewel de huidige gegevens slechts momentopnames vastleggen en geen veranderingen over maanden of jaren, is deze bron een belangrijke stap in de richting van het gebruik van digitale pathologie en AI om colorectale kanker beter te begrijpen en uiteindelijk beter te behandelen.
Bronvermelding: Wang, H., Li, H., Xue, J. et al. Large-Scale Histological Image Dataset with Metadata for Colorectal Cancer Microenvironment. Sci Data 13, 431 (2026). https://doi.org/10.1038/s41597-026-06675-9
Trefwoorden: colorectale kanker, tumor-micro-omgeving, digitale pathologie, diep leren, medische beelddatabank