Clear Sky Science · nl
De 2024 Brain Tumor Segmentation Challenge Meningioma Radiotherapy (BraTS-MEN-RT) dataset
Waarom het in kaart brengen van hersentumoren belangrijk is
Wanneer iemand behandeld wordt voor een hersentumor, moeten artsen de straling nauwkeurig richten: genoeg om tumoren te doden, maar niet zo veel dat gezond hersenweefsel wordt beschadigd. Bij een veelvoorkomend type hersentumor, het meningeoom, hangt deze richtingsbepaling af van deskundigen die de tumor met de hand aftekenen op driedimensionale MRI-scans. Dat werk is traag, nauwgezet en kan per specialist verschillen. Dit artikel beschrijft een grote nieuwe internationale dataset die vastlegt hoe experts meningeomen afbakenen voor radiotherapie, en legt zo de basis voor computerprogramma’s die dit sneller en consistenter kunnen doen.
Een veelvoorkomende hersentumor met een complexe behandeling
Meningeomen ontstaan uit de hersenvliezen en zijn de meest voorkomende primaire hersentumoren bij volwassenen. Veel zijn langzaam groeiend en goedaardig, maar anderen kunnen na een operatie terugkeren of zich agressiever gedragen, waardoor radiotherapie een belangrijk onderdeel van de behandeling is. Voordat men bestraling toedient, moeten clinici op MRI het “doelvolume” definiëren: de volledige omvang van de tumor en, in postoperatieve gevallen, de chirurgische holte waar tumorcellen kunnen achterblijven. Dat is ingewikkelder dan het klinkt. Littekens, veranderingen door een operatie, metalen implantaten en gespecialiseerde hoofdframes die gebruikt worden voor gerichte bestraling kunnen beelden vervormen en de tumorgrens moeilijk zichtbaar maken, zelfs voor ervaren deskundigen.
Een gedeelde beeldbibliotheek opbouwen
Om deze cruciale stap te verbeteren, bundelden onderzoekers van zeven grote centra in de Verenigde Staten en het Verenigd Koninkrijk hun krachten om de BraTS-MEN-RT dataset te creëren. Deze bevat 750 MRI-onderzoeken die werden gebruikt in echte radiotherapieschema’s voor patiënten met een meningeoom, waarvan 570 scans en 500 door experts getekende doelvolumes publiek beschikbaar zijn. De scans zijn contrastversterkte 3D-MRI-beelden die nauw aansluiten bij wat artsen daadwerkelijk gebruiken in de planningskamer: ze behouden de oorspronkelijke resolutie en oriëntatie en omvatten het hele hoofd, niet alleen de hersenen. De gevallen bestrijken een breed leeftijdsbereik, mannen en vrouwen, intacte tumoren en postoperatieve situaties, en meerdere typen bestralingstherapie. Deze diversiteit is essentieel voor het trainen van computermodellen die betrouwbaar moeten werken in verschillende ziekenhuizen en op verschillende scanners.
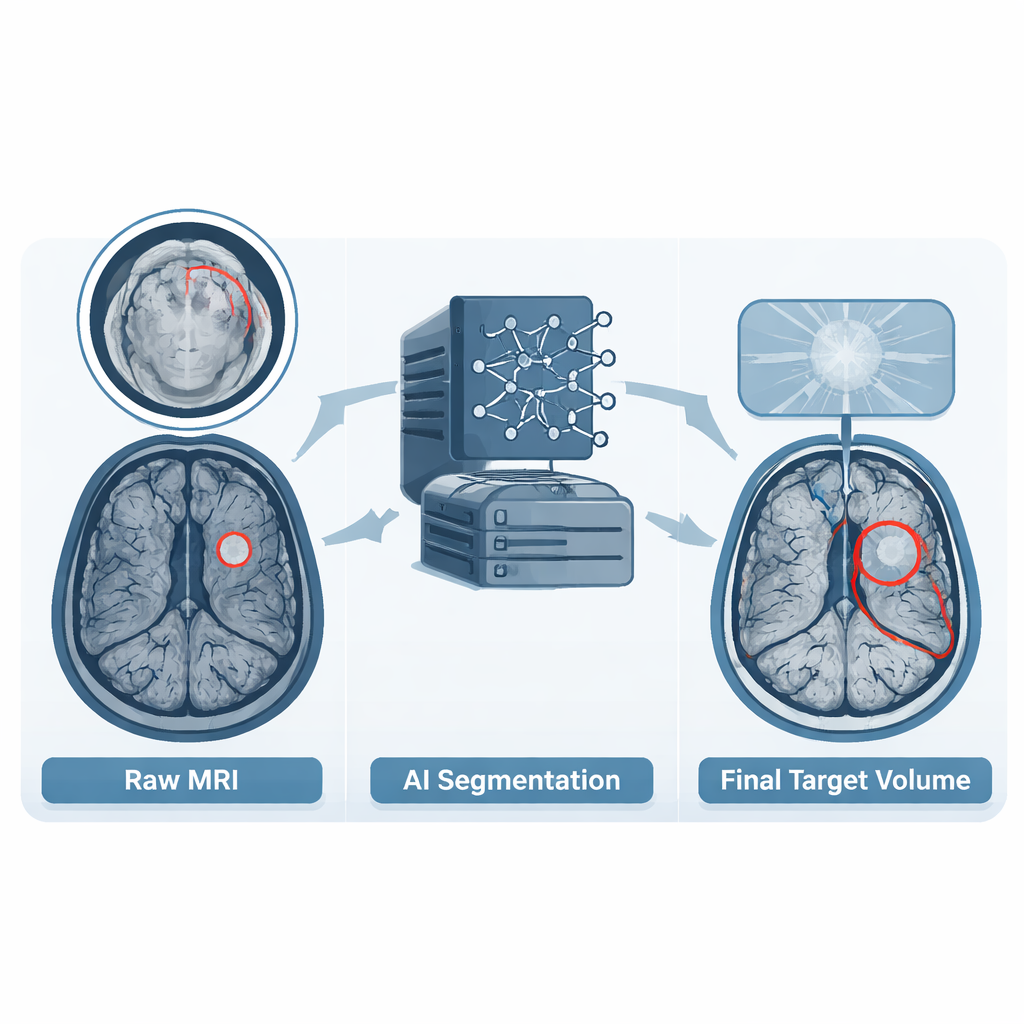
Privacy beschermen terwijl het medische relevante blijft
Aangezien elke MRI ook iemands gezicht vastlegt, nam het team speciale maatregelen om de identiteit van patiënten te beschermen. Ze gebruikten een geautomatiseerde methode die gelaatstrekken uit de beelden verwijdert terwijl de schedel, hersenen en tumoren intact blijven. Elke ontdane scan werd vervolgens laag voor laag gecontroleerd door een neuroradioloog en een radiotherapeut-oncoloog om zeker te zijn dat geen tumormateriaal per ongeluk was weggesneden, vooral bij tumoren nabij de schedelbasis. Als een tumor te ver in het verwijderde gebied reikte en niet veilig kon worden hersteld, werd dat geval uitgesloten. Deze balans tussen privacy en medische bruikbaarheid is cruciaal om grote beeldverzamelingen veilig deelbaar te maken.
Deskundig oordeel omzetten in trainingsmateriaal
Naast de beelden bevat de dataset gedetailleerde contouren van de tumorregio’s, bekend als gross tumor volumes. Wanneer ziekenhuizen deze volumes al hadden getekend in hun routinematige planning, werden die contouren als uitgangspunt gebruikt. In andere gevallen, of wanneer contouren niet aan afgesproken richtlijnen voldeden, gebruikte het team een modern deep-learningmodel om een initiële schatting te maken. Een resident in de radiotherapie beoordeelde vervolgens elk geval laag voor laag en paste de grenzen aan zodat ze voldeden aan de huidige behandelstandaarden en voegde eventuele aanvullende tumorhaarden toe die gemist waren. Ten slotte controleerde een gecertificeerde neuroradioloog elke contour en vroeg om verdere verfijningen indien nodig. Dit meerstapsproces veranderde uiteenlopende praktijken uit de dagelijkse klinische routine in een eenduidige, consistente referentieset waar computers van kunnen leren.
Hoe dit de zorg voor patiënten vooruit helpt
Door deze zorgvuldig samengestelde dataset vrij beschikbaar te maken voor de onderzoeksgemeenschap, leveren de auteurs het ontbrekende ingrediënt om algoritmen te bouwen en te testen die automatisch meningeoomdoelen op radiotherapieplanningsscans kunnen in kaart brengen. Als zulke hulpmiddelen nauwkeurig blijken, kunnen ze clinici tijd besparen, variatie tussen experts en instellingen verminderen en helpen verzekeren dat meer patiënten precies gerichte bestraling krijgen. In eenvoudige termen zet dit werk duizenden uren specialistisch werk om in een herbruikbare bron die de behandeling van hersentumoren veiliger, consistenter en beter toegankelijk kan maken.
Bronvermelding: LaBella, D., Schumacher, K., Mix, M. et al. The 2024 Brain Tumor Segmentation Challenge Meningioma Radiotherapy (BraTS-MEN-RT) dataset. Sci Data 13, 306 (2026). https://doi.org/10.1038/s41597-026-06649-x
Trefwoorden: meningeoom, radiotherapie, MRI, tumorsegmentatie, medische beeldvorming dataset