Clear Sky Science · nl
Tijdelijke multiomics-genexpressiegegevens tijdens differentiatie van menselijk embryonaal stamcel-afgeleide polyhormonale cellen
Hoe cellen leren organen te worden
Ons lichaam begint als kleine cluster van identieke cellen die op de een of andere manier leren uiteenlopende weefsels te vormen, van hersenen tot alvleesklier. Deze studie volgt dat leerproces in het laboratorium door gebruik te maken van menselijk embryonaal stamcellen die stap voor stap worden gestuurd naar vroege pancreatische cellen. Door de activiteit van duizenden genen door de tijd heen op meerdere niveaus te volgen, creëert het werk een rijk referentiekaartje dat onderzoekers kan helpen de menselijke ontwikkeling beter te begrijpen en op langere termijn strategieën voor de behandeling van ziekten zoals diabetes te verbeteren.
Stemcellen zien een pad kiezen
Menselijke embryonale stamcellen zijn bijzonder omdat ze vrijwel elk celtype in het lichaam kunnen worden. In deze studie leidden onderzoekers deze stamcellen naar een specifieke bestemming: een pancreatische lijn die polyhormonale cellen wordt genoemd, die sleutelhormonen zoals insuline en glucagon kunnen produceren. Ze imiteerden vroege ontwikkeling in een schaaltje door mediumstappen te wijzigen, waarbij cellen eerst in een primitieve darmachtige toestand—endoderm—werden gebracht en vervolgens in de loop van 17 dagen naar hormoonproducerende pancreatische cellen ontwikkelden. Monsters werden op tien zorgvuldig gekozen tijdstippen genomen om de hele reis van flexibele stamcel naar gespecialiseerde hormoonproducerende cel vast te leggen. 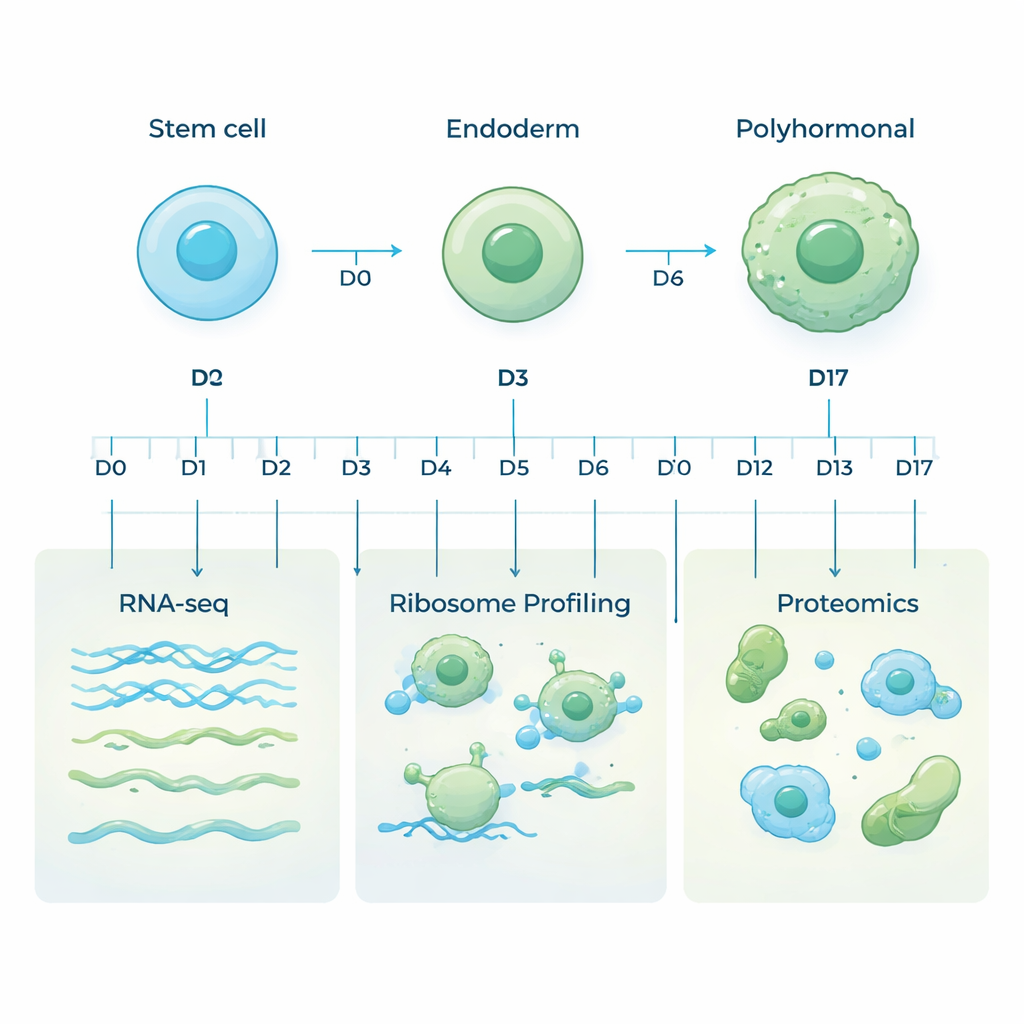
Onder de motorkap kijken op drie niveaus
De meeste studies kijken alleen naar boodschapper-RNA (mRNA), de moleculen die genetische instructies dragen. Maar mRNA is slechts een deel van het verhaal: niet elk bericht wordt vertaald naar eiwit, en eiwitten kunnen op verschillende snelheden worden gemaakt of afgebroken. Om een vollediger beeld te krijgen, gebruikte het team drie complementaire benaderingen op dezelfde monsters. RNA-sequencing bepaalde welke genen werden afgeschreven naar mRNA. Ribosoomprofilering volgde welke boodschappen actief werden gelezen door de eiwitproductiemachines van de cel. Massaspectrometrie-gebaseerde proteomics mat vervolgens de daadwerkelijke aanwezige eiwitten. Samen onthullen deze lagen hoe genactiviteit wordt gereguleerd terwijl cellen hun identiteit veranderen.
Belangrijke signalen van celidentiteit volgen
Om te controleren of de cellen echt het bedoelde ontwikkelingspad volgden, hielden de wetenschappers bekende markergenen in de gaten. Vroeg waren klassieke stamcelmarkers zoals OCT4 en NANOG hoog en namen ze af naarmate differentiatie vorderde. Toen cellen het endodermstadium binnengingen, stegen markers zoals KIT en SOX17. In de laatste fasen verschenen de polyhormonale markers insuline (INS) en glucagon (GCG) sterk op zowel RNA- als eiwitniveau, wat bevestigt dat de cellen een pancreashormoon-producerende identiteit hadden aangenomen. Hoewel één van de biologische replicaten iets langzamer door deze stadia ging dan de andere, volgden beide hetzelfde algemene pad, wat wijst op kleine natuurlijke verschillen en niet op technische fouten. 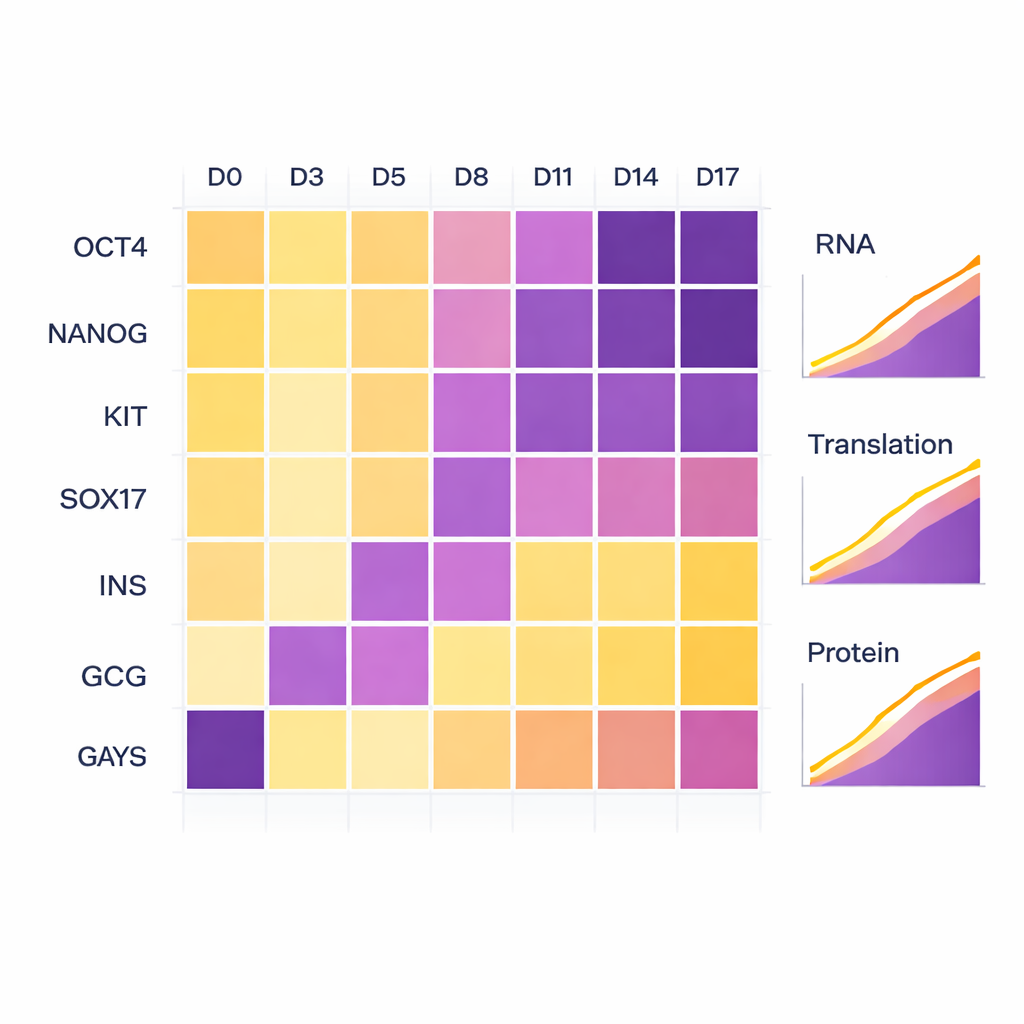
Kwaliteitscontroles voor een betrouwbare bron
Omdat dit werk bedoeld is als een communityresource, besteedden de auteurs uitgebreide moeite aan het controleren van datakwaliteit en consistentie. Voor elk van de drie methoden beoordeelden ze sequencing- en meetnauwkeurigheid, dekking van genen en de overeenstemming tussen herhaalde experimenten. Stamcel- en polyhormonale stadia vertoonden duidelijke en reproduceerbare verschillen op RNA-, translatie- en eiwitniveaus. Principale componentenanalyses—statistische kaarten die vergelijkbare monsters groeperen—lieten zien dat tijdpunten in volgorde lagen, met vroege en late stadia duidelijk gescheiden en biologische replicaten die nauw samenclusteren. De proteomicsgegevens alleen volgden betrouwbaar bijna 7.500 eiwitten over alle tijdpunten, met relatief weinig ontbrekende metingen, wat de diepgang van de dataset onderstreepte.
Een basis voor toekomstige ontdekkingen
De auteurs maken alle ruwe en verwerkte gegevens openbaar beschikbaar, samen met analysecodes en referentiebestanden, zodat andere onderzoekers de dataset kunnen hergebruiken en opnieuw analyseren. Verder dan het beschrijven van hoe het ene celtype in het andere verandert, biedt dit werk een gedetailleerd tijdsge-resolveerd beeld van hoe genberichten, hun translatie en resulterende eiwitten tijdens een belangrijke ontwikkelingsovergang met elkaar omgaan. Voor niet-specialisten is de belangrijkste conclusie dat celfate wordt gecontroleerd door meerdere regulatielagen die in de loop van de tijd samenwerken, en dat deze dataset een hoogresolutief "filmpje" van die veranderingen levert. Wetenschappers kunnen deze bron nu gebruiken om te onderzoeken waarom sommige genen vroeg veranderen en andere laat, hoe verschillende organen vergelijkbare of verschillende regels kunnen volgen, en hoe stamcellen beter naar medisch nuttige bestemmingen kunnen worden geleid.
Bronvermelding: Keskin, A., Shayya, H.J., Patel, A. et al. Temporal multiomics gene expression data across human embryonic stem cell-derived polyhormonal cell differentiation. Sci Data 13, 278 (2026). https://doi.org/10.1038/s41597-026-06606-8
Trefwoorden: stamcellen, pancreasontwikkeling, genexpressie, multiomics, polyhormonale cellen