Clear Sky Science · nl
Een CT-dataset met RECIST-metingen en uitgebreide segmentatiemaskers voor tumoren en lymfeklieren
Waarom deze kankerbeeldvormingsbron ertoe doet
De zorg voor kanker steunt steeds meer op medische beelden om te bepalen of behandelingen effect hebben. Toch zijn de zorgvuldige, plak‑voor‑plak metingen die artsen op CT-scans uitvoeren tijdrovend en kunnen ze tussen experts verschillen. Dit artikel presenteert een nieuwe, vrij beschikbare verzameling CT-scans van kankerpatiënten, waarbij tumoren en lymfeklieren nauwgezet zijn omlijnd en gemeten volgens een veelgebruikt klinisch protocol. De dataset is bedoeld om onderzoekers te helpen computersystemen te bouwen en testen die op termijn veel van dit eentonige werk kunnen overnemen en het monitoren van kankerbehandeling wereldwijd sneller en consistenter kunnen maken.
Hoe artsen momenteel tumoren volgen
Om te beoordelen of een kankerbehandeling helpt, volgen radiologen vaak een standaard die RECIST 1.1 heet. In de praktijk betekent dat dat ze een paar “target”-tumoren kiezen op de CT-scans van een patiënt en de langste zichtbare diameter van elk in millimeters noteren. In de tijd vergelijken ze de som van deze diameters met eerdere scans om te beslissen of de ziekte gekrompen, stabiel gebleven of gegroeid is. Hoewel deze methode veel broodnodige orde bracht in klinische onderzoeken, heeft ze ook nadelen: ze hangt sterk af van welke tumoren de arts kiest, berust op eendimensionale metingen in plaats van op werkelijke 3D-grootte, en kost doorgaans meer dan 10 minuten per patiënt per beoordeling. Nu het aantal kankergevallen wereldwijd toeneemt, leggen deze beperkingen echte druk op radiologieafdelingen.
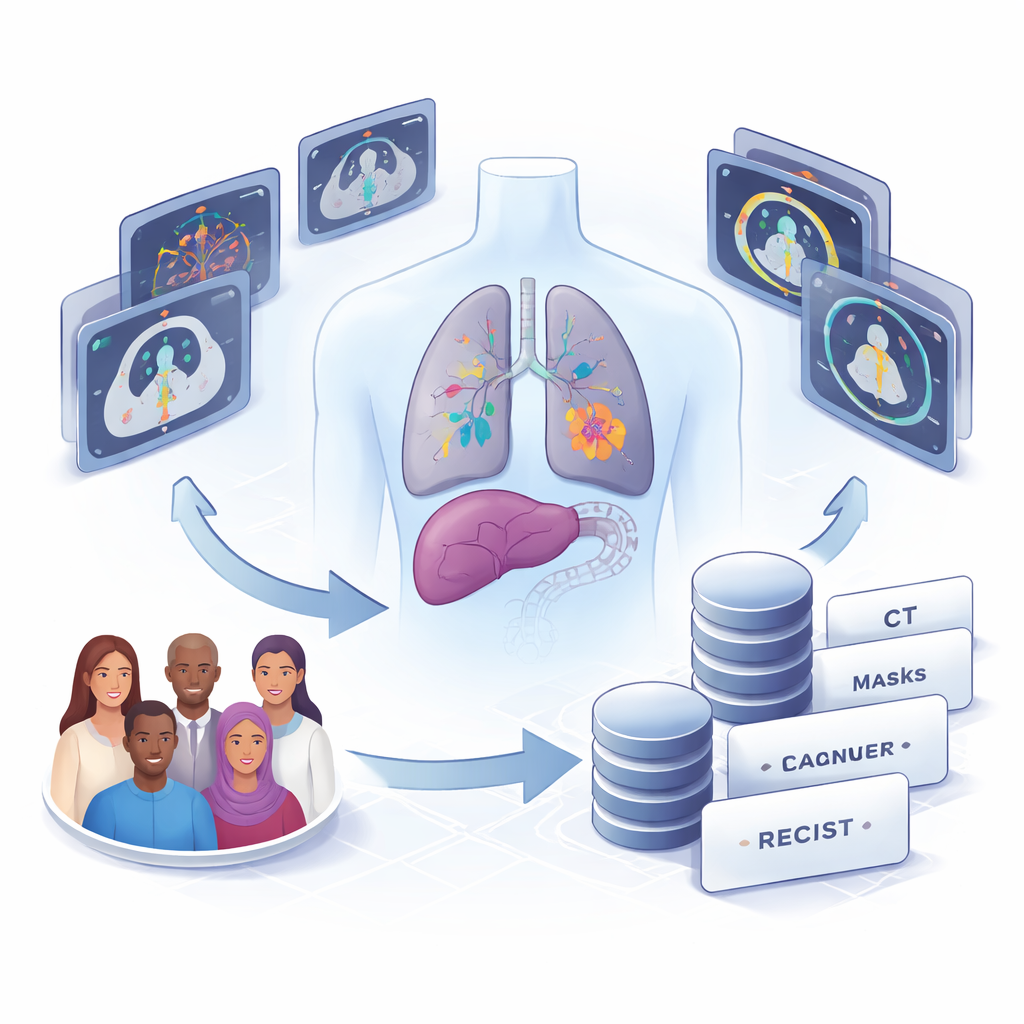
Wat de nieuwe CT-dataset bevat
De auteurs verzamelden CT-scans van 22 volwassenen die werden behandeld voor verschillende vormen van kanker in het Klinisch Ziekenhuis van de Universiteit van Chili, waaronder long-, lever-, colorectale, borst-, eierstok-, maag-, galblaas-, blaaskanker en melanoom. Uit 58 thoracale en abdominale scanseries gemaakt tussen 2017 en 2023 identificeerden zij elke solide tumor of vergrote lymfeklier die groot genoeg was om te meten. In totaal hebben ze handmatig 1.246 individuele laesies omlijnd: 1.148 metastasen (uitgezaaide tumoren), 93 vergrote lymfeklieren en 5 primaire tumoren. Voor 82 van deze laesies zijn ook de officiële RECIST-metingen uit klinische rapporten opgenomen, waardoor een directe vergelijking mogelijk is tussen routinematige praktijk en geautomatiseerde methoden.
Hoe experts en AI samenwerkten
Het produceren van zulke gedetailleerde omlijningen zou normaal gesproken onwerkbaar traag zijn, dus het team gebruikte een “human‑in‑the‑loop”-strategie. Ervaren radiologen en artsen in opleiding tekenden ruwe 3D-vakken rond verdachte tumoren, en een krachtig segmentatiemodel genaamd MedSAM stelde beginranden voor. Artsen in opleiding corrigeerden vervolgens deze randen, en senior radiologen voerden een definitieve controle uit. Na elke batch scans werd het AI-model opnieuw getraind op de verbeterde omlijningen en ingezet om te assisteren bij de volgende batch. Met elke cyclus kroop de prestatie dichter naar wat menselijke experts zouden accepteren, waardoor de benodigde inspanning voor verdere correcties afnam terwijl de nauwkeurigheid behouden bleef.
Wat de gegevens over tumoren laten zien
Aangezien elke laesie in de scans driedimensionaal was omlijnd, konden de auteurs hun omvang en dichtheid in detail bestuderen. De meeste tumoren zaten in de longen en de lever. Longtumoren waren doorgaans klein in volume maar hadden vaak relatief lange diameters, terwijl lymfeklieren grotere volumes maar iets kortere hoofddiameters lieten zien dan levertumoren. Het team onderzocht ook hoe licht of donker deze regio’s op CT leken, een eigenschap gerelateerd aan weefsel‑dichtheid. Longtumoren, omringd door lucht, vertoonden zeer andere intensiteitspatronen dan levertumoren en lymfeklieren, wat suggereert dat eenvoudige numerieke kenmerken uit CT-beelden kunnen helpen onderscheid te maken tussen soorten laesies. Belangrijk is dat de studie een sterke relatie bevestigde tussen de langste diameter van een laesie en het werkelijke 3D-volume, wat het idee ondersteunt dat diameter‑gebaseerde regels zoals RECIST als een praktisch alternatief voor volledige volumetrische metingen kunnen dienen wanneer ze zorgvuldig worden toegepast.
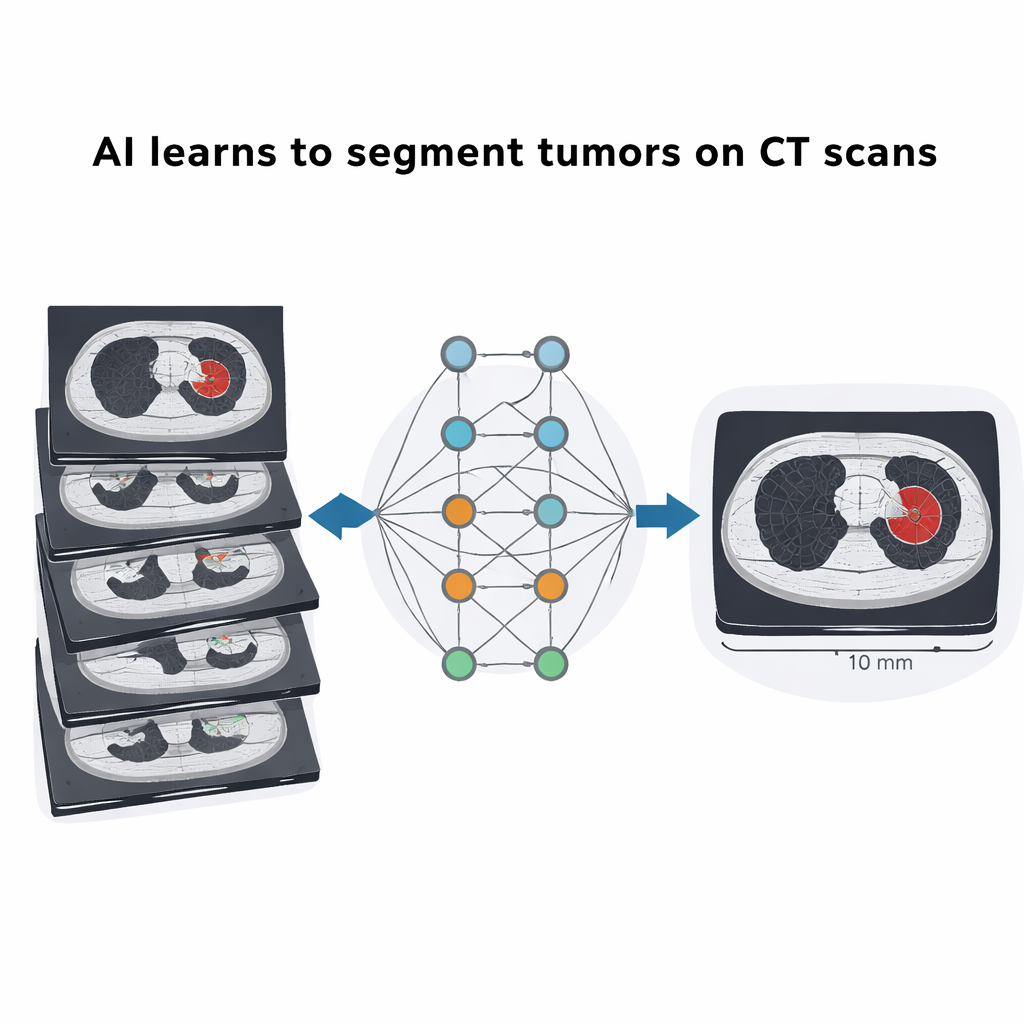
De dataset testen met deep learning
Om te laten zien hoe de dataset gebruikt kan worden, trainden en verfijnden de onderzoekers twee soorten deep learning-systemen. Ten eerste fine‑tunden ze MedSAM om tumoren automatisch te segmenteren vanaf eenvoudige begrenzingsboxen, en behaalden overlap-scores met expertsomlijningen die in dezelfde orde van grootte lagen als scores gemeld op veel grotere internationale datasets. Ten tweede pasten ze een veelgebruikt framework genaamd nnUNet aan, vertrekkend van modellen getraind op wereldwijde long- en leverbeeldvorming‑uitdagingen en deze vervolgens fijn afstemmend op deze nieuwe Chileense data. Na fine‑tuning evenaarden of overtroffen de systemen hun oorspronkelijke prestaties, met name voor longtumoren, ondanks dat de patiëntengroep relatief klein was. Dit toont aan dat zorgvuldig samengestelde lokale data de betrouwbaarheid van AI-hulpmiddelen in een specifiek ziekenhuis aanzienlijk kunnen verbeteren.
Wat dit betekent voor toekomstige kankerzorg
Voor niet‑specialisten is de kernboodschap dat deze dataset een instrument is dat mogelijkheden biedt, geen diagnostisch product op zichzelf. Door CT-scans openlijk te delen waarin elke zichtbare tumor en lymfeklier is omlijnd en in veel gevallen nauwkeurig gemeten, bieden de auteurs een realistische oefenplaats voor algoritmen die tumormonitoring willen automatiseren. Dergelijke hulpmiddelen kunnen radiologen helpen minder tijd te besteden aan handmatige metingen en meer aan complexe beoordelingen, terwijl ook de variatie tussen beoordelaars afneemt. Omdat de data uit een Latijns-Amerikaans ziekenhuis komen en onder een permissieve licentie worden vrijgegeven, helpen ze er bovendien voor te zorgen dat toekomstige medische AI op diversere patiënten wordt getest, wat de kans vergroot dat geautomatiseerde kankermonitoring betrouwbaar werkt voor mensen wereldwijd.
Bronvermelding: Rojas-Pizarro, R., Vásquez-Venegas, C., Pereira, G. et al. A CT Dataset with RECIST Measurements and Comprehensive Segmentation Masks for Tumors and Lymph Nodes. Sci Data 13, 270 (2026). https://doi.org/10.1038/s41597-026-06597-6
Trefwoorden: kankerbeeldvorming, CT-scans, tumorsegmentatie, RECIST, medische AI-datasets