Clear Sky Science · nl
BreastDCEDL: Een gestandaardiseerde, deep learning-klaar borst DCE-MRI-dataset van 2.070 patiënten
Waarom dit van belang is voor borstkankerzorg
Wanneer iemand de diagnose borstkanker krijgt, moeten artsen snel beslissen welke behandelingen waarschijnlijk het beste werken. Krachtige MRI-scans kunnen laten zien hoe een tumor zich gedraagt, maar van die scans betrouwbare, computergestuurde hulpmiddelen maken om de behandeling te sturen is moeilijk geweest. Dit artikel introduceert BreastDCEDL, een grote, zorgvuldig voorbereide verzameling borstdce-MRI-scans die speciaal is ontworpen om onderzoekers te helpen kunstmatige intelligentie (AI)-systemen te bouwen en te testen die voorspellen hoe tumoren op therapie zullen reageren.
Tumoren in de tijd volgen
Artsen gebruiken vaak een speciaal soort MRI, dynamische contrastversterkte MRI (DCE-MRI), om borsttumoren te bekijken. Bij deze scan worden beelden gemaakt voor en na injectie van een contrastvloeistof, waarmee wordt vastgelegd hoe bloed in de tumor door enkele minuten heen stroomt. Kankweefsel heeft vaak lekkende, rommelige bloedvaten, waardoor het anders oplicht en vervaagt dan gezond weefsel. Deze time-lapsebeelden kunnen laten zien hoe agressief een tumor is en kunnen helpen voorspellen of deze volledig zal verdwijnen na krachtige geneesmiddelen zoals chemotherapie.
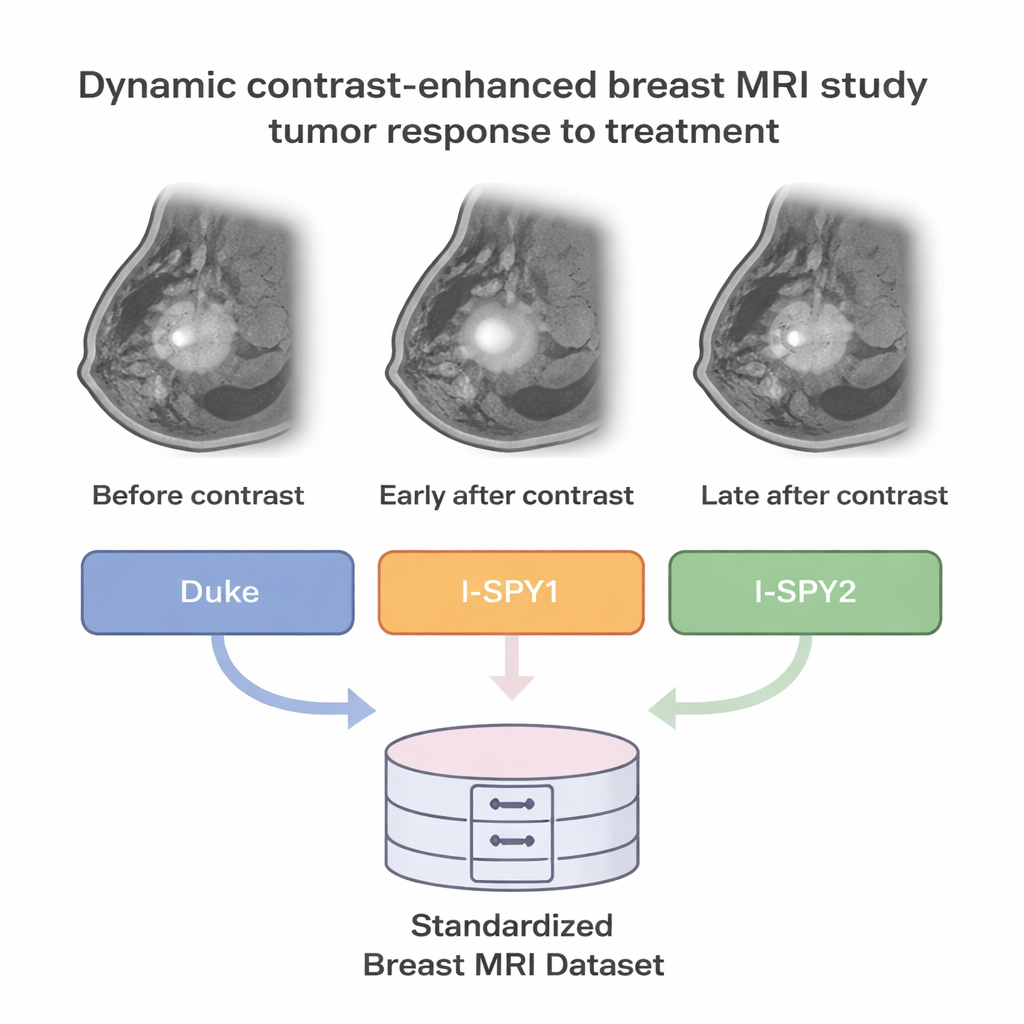
Versnipperde scans omzetten in één duidelijke bron
Tot nu toe werd vooruitgang in AI voor borst-MRI vertraagd door versnipperde data: verschillende ziekenhuizen slaan beelden in verschillende formaten op, gebruiken verschillende scanners en leggen klinische gegevens op uiteenlopende manieren vast. Het BreastDCEDL-project pakte dit probleem aan door pretreatment DCE-MRI-scans van 2.070 patiënten samen te brengen uit drie grote onderzoeksgroepen, bekend als I-SPY1, I-SPY2 en Duke. Het team zette meer dan 8,5 miljoen individuele beeldsneden om in iets meer dan elfduizend 3D-volumes met behulp van een standaardformaat dat veel wordt gebruikt in medisch beeldvormingsonderzoek. Ze sorteerden beelden zorgvuldig in de tijd (voor contrast, vroeg na en later na) en in de ruimte, zodat de scans van elke patiënt correct op elkaar aansluiten.
De tumoren markeren en de feiten koppelen
Om AI te laten leren, moet het weten waar de tumor zit en wat er met de patiënt gebeurde. In BreastDCEDL heeft elke patiënt tumormarkeringen en belangrijke klinische informatie. Voor de I‑SPY-groepen werden complexe computercodes die tumoromtrekken beschrijven omgezet in eenvoudige 3D-masks die tumorgebieden voxel voor voxel markeren. Voor de Duke-groep tekenden deskundige radiologen begrenzingsvakken rond de grootste tumor in elk geval. Naast de beelden bevat de dataset leeftijd van de patiënt, basisdemografische gegevens, tumorgrootte, hormone receptor (HR)-status, HER2-status en of de tumor volledig verdween na behandeling — een resultaat dat pathologisch compleet respons of pCR wordt genoemd. Deze uitkomst, beschikbaar voor 1.452 patiënten, hangt nauw samen met lange-termijn overleving en is een belangrijk doel voor voorspellende modellen.
Eerlijke testopzetten voor AI-hulpmiddelen
Om het vergelijken van nieuwe AI-methoden eenvoudig te maken, leveren de auteurs vaste trainings-, validatie- en testgroepen, met vergelijkbare pCR-percentages daartussen. Dat betekent dat verschillende onderzoeksteams hun modellen op exact dezelfde patiëntengroepen kunnen testen, wat prestatieclaims betrouwbaarder maakt. De dataset behoudt ook de natuurlijke variatie die in echte ziekenhuizen voorkomt: scans komen van veel centra, verschillende MRI-machines en licht verschillende manieren om HR- en HER2-positiviteit te definiëren. In plaats van deze verschillen weg te poetsen, legt BreastDCEDL ze duidelijk vast, zodat onderzoekers zelf kunnen beslissen hoe ze ermee omgaan en kunnen testen of hun modellen nog steeds werken over gevarieerde patiëntpopulaties en scancondities heen.
Wat dit vrijmaakt voor toekomstig onderzoek
BreastDCEDL is meer dan een stapel beelden; het is een goed georganiseerd gereedschapssysteem voor veel soorten studies. Onderzoekers kunnen AI-systemen trainen om tumoren te lokaliseren, tumervolume te meten, pCR te voorspellen voordat de behandeling begint en te onderzoeken hoe beeldpatronen samenhangen met tumorbiologie. Patiënten zonder uitkomstgegevens helpen nog steeds door extra voorbeelden te bieden voor unsupervised en semi-supervised leren. Omdat alle bestanden een eenvoudig naamgevingssysteem en gemeenschappelijk formaat volgen, kunnen wetenschappers ze snel laden en analyseren met standaardsoftware, wat dagen van handmatige voorbereiding bespaart en de kans op fouten verkleint.
Een duidelijker pad naar gepersonaliseerde behandeling
In eenvoudige bewoordingen zet dit werk een rommelige verzameling borst-MRI-scans uit meerdere ziekenhuizen om in een schone, gedeelde basis voor AI-onderzoek. Door te standaardiseren hoe beelden en klinische informatie worden opgeslagen en door tumoren en uitkomsten consistent te markeren, geeft BreastDCEDL onderzoekers wat ze nodig hebben om computerhulpmiddelen te bouwen en eerlijk te testen die artsen op den duur kunnen helpen de juiste behandeling voor elke patiënt te kiezen. Hoewel het op zichzelf geen kanker geneest, verwijdert het een belangrijke hindernis op weg naar meer precieze, datagedreven borstkankerzorg.
Bronvermelding: Fridman, N., Solway, B., Fridman, T. et al. BreastDCEDL: A standardized deep learning-ready breast DCE-MRI dataset of 2,070 patients. Sci Data 13, 264 (2026). https://doi.org/10.1038/s41597-026-06589-6
Trefwoorden: borst MRI, kankerbeeldvorming, medische AI, behandelingsrespons, medische datasets