Clear Sky Science · nl
Vitamine B2-metabolisme bevordert FSP1-stabiliteit om ferroptose te voorkomen
Hoe een alledaagse vitamine cellen helpt kiezen tussen leven en dood
Onze cellen balanceren voortdurend tussen overleven en zelfvernietiging. Een spectaculaire vorm van celdood, ferroptose genoemd, trok aandacht omdat ze selectief kankercellen kan doden die resistent zijn tegen andere behandelingen. Deze studie toont aan dat een gewone voedingsstof — vitamine B2, of riboflavine — stilletjes het evenwicht verplaatst door een cruciaal beschermend eiwit te stabiliseren. Het begrijpen van deze verborgen verbinding tussen voeding, celmetabolisme en kankerceldood kan onderzoekers helpen slimmere therapieën te ontwerpen en toekomstige voedingsadviezen te verfijnen.
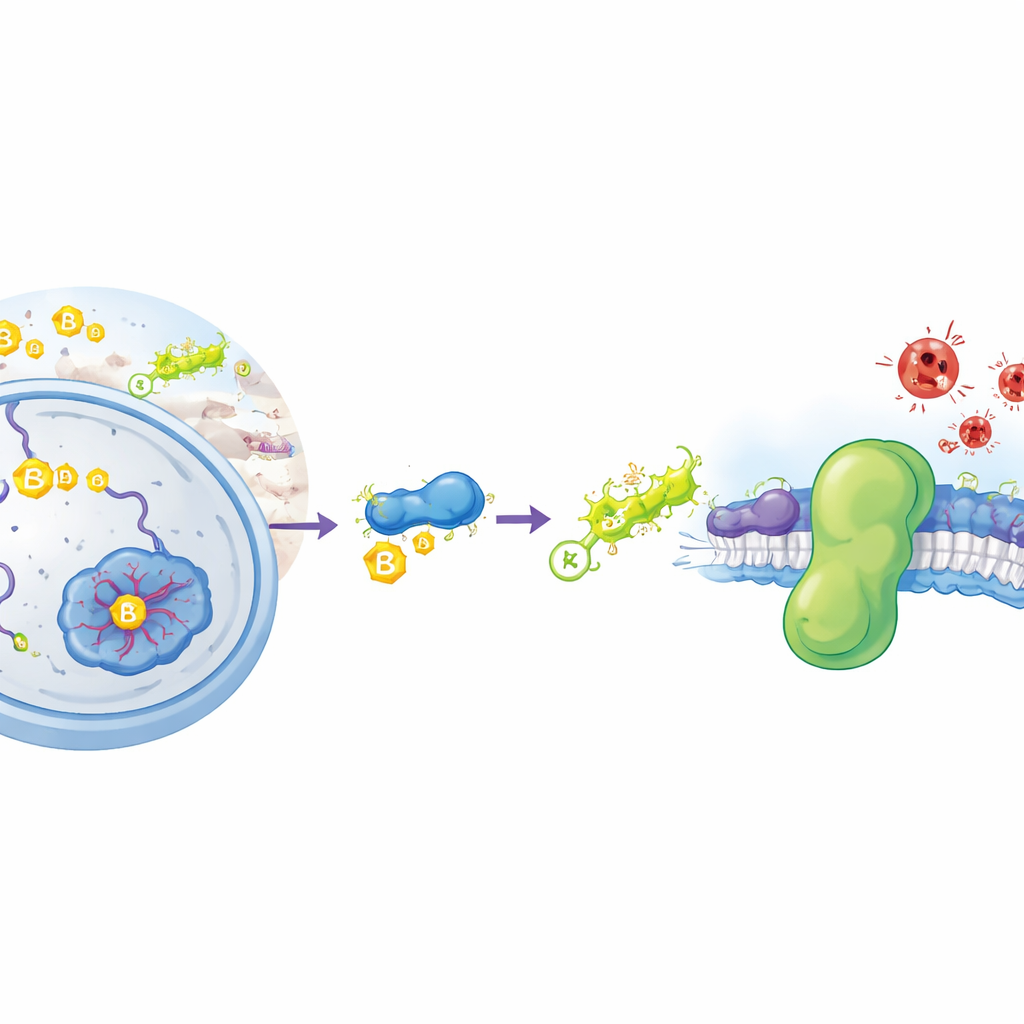
Een bijzondere soort roest binnenin cellen
Ferroptose is een vorm van celdood die wordt aangedreven door een chemisch proces dat doet denken aan het roesten van metaal: de ongecontroleerde oxidatie van vetten in celmembranen. Wanneer deze vetten afbreken, verliezen membranen hun integriteit en barsten cellen. Onze cellen zetten normaal gesproken verschillende verdedigingslinies in om dit te voorkomen. Een belangrijke verdedigingslinie is het enzym GPX4, dat met behulp van het kleine molecuul glutathion schadelijke lipideperoxiden afbreekt. Een tweede, parallelle verdedigingslinie is een eiwit genaamd FSP1, dat op celmembranen zit en gebruikmaakt van kleine vetachtige moleculen om destructieve radicalen te onderscheppen voordat ze zich verspreiden. Kankercellen zetten vaak FSP1 hoger aan om ferroptose te vermijden, waardoor dit eiwit een aantrekkelijk doelwit is voor nieuwe kankertherapieën. Tot nu toe wisten wetenschappers echter niet hoe cellen reguleren hoeveel FSP1 wordt geproduceerd en hoe lang het overleeft.
Een cellulair “brandstofmeter” bouwen voor een doodsblokker
Om de verborgen beheerders van FSP1 te vinden, brachten de onderzoekers eerst menselijke botkankercellen zodanig in kaart dat ze een fluorescerende reporter droegen. Ze labelden het natuurlijke FSP1-eiwit met een groen signaal en koppelden dat aan een blauw signaal dat rapporteert hoeveel FSP1-boodschap de cel maakt. Dit slimme ontwerp liet hen veranderingen in genactiviteit (blauw) onderscheiden van veranderingen in eiwitstabiliteit (groen). Met dit tweekleurensysteem gebruikten ze CRISPR–Cas9 om systematisch bijna elk gen in het genoom te verstoren en sorteerden vervolgens cellen met hoge of lage FSP1-niveaus. Door te vergelijken welke gids-RNA’s in elke groep verrijkt waren, brachten ze honderden genen in kaart die FSP1 zowel kunnen versterken als verminderen, werkend op het niveau van gencontrole of eiwitomzetting.
De verborgen taak van vitamine B2: een stabiliserend handvat maken
Onder de meest opvallende vondsten waren twee enzymen, riboflavinekinase (RFK) en FAD-synthase (FLAD1), die vitamine B2 omzetten in een cofactor genaamd FAD. FSP1 is een flavoproteïne dat normaal gesproken FAD stevig bindt om zijn chemische reacties uit te voeren. Wanneer RFK of FLAD1 werden verwijderd, of wanneer cellen werden gekweekt in medium met te weinig vitamine B2, daalden de FSP1-eiwitniveaus scherp terwijl de genactiviteit vergelijkbaar bleef. Het team toonde aan dat dit verlies cellen veel gevoeliger maakte voor ferroptose wanneer GPX4 werd geblokkeerd. Belangrijk is dat vitamine B2 zelf niet als klassieke antioxidant fungeerde: in een gevoelige proefbuisassay stopte het de lipideoxidatie niet, in tegenstelling tot vitamine E. In plaats daarvan herstelde het toevoegen van FAD (en gedeeltelijk de voorloper FMN) aan deficiënte cellen zowel FSP1-niveaus als de weerstand tegen ferroptotische celdood, terwijl extra vitamine B2 alleen niet hielp als de verwerkende enzymen ontbraken.
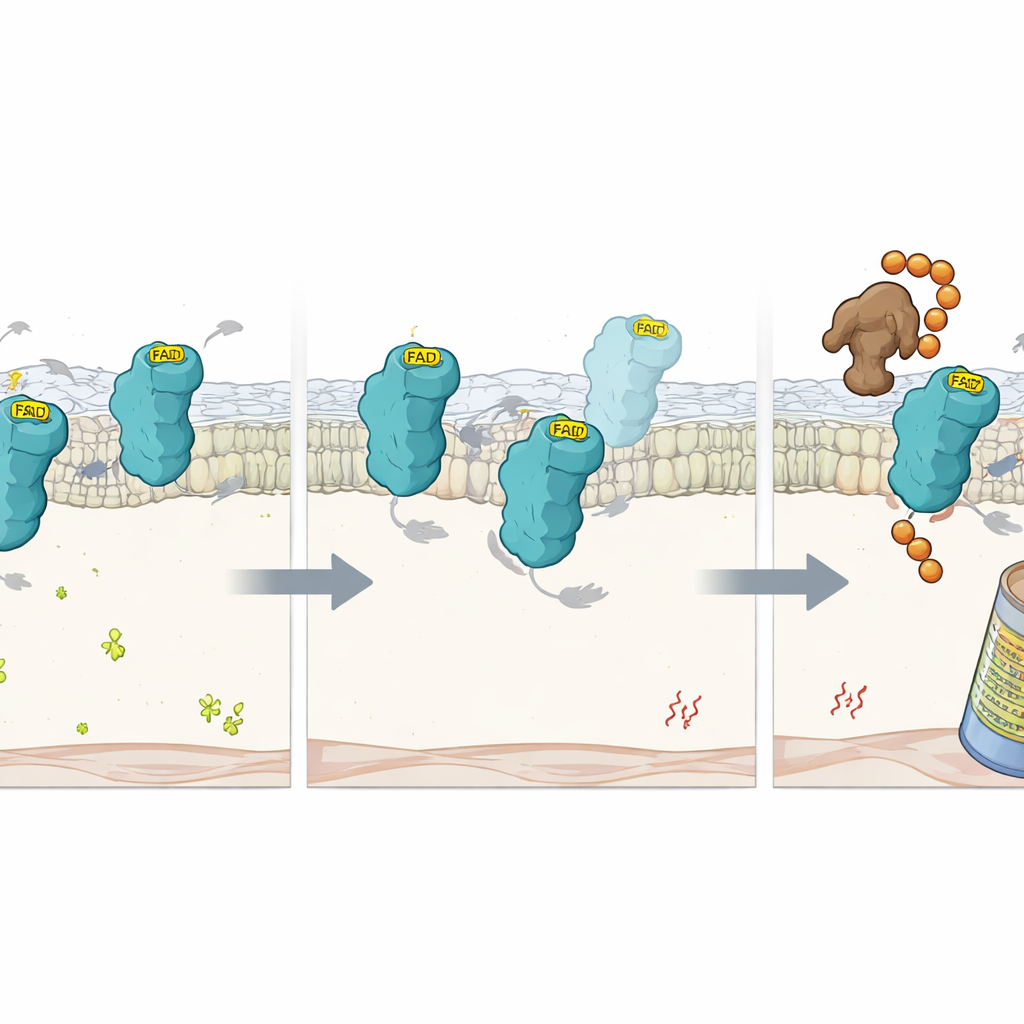
Wat er gebeurt wanneer de cofactor ontbreekt
Om dieper te kijken bestudeerden de wetenschappers precieze mutaties in FSP1 die het vermogen om FAD vast te houden ondermijnen. Deze gemuteerde eiwitten vouwden nog grotendeels normaal, maar verloren hun FAD en katalytische activiteit. In cellen verdwenen ze veel sneller dan normaal FSP1, tenzij het proteasoom — de eiwitverslindende machinerie van de cel — werd geblokkeerd. Dit suggereerde dat FAD-binding zelf fungeert als een stabiliserend handvat dat FSP1 beschermt tegen het labelen als defect. Met een andere gerichte CRISPR-screen onder omstandigheden van lage FAD identificeerde het team een E3-ligase genaamd RNF8 als een sleutelfactor die FAD-vrij FSP1 herkent. Wanneer RFK werd verwijderd, voegde RNF8 ketens van ubiquitinetags toe aan het lege eiwit, waardoor het werd gericht op afbraak door het proteasoom. Het verwijderen van RNF8 vertraagde de FSP1-omzetting in FAD-arme cellen, hoewel het de verloren beschermende functie zonder de cofactor niet kon herstellen.
Van moleculaire schakelingen naar ideeën voor kankertherapieën
Door deze onderdelen te combineren stellen de auteurs een eenvoudig maar krachtig model voor. Vitamine B2, na omzetting in FAD door RFK en FLAD1, bindt aan FSP1 en is essentieel voor zowel diens biochemische activiteit als zijn levensduur. Wanneer de vitamine B2-voorziening of de verwerking tekortschiet, kan nieuwgemaakt FSP1 geen FAD bemachtigen, wordt het door RNF8 gemarkeerd en snel afgebroken door het proteasoom, waardoor cellen kwetsbaarder worden voor ferroptotische schade. Gegevens uit kankerstudies suggereren dat tumoren met hogere RFK-expressie meer resistent zijn tegen ferroptose-inducerende middelen, wat de relevantie van deze route in de praktijk benadrukt. Voor niet-specialisten is de kernboodschap dat een vertrouwde vitamine veel meer doet dan als simpele antioxidant optreden: zij helpt bepalen of een krachtig anti-doods-eiwit paraat blijft of wordt weggevaagd. Door het metabolisme van vitamine B2 of de stabiliteit van FSP1 bij te stellen, zouden toekomstige behandelingen ferroptose beter kunnen benutten om kankercellen te elimineren en tegelijkertijd gezond weefsel te sparen.
Bronvermelding: Deol, K.K., Harris, C.A., Tomlinson, S.J. et al. Vitamin B2 metabolism promotes FSP1 stability to prevent ferroptosis. Nat Struct Mol Biol 33, 525–536 (2026). https://doi.org/10.1038/s41594-026-01759-x
Trefwoorden: ferroptose, vitamine B2, FSP1, kankercelsterfte, celmetabolisme