Clear Sky Science · nl
Kaart van transposonelement–genchimera’s: oorsprong en rol bij het vergroten van transcriptomeplasticiteit
Verborgen passagiers in ons DNA
Een groot deel van ons DNA bestaat uit oude virale ‘meereizigers’ die transposable elementen worden genoemd — stukjes genetische code die vroeger als parasieten door genomen sprongen. Deze studie laat zien dat die oude virale fragmenten niet gewoon stilstaand vuilnis zijn: ze kunnen zich in onze eigen genen invoegen om hybride boodschappen te maken, cellen helpen zich aan veranderende omstandigheden aan te passen en soms ziektes aanwakkeren. Door deze hybriden in kaart te brengen tijdens ontwikkeling, veroudering en kanker, laten de auteurs een verrassende manier zien waarop viraal DNA nog steeds de menselijke biologie vormgeeft.
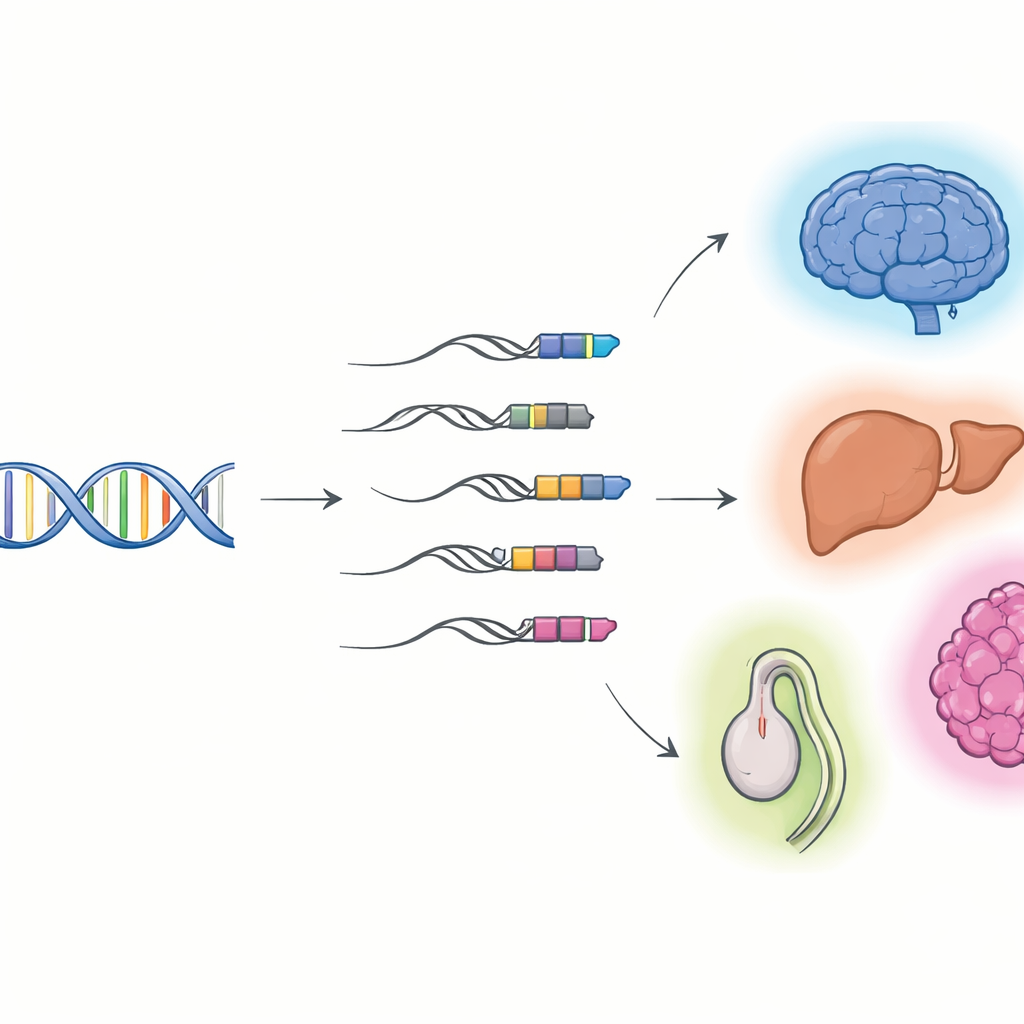
Wanneer viraal DNA deel van onze genen wordt
De onderzoekers richtten zich op “TE–genchimera’s”: RNA‑moleculen die beginnen in een transposable element en vervolgens doorlopen in een gastheer‑gen. Met long‑read sequencing, dat volledige RNA‑moleculen van begin tot eind kan vangen, gecombineerd met standaard short‑read sequencing, stelden ze gedetailleerde catalogi van deze hybriden samen in muis‑ en menselijke cellen en organen. Ze vonden duizenden eerder onbekende chimere transcripties, waarvan de meeste niet‑coderende RNA’s zijn in plaats van blauwdrukken voor eiwitten. Veel beginnen in een klasse virale resten die long terminal repeats (LTR’s) worden genoemd, die vaak vooraan genen zitten en als alternatieve aan/uit‑schakelaars kunnen werken. Verschillende weefsels en organen gebruiken uiteenlopende sets van deze chimera’s, met bijzonder veel activiteit in de hersenen, de lever en de testis, en hun gebruik verandert wanneer weefsels zich ontwikkelen van foetaal naar volwassen stadium.
Chimera’s bij veroudering en kanker
Om te onderzoeken hoe deze viraal‑gastheerhybriden zich gedragen in echte populaties, doorzochten de onderzoekers grote menselijke datasets die tientallen weefsels van honderden mensen omvatten, evenals tumor‑monsters. Ze identificeerden enkele honderden chimera’s met hoge betrouwbaarheid die bij meerdere individuen terugkeren. Hun expressie verschilt niet alleen tussen organen maar ook met leeftijd: in weefsels zoals bloed en hersenen nemen sommige LTR‑gedreven chimera’s af bij oudere volwassenen, terwijl ze in bepaalde perifere weefsels juist toenemen. In veel soorten kanker zijn deze op LTR’s gebaseerde hybriden in tumoren over het algemeen verhoogd vergeleken met nabijgelegen normaal weefsel, en patiënten van wie de tumoren er meer van tot expressie brengen, hebben vaak een slechtere prognose. In datasets van mensen die resistent zijn tegen chemotherapie of immunotherapie zitten de genen die door nieuwe LTR‑gedreven exons worden beïnvloed vaak in pathways die gekoppeld zijn aan de werking van die geneesmiddelen, wat suggereert dat TE‑chimera’s tumoren kunnen helpen zichzelf te herbedraden onder behandelingsdruk.
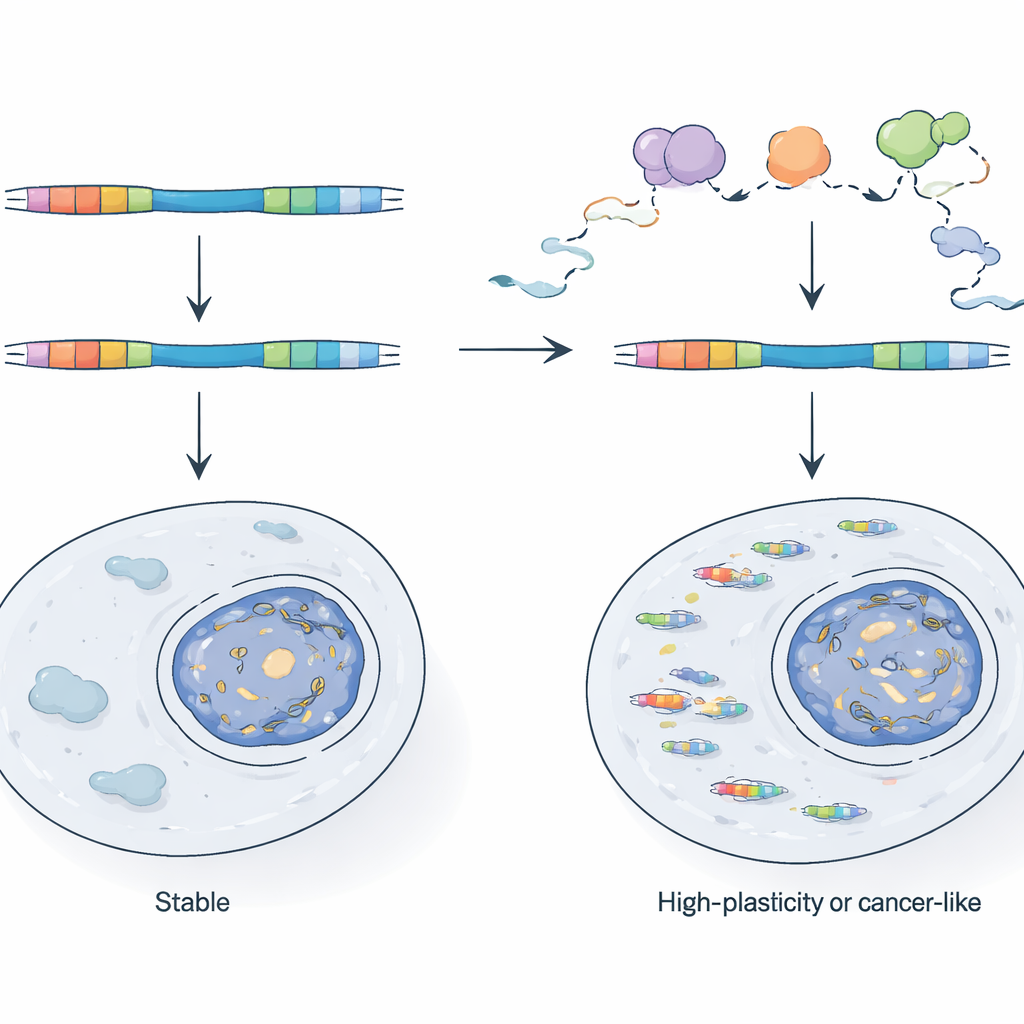
Hoe cellen virale hybriden onder controle houden
Gezien hun potentie, waarom overspoelen TE‑chimera’s normale cellen niet? De auteurs tonen aan dat cellen vertrouwen op een RNA‑kwaliteitscontrolesysteem, gecentreerd rond het nucleaire exosoomcomplex, om veel van deze transcripties tijdens hun ontstaan te patrouilleren en te vernietigen. Wanneer ze in muis‑stamcellen een essentieel exosoomcomponent genetisch verzwakken, worden LTR‑gedreven promoters veel actiever en nemen chimere RNA’s sterk toe. Door nieuwgemaakte RNA te vergelijken met stabiel RNA laten ze zien dat sommige LTR’s normaal gesproken in toom worden gehouden omdat hun transcripties snel worden afgebroken, terwijl andere gecontroleerd worden op het niveau van hoe vaak transcriptie start. Deze actieve LTR’s liggen vaak in genoomregio’s die al toegankelijk en frequent getranscribeerd zijn, wat aangeeft dat dichtbij een actief gen of antisense‑transcript zitten een viraal fragment kan helpen ontsnappen aan traditionele epigenetische stillegging.
Splicing, stamcelplaticiteit en een viraal “hoofdschakelaar”
Het verhaal wordt complexer wanneer het splicing‑apparaat van de cel verstoord is. De auteurs schakelen verschillende kernsplicingfactoren uit of remmen het spliceosoom chemisch en zien een gedeeld resultaat met verlies van het exosoom: een sterke toename van LTR‑gedreven chimera’s en van korte, intron‑arme genen. Een van de winnaars is MERVL, een endogeen retrovirus dat actief is in zeer vroege muizembrio’s. Wanneer MERVL’s interne sequentie en de daaronder liggende transcriptiefactoren worden opgevoerd, verschuiven stamcellen naar een meer ‘totipotente‑achtige’ staat, gelijkend op vroege embryonale cellen die alle weefsels kunnen vormen. Omgekeerd dempt afbraak van MERVL‑RNA met antisense oligonucleotiden deze verschuiving en vermindert de LTR‑promoteractiviteit, wat aangeeft dat MERVL fungeert als een hoofdschakelaar die een breder netwerk van TE‑chimera’s en celtoestandplaticiteit kan activeren.
Virale innovatie over de evolutie heen
Door vele zoogdiergenomen heen traceren de onderzoekers wanneer verschillende TE‑families begonnen exons aan gastheergenen te doneren. Zowel bij mensen als muizen blijken relatief jonge LTR‑families bijzonder geneigd te zijn chimera’s te vormen in de ‘sense’‑oriëntatie die als onderdeel van gastheertranscripten gelezen kan worden. Dit patroon suggereert dat nieuwe golven van TE‑inserties herhaaldelijk ruwe bouwstenen in genregulerende netwerken hebben geleverd door evolutionaire tijd. In plaats van puur schadelijk te zijn, kunnen deze inserties door het transcriptie‑ en afbraakmachinerie van de cel worden getest: de meeste worden stilgelegd of afgebroken, maar een minderheid belandt op de juiste plaats en in de juiste context om te worden geadopteerd als nuttige regulatorische elementen of nieuwe genstarters.
Waarom deze virale resten ertoe doen
Voor niet‑specialisten toont dit werk aan dat een groot en ooit afgedaan deel van ons genoom actief bepaalt hoe genen worden afgelezen, hoe cellen van identiteit veranderen en hoe ziekten voortschrijden. Oude virale sequenties kunnen worden omgezet in alternatieve gen‑‘voordeuren’, waarbij hybride RNA’s ontstaan die normaal gesproken door cellulaire opruimsystemen worden gecontroleerd. Wanneer die bewaking of het normale splicen hapert, kunnen deze hybriden oplopen, waardoor stamcellen flexibeler worden of tumoren zich aanpassen en therapieresistentie ontwikkelen. Over miljoenen jaren heeft de evolutie herhaaldelijk aan deze virale fragmenten gesleuteld, velen van parasieten tot bouwstenen van regulatorische complexiteit omgevormd — en ons een transcriptome nagelaten dat veel plastischer en dynamischer is dan een eenvoudige genenlijst zou doen vermoeden.
Bronvermelding: Cheon, Y., Alvstad, E.G., Torre, D. et al. Transposable element–gene chimera cartography, origination and role in enhancing transcriptome plasticity. Nat Struct Mol Biol 33, 448–463 (2026). https://doi.org/10.1038/s41594-026-01757-z
Trefwoorden: transposable elementen, chimere transcripties, RNA‑bewaking, platiciteit van stamcellen, kankerevolutie