Clear Sky Science · nl
Stressaanpassing van mitochondriale eiwitinvoer door OMA1-gemedieerde afbraak van DNAJC15
Hoe onze cellen omgaan als hun energiecentrales onder stress staan
Elke cel in uw lichaam is afhankelijk van kleine structuren genaamd mitochondriën om voedsel om te zetten in bruikbare energie. Als miniatuurfabrieken importeren mitochondriën voortdurend nieuwe onderdelen — eiwitten die elders in de cel zijn gemaakt — om hun machinerie draaiende te houden. Dit artikel onthult hoe cellen, wanneer mitochondriën gestrest of beschadigd zijn, deze stroom van eiwitinvoer doelbewust terugschakelen. Daarmee beschermen ze zichzelf tegen overbelasting en coördineren ze een bredere stressreactie die niet alleen mitochondriën omvat, maar ook een ander belangrijk compartiment: het endoplasmatisch reticulum.
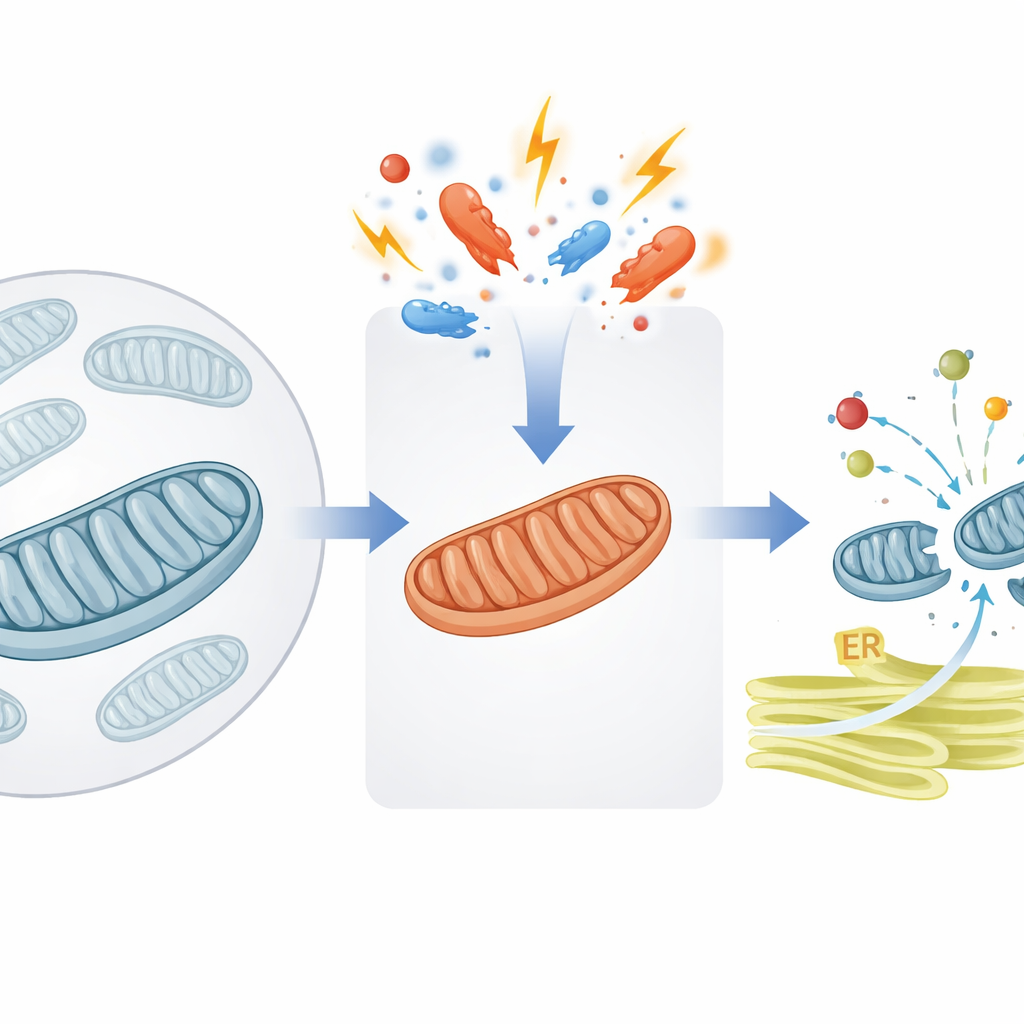
Een veiligheidsklep voor mitochondriale eiwitstromen
Mitochondriën vertrouwen op duizenden eiwitten die eerst in het hoofdcompartiment van de cel worden gemaakt en vervolgens worden aangeleverd. De auteurs richten zich op een cruciale poort in het binnenmembraan van mitochondriën, ondersteund door een hulpstof genaamd DNAJC15. Onder normale omstandigheden helpt DNAJC15 nieuwe eiwit‑'pakketten' door het importkanaal te trekken en het mitochondrion binnen te brengen, waar veel van deze eiwitten deel gaan uitmaken van de energieproducerende machinerie, bekend als oxiderende fosforylering (OXPHOS). De studie laat zien dat wanneer mitochondriën stress ervaren — zoals verminderde energieproductie of veranderingen in membraaneigenschappen — de cel een moleculaire schakelaar omzet die bepaalt hoeveel eiwitten het organel nog wil importeren.
OMA1: de stress‑geactiveerde schaar
Centraal in deze schakel staat een stressgevoelig enzym genaamd OMA1, ingebed in het binnenmembraan van mitochondriën. Wanneer mitochondriën problemen ondervinden, wordt OMA1 actief en knipt het DNAJC15 op een specifieke plaats dicht bij het begin. Deze knip produceert een kortere versie van DNAJC15 die snel wordt afgebroken door een ander mitochondriaal enzymcomplex, het m‑AAA protease. Daardoor raakt de volledige, importcompetente vorm van DNAJC15 verloren. De auteurs tonen aan dat cellen zonder DNAJC15, of waarin DNAJC15 snel wordt vernietigd na OMA1‑activatie, een verminderde capaciteit hebben om nieuwe eiwitten in mitochondriën te brengen, vooral die nodig zijn voor de bouw en het onderhoud van OXPHOS‑complexen.
Het vertragen van energieassemblage om aan mitochondriale gezondheid aan te passen
Met grootschalige eiwitmetingen en importtests vond het team dat DNAJC15 bijzonder belangrijk is voor het leveren van eiwitten aan het mitochondriale interieur die betrokken zijn bij genexpressie en de assemblage van de ademhalingsketen. Wanneer DNAJC15 ontbreekt, hopen deze eiwitten zich trager op binnen mitochondriën en neemt het vermogen van de organellen om zuurstof te verbruiken en energieproductie aan te drijven — gemeten in geïsoleerde mitochondriën — af, vooral voor complex I van de ademhalingsketen. Een ander onderdeel van het importkanaal, TIMM17A, werkt samen met DNAJC15: het verlies van beide veroorzaakt bijzonder sterke defecten in de niveaus van mitochondriale ribosomale eiwitten en OXPHOS‑componenten. Gezamenlijk suggereren deze bevindingen dat OMA1‑gemedieerde vernietiging van DNAJC15 een manier is om tijdelijk de bouw van nieuwe energiemachinerie te remmen totdat het organel hersteld is.
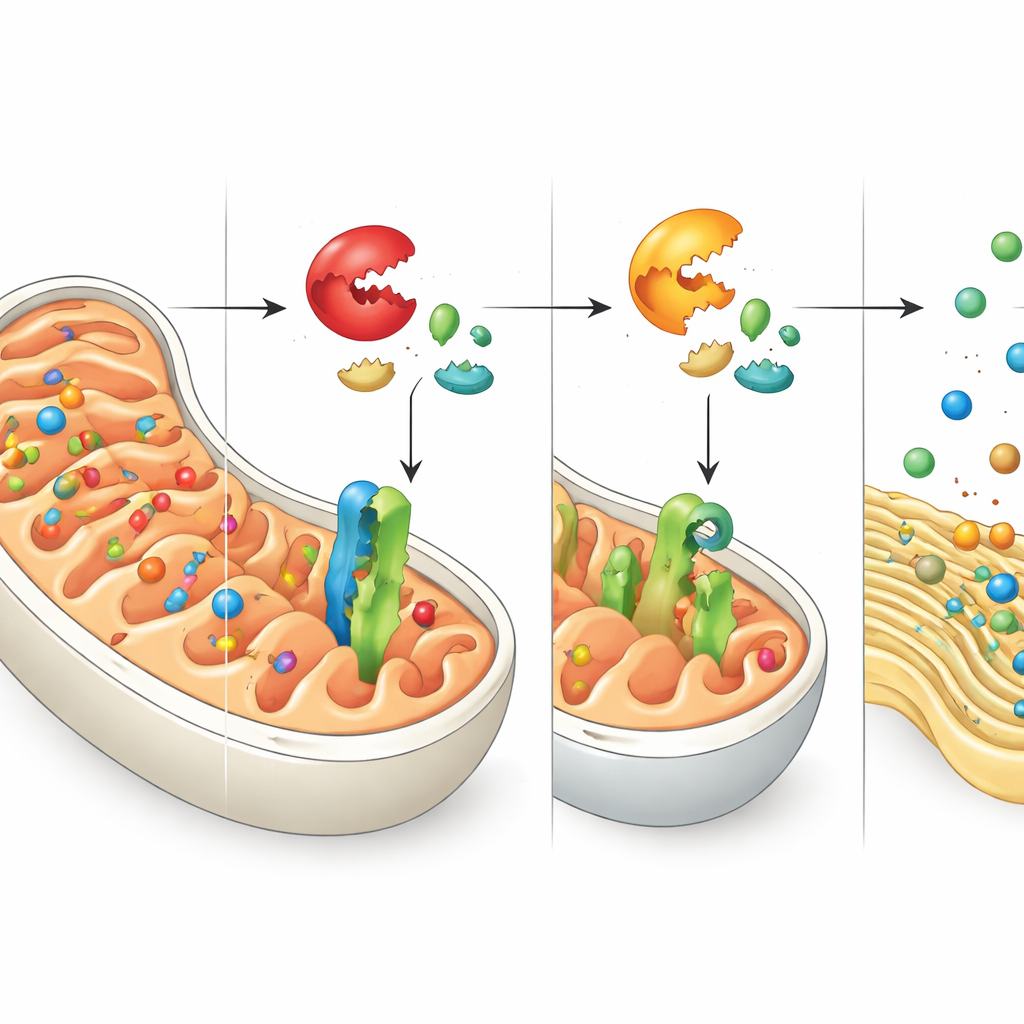
Verkeerd geleverde pakketten en een hulpoproep naar het ER
Het uitschakelen van DNAJC15 stopt de cel er niet van om mitochondriale eiwitten te maken — het verhindert vooral dat ze hun bedoelde bestemming bereiken. De auteurs onderzochten waar deze gestrande eiwitten naartoe gaan en vonden dat velen eindigen in het endoplasmatisch reticulum (ER), een netwerk van membranen dat normaal helpt bij het vouwen en verwerken van andere eiwitsets. Deze verdwaalde mitochondriale eiwitten raken ingebed in ER‑membranen en verstoren het eigen kwaliteitscontrole‑evenwicht van het ER. Als reactie activeert de cel een beschermend programma dat bekendstaat als de unfolded protein response, specifiek via een tak die wordt gecontroleerd door de sensor ATF6. Deze respons vergroot het vermogen van het ER om met misgevouwen of verkeerd geplaatste eiwitten om te gaan, en onthult daarmee een nauwe coördinatie tussen mitochondriale en ER‑stresssystemen.
Een gecoördineerde vertraging ter bescherming van de cel
Samengevat schetst de studie het beeld van een ingebouwd remsysteem voor mitochondriale biogenese. Wanneer mitochondriën onder stress staan, knipt OMA1 DNAJC15 en veroorzaakt indirect de vernietiging daarvan, waardoor de instroom van nieuwe, energiegerelateerde eiwitten in aangetaste organellen wordt verminderd. Een deel van deze eiwitten wordt tijdelijk gebufferd in het ER, dat op zijn beurt een beschermende respons opzet. Door de importcapaciteit van mitochondriën te koppelen aan de gezondheid van het organel, en door het ER in te schakelen als back‑uplocatie voor overtollige eiwitten, kunnen cellen voorkomen dat beschadigde mitochondriën worden verstopt en tijd winnen om ze te repareren of volledig te verwijderen. Voor een niet‑specialistische lezer laat dit werk zien hoe diep geïntegreerd onze cellulaire kwaliteitscontrolesystemen zijn: zelfs de kleinste misstappen in één compartiment worden waargenomen en door andere compartimenten gecompenseerd om energieproductie — en het leven zelf — op koers te houden.
Bronvermelding: Kroczek, L., Nolte, H., Lasarzewski, Y. et al. Stress adaptation of mitochondrial protein import by OMA1-mediated degradation of DNAJC15. Nat Struct Mol Biol 33, 499–511 (2026). https://doi.org/10.1038/s41594-026-01756-0
Trefwoorden: mitochondriale stress, eiwitinvoer, cellulaire kwaliteitscontrole, oxiderende fosforylering, endoplasmatisch reticulum