Clear Sky Science · nl
Structuur en mechanisme van antiphage retron Eco2
Hoe bacteriën een ingebouwde "zelfmoordknop" gebruiken om virussen te bestrijden
Virussen die bacteriën infecteren, fagen genoemd, zijn overal — van oceanen tot onze eigen darm. Deze studie onthult hoe een klein genetisch toestel in sommige bacteriën, bekend als de Eco2-retron, hen helpt een fagenaanval te overleven. Door de 3D-structuur van Eco2 en de activeringswijze te laten zien, verklaart het werk een nieuw soort noodverdediging: wanneer een infectie wordt gedetecteerd, schakelt de cel doelbewust haar eigen eiwitproductie uit om te voorkomen dat het virus zich verspreidt.
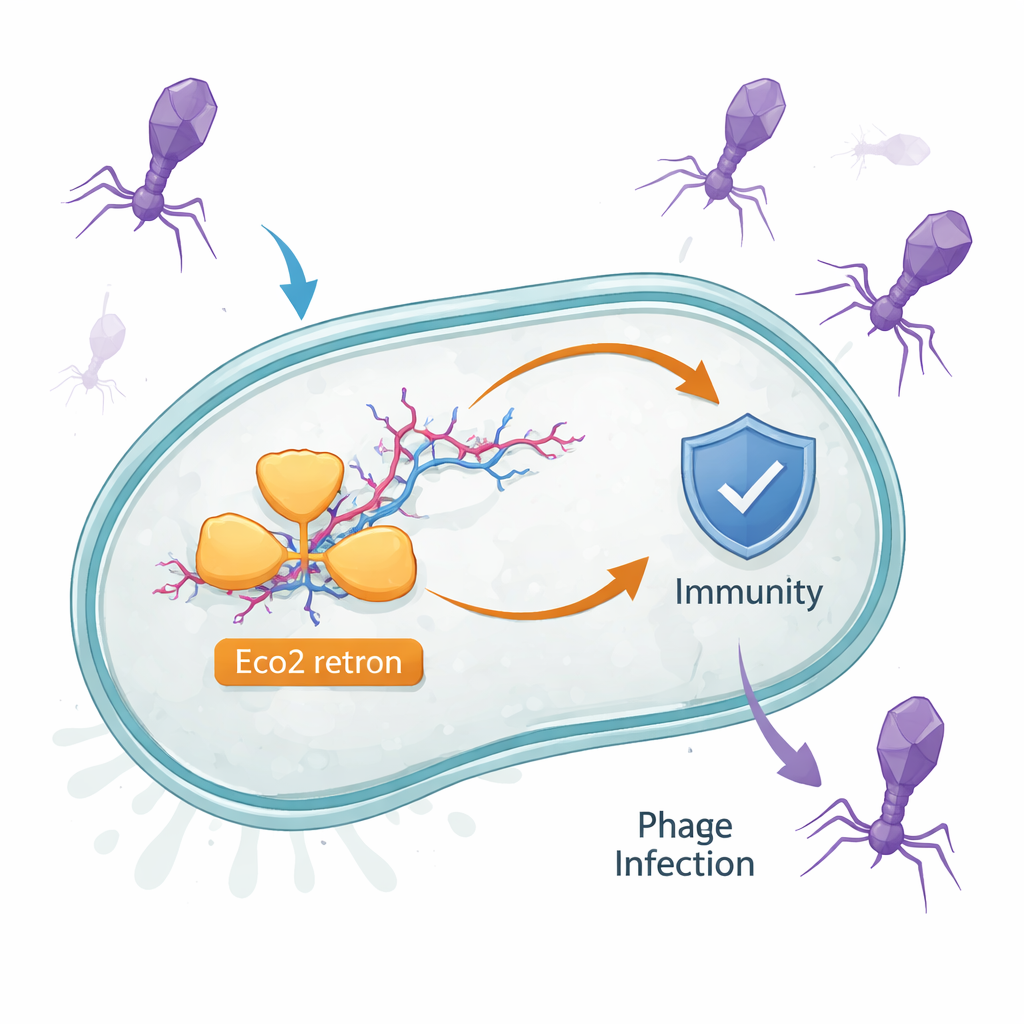
Een verborgen DNA–RNA-toestel in bacteriële cellen
Bacteriën dragen veel kleine verdedigingssystemen die alleen tijdens een infectie in actie komen. Eco2 is een van deze systemen. Het komt voor in Escherichia coli en bestaat uit één enkel eiwit dat zowel RNA naar DNA omzet als nucleïnezuren kan knippen. Dit eiwit werkt samen met een eigenaardige molecule genaamd msDNA, een hybride van RNA en enkelstrengs DNA die vertakt als een klein vorkachtig twijgje. Eerdere aanwijzingen suggereerden dat retrons zoals Eco2 tegen fagen verdedigen, maar hoe één eiwit en zijn msDNA-partner infectie waarnemen en reageren, was onduidelijk.
Brede bescherming tegen veel virussen
De onderzoekers vroegen zich eerst af hoe goed Eco2 bacteriën beschermt tegen een grote verscheidenheid aan fagen. Door cellen met Eco2 bloot te stellen aan een uitgebreide, diverse verzameling virussen ontdekten ze dat Eco2 veel fagfamilies blokkeert, maar niet allemaal. Wanneer sommige fagen wisten te ontsnappen, vertoonden hun genomen mutaties in genen die virale DNA-knippende enzymen coderen, met name een genaamd DenB. Dit patroon wees erop dat Eco2 wordt geactiveerd door specifieke virale nucleasen: wanneer die enzymen door mutatie worden uitgeschakeld, kan het virus de verdediging omzeilen.
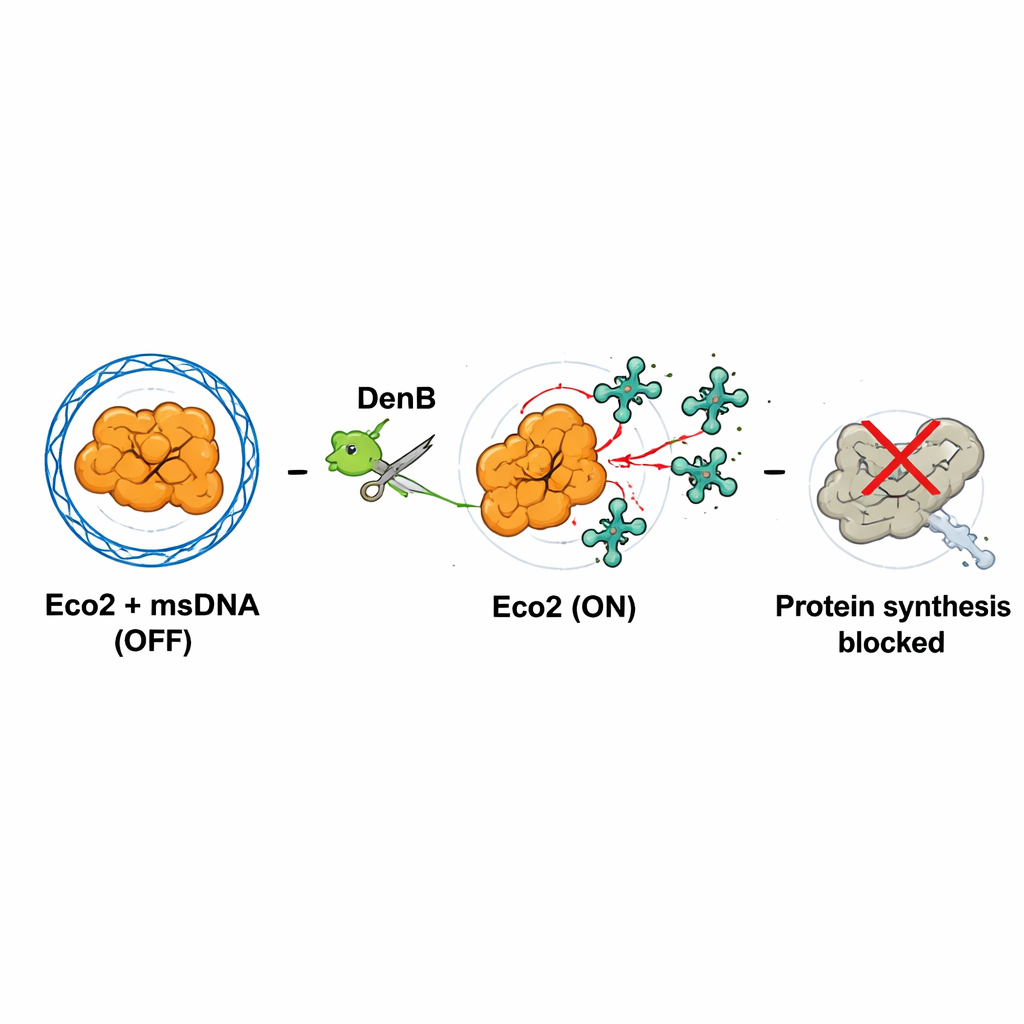
Een moleculair schild met drie armen
Om te zien hoe Eco2 is opgebouwd, gebruikte het team cryogene elektronenmicroscopie om het complex tot bijna atomaire detail te visualiseren. Eco2 werkt niet alleen: drie kopieën van het Eco2-eiwit assembleren zich tot een driearmige, shuriken-achtige structuur. Het vertakte msDNA loopt door en rond deze drie eiwitten en bindt ze aan elkaar. Daarbij vormt msDNA een driewegkruising in het centrum en "omhult" het fysiek het nuclease-deel van Eco2, waardoor de knipplaats wordt geblokkeerd. Waterstof–deuteriumuitwisselingsexperimenten, die volgen hoe flexibel verschillende regio’s zijn, toonden aan dat msDNA-binding het complex verstevigt en stabiliseert. In deze rusttoestand is Eco2 effectief vergrendeld in de UIT-positie.
Viral aanval zet het systeem aan
De sleutel tot activatie is de vernietiging van msDNA. Het virale enzym DenB, dat normaal gesproken helpt bij de verwerking van fag-DNA, knipt ook in het msDNA dat Eco2 omsluit. De auteurs imiteerden dit proces met zowel gezuiverd DenB als een standaard DNA-knipend enzym en zagen dat zodra msDNA wordt doorgesneden, de nucleasesite van Eco2 wordt blootgelegd en zich herschikt naar een actieve configuratie. Hoogwaardige structuren van deze "AAN-stand" toonden dat een kritisch aminozuur in de nuclease-pocket beweegt naar een positie waar het correct een magnesiumion kan binden, wat essentieel is voor het knippen van RNA. Zo trekt virale nuclease-activiteit, bedoeld om het gastheer-DNA te herstructureren, per ongeluk de veiligheidspen van Eco2 eruit.
De eigen tRNAs van de cel knippen om het virus te stoppen
Wat knipt geactiveerd Eco2? Met behulp van celvrije systemen, radioactieve etikettering en RNA-sequencing tijdens echte infecties, ontdekte het team dat Eco2 voornamelijk transfer-RNA’s (tRNA’s) insnijdt, de adaptermoleculen die aminozuren aan de ribosomen aanleveren. Eco2 knipt deze tRNA’s dicht bij hun staartuiteinden, vooral op plaatsen rijk aan de base cytosine. Wanneer veel tRNA’s beschadigd zijn, kunnen de ribosomen van de cel geen eiwitten meer efficiënt maken. In aanwezigheid van DenB en actief Eco2 daalde de productie van groen fluorescent eiwit scherp, en zowel bacteriële als fage-RNA’s werden afgebroken. Deze stopzetting vertegenwoordigt waarschijnlijk een "abortive infection": de geïnfecteerde bacteriële cel offert haar eigen groei op zodat het virus zich niet succesvol kan repliceren en verspreiden.
Waarom dit verder belangrijk is dan alleen voor bacteriën
Dit werk laat zien hoe een minimale retron een viraal enzym kan waarnemen, kan omschakelen van een inactieve naar een actieve vorm, en vervolgens de eiwitsynthese kan lamleggen door tRNA’s te richten. Voor niet-specialisten is het kernidee dat bacteriën virussen soms verslaan niet door precieze targeting, maar door op het juiste moment de stekker uit hun eigen cellulaire machinerie te trekken. Naast het verdiepen van ons begrip van microbiële immuniteit bieden de gedetailleerde structuren van Eco2 en zijn msDNA-skelet een blauwdruk voor ingenieurs die retrons willen herbestemmen als hulpmiddelen voor genombewerking en synthetische biologie.
Bronvermelding: Jasnauskaitė, M., Juozapaitis, J., Liegutė, T. et al. Structure and mechanism of antiphage retron Eco2. Nat Struct Mol Biol 33, 330–340 (2026). https://doi.org/10.1038/s41594-026-01754-2
Trefwoorden: immuniteit tegen bacteriofagen, retron Eco2, bacteriële antivirale verdediging, tRNA-splitsing, msDNA