Clear Sky Science · nl
Structuur en functie van het aminozuur-detecterende SEAC–EGOC-supercomplex in gist
Hoe cellen beslissen wanneer ze moeten groeien
Elke cel moet voortdurend beslissen of ze het zich kan veroorloven om te groeien of dat ze hulpbronnen moet sparen. Die beslissing hangt sterk af van aminozuren, de bouwstenen van eiwitten en een belangrijke bron van stikstof. Dit artikel onthult, met opmerkelijke structurele details, hoe gistcellen de beschikbaarheid van aminozuren waarnemen via een gigantische moleculaire assemblage en die informatie gebruiken om een belangrijke groeiregulator, TORC1, aan of uit te schakelen. Omdat hetzelfde circuit bewaard is gebleven in menselijke cellen en verband houdt met kanker en stofwisseling, bieden inzichten uit gist een venster op hoe onze eigen cellen beoordelen wanneer de omstandigheden geschikt zijn voor groei.
Een ingewikkeld knooppunt op het recyclecentrum van de cel
In gist bevindt zich een centraal beslissingscomplex, SEAC, op het membraan van de vacuole, een organel dat fungeert als het recyclecentrum van de cel. Daar ontmoet het een ander complex, EGOC, dat informatie over aminozuurniveaus doorgeeft. Gezamenlijk sturen ze signalen naar TORC1, de belangrijkste groeischakelaar. SEAC heeft twee functionele helften: SEACIT, dat TORC1 kan uitschakelen, en SEACAT, waarvan lange tijd gedacht werd dat het SEACIT in toom houdt. De auteurs gebruikten hoogresolutie kryo-elektronenmicroscopie om het volledige SEAC gebonden aan EGOC te visualiseren, waarmee ze een momentopname vastlegden van dit moleculaire knooppunt precies waar signalering plaatsvindt, op het oppervlak van de vacuole. 
De moleculaire architectuur van dichtbij bekijken
De structuur toont SEAC als een grote kern opgebouwd uit SEACAT-subunits, waaruit twee flexibele "vleugels" van SEACIT uitsteken. Elke vleugel kan één EGOC-complex binden, wat betekent dat één SEAC twee signaalinputs tegelijk kan verwerken. Opmerkelijk is dat EGOC alleen aan de vleugels vasthecht en niet aan de kern, en dat de algemene vorm van SEAC nauwelijks verandert wanneer EGOC aanwezig is. Dit toont aan dat SEACAT het actieve centrum van SEACIT niet fysiek blokkeert en EGOC niet verhindert om te binden. De oriëntatie van het complex op het vacuolemembraan positioneert ook de SEAC-kern naar het cytoplasma, waar het kan interageren met aanvullende regulatoren, terwijl de vleugels dicht bij het membraan liggen en ideaal geplaatst zijn om EGOC en andere membraangebonden partners te bereiken.
Hoe SEAC het juiste signaal kiest
De auteurs zoomden in op de contacten tussen SEAC en EGOC en ontdekten dat SEAC alleen de "actieve" versie van EGOC herkent, waarin een van zijn kleine GTPase-eiwitten, Gtr1, een GTP-achtig nucleotide draagt, terwijl zijn partner Gtr2 GDP gebonden heeft. SEACIT levert een katalytische "vinger" die reikt in de nucleotidenbinding van Gtr1 en de afbraak van GTP versnelt, waardoor EGOC van actief naar inactief schakelt. Gedetailleerde kryo-EM-kaarten en mutatie-experimenten tonen aan dat deze katalytische vinger en een aangrenzend hulpresidu essentieel zijn voor de interactie en voor het correct aflezen van de nucleotidetoestand. Toen de auteurs deze sleutelresiduen wijzigden, lokaliseerde SEAC niet langer correct naar de vacuole en kon EGOC niet productief binden.
Snel versus langzaam regelen van de groeischakelaar
Om te begrijpen wat dit betekent voor de levende cel volgden de onderzoekers de activiteit van TORC1 in de tijd toen aminozuren werden verwijderd en vervolgens opnieuw werden toegevoegd. In normale cellen schakelt TORC1 binnen enkele minuten uit bij stikstofschaarste en schakelt het snel weer in wanneer aminozuren terugkeren. Wanneer de katalytische vinger in SEACIT was uitgeschakeld, of SEACIT-subunits verwijderd, reageerde TORC1 nauwelijks in dit vroege tijdsvenster. Hetzelfde gold toen zowel Gtr1 als Gtr2 werden verwijderd, wat laat zien dat het SEAC–EGOC-paar de dominante, snelle route is voor aminozuurregeling van TORC1. Echter, op latere tijdstippen—ongeveer een halfuur—paste TORC1 zijn activiteit langzaam aan zelfs in deze mutants, wat aangeeft dat er ook een aparte, langzamere route naar TORC1 bestaat die onafhankelijk is van dit GTPase-systeem.
Een onverwachte rol voor een verre subunit
Een bijzonder intrigerende bevinding betreft Sea2, een SEACAT-component met een flexibele "propeller"-domein dat uitsteekt uit de kern. Het verwijderen van Sea2, of alleen zijn propeller, veroorzaakte signaaldefecten die bijna identiek waren aan die gezien wanneer de katalytische activiteit van SEAC verloren ging: TORC1 reageerde traag op zowel aminozuuronttrekking als -herintroductie. Toch ligt Sea2 ver van het katalytische centrum en raakt het de SEACIT-vleugel niet direct, waardoor een eenvoudig blokkeringsmechanisme onwaarschijnlijk is. Genetische experimenten waarin verlies van Sea2 werd gecombineerd met een katalytisch dood SEAC-variant suggereerden dat het volledig aan- of uitzetten van GAP-activiteit beide de snelle respons verstoort, terwijl een tussentijdse regulatie nodig is. De auteurs stellen voor dat Sea2’s propeller fungeert als een aanhechtingsplatform voor een onbekende factor die de activiteit van SEACIT matigt, waardoor cellen TORC1 kunnen fijnregelen in plaats van het permanent uit te schakelen.
Wat dit betekent voor beslissingen over celgroei
Samengevat herinterpreteert de studie SEAC niet als twee tegengestelde assemblages maar als één geïntegreerde machine waarvan de katalytische vleugel (SEACIT) en de structurele kern (SEACAT) samenwerken om aminozuren te detecteren en de groeischakelaar TORC1 snel aan te passen. De enzymatische werking van SEACIT op EGOC levert de snelle, nauwkeurige controle, terwijl Sea2’s propeller waarschijnlijk regulatoren rekruteert die deze activiteit moduleren. Tegelijkertijd zorgen tragere, parallelle routes ervoor dat TORC1 uiteindelijk nog steeds de voedingsstatus weerspiegelt, zelfs als de primaire sensor verstoord is. Omdat nauw verwante complexen hetzelfde werk uitvoeren in menselijke cellen, verhelderen deze inzichten uit gist hoe onze eigen cellen groei afwegen tegen voedingsaanbod, met implicaties voor het begrijpen van ziekten waarbij TORC1-signaalering verstoord is.
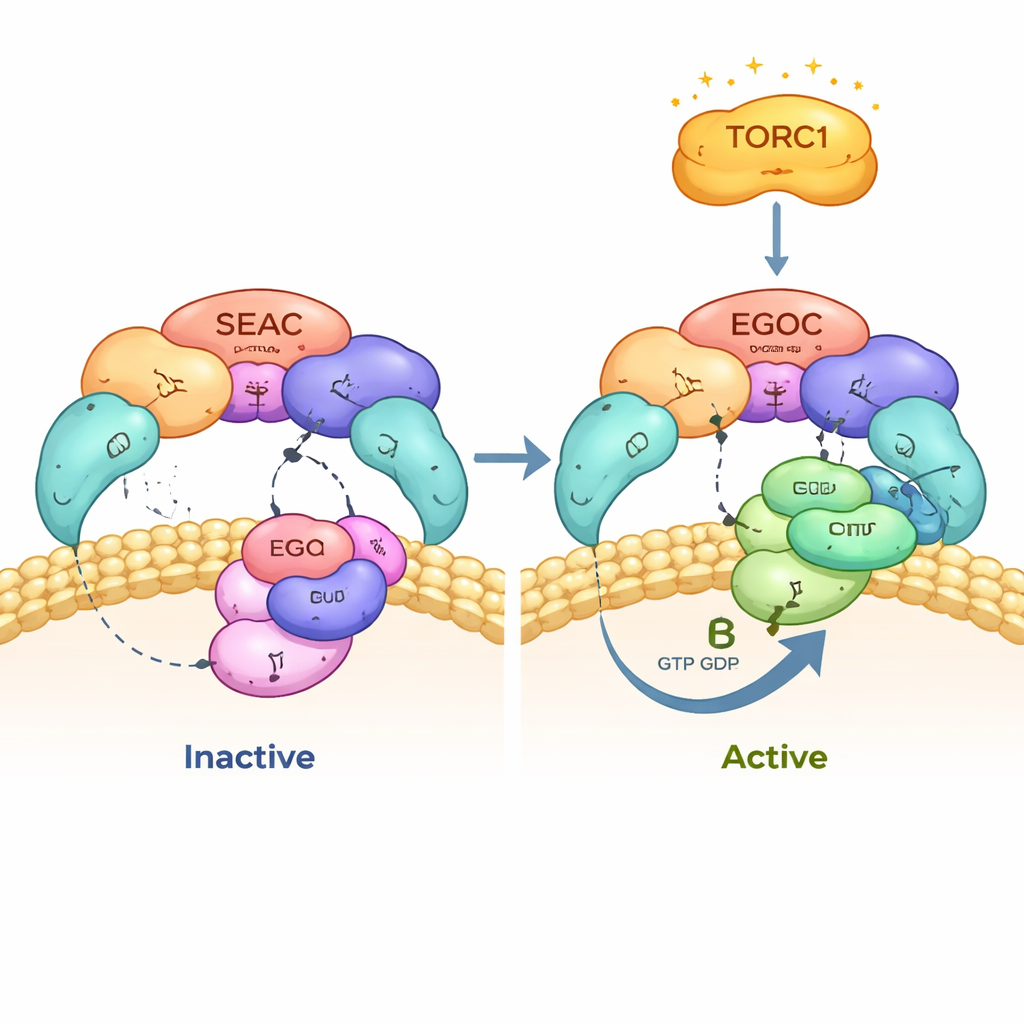
Bronvermelding: Tafur, L., Bonadei, L., Zheng, Y. et al. Structure and function of the yeast amino acid-sensing SEAC–EGOC supercomplex. Nat Struct Mol Biol 33, 488–498 (2026). https://doi.org/10.1038/s41594-026-01746-2
Trefwoorden: detectie van aminozuren, TORC1-signaaltransductie, SEAC GATOR-complex, controle van celdeling, kryo-elektronenmicroscopie