Clear Sky Science · nl
De filamentachtige ultrastructuur van het PopZ-condensaat is vereist voor zijn cellulaire functie
Hoe cellen zachte druppels gebruiken om georganiseerd te blijven
In elke levende cel is de chemie drukkend en chaotisch. Toch slagen cellen erin cruciale moleculen op de juiste plek en het juiste moment te houden. Eén manier waarop ze dit doen is door het vormen van kleine, vloeibare-achtige druppels, of condensaten, die bepaalde eiwitten verzamelen terwijl andere worden uitgesloten. Deze studie kijkt nauwkeurig naar één zo’n drup-bouwend eiwit in bacteriën, genoemd PopZ, en toont aan dat het interne geraamte van kleine filamenten essentieel is om de levensnoodzakelijke processen van de cel op koers te houden.
Een microscopische organisator aan de polen van de cel
In de bacterie Caulobacter crescentus verzamelt PopZ zich aan de twee uiteinden, of polen, van de cel waar het geconcentreerde compartimenten vormt. Deze PopZ-rijke “microdomeinen” helpen de celcyclus te regelen door specifieke partner-eiwitten aan te trekken en het chromosoom tijdens deling te verankeren. Wanneer PopZ wordt verwijderd, delen cellen moeizaam, verliezen hun normale vorm en gaan ze slordig om met hun DNA. Eerder onderzoek toonde aan dat als PopZ-druppels te vloeibaar of te stijf zijn, cellen ook moeite hebben. Wat onbekend bleef, was hoe de gedetailleerde structuur binnen deze druppels — de manier waarop PopZ-moleculen zich tot grotere vormen assembleren — aanleiding geeft tot hun materiaaleigenschappen en tot correct cellulair gedrag.
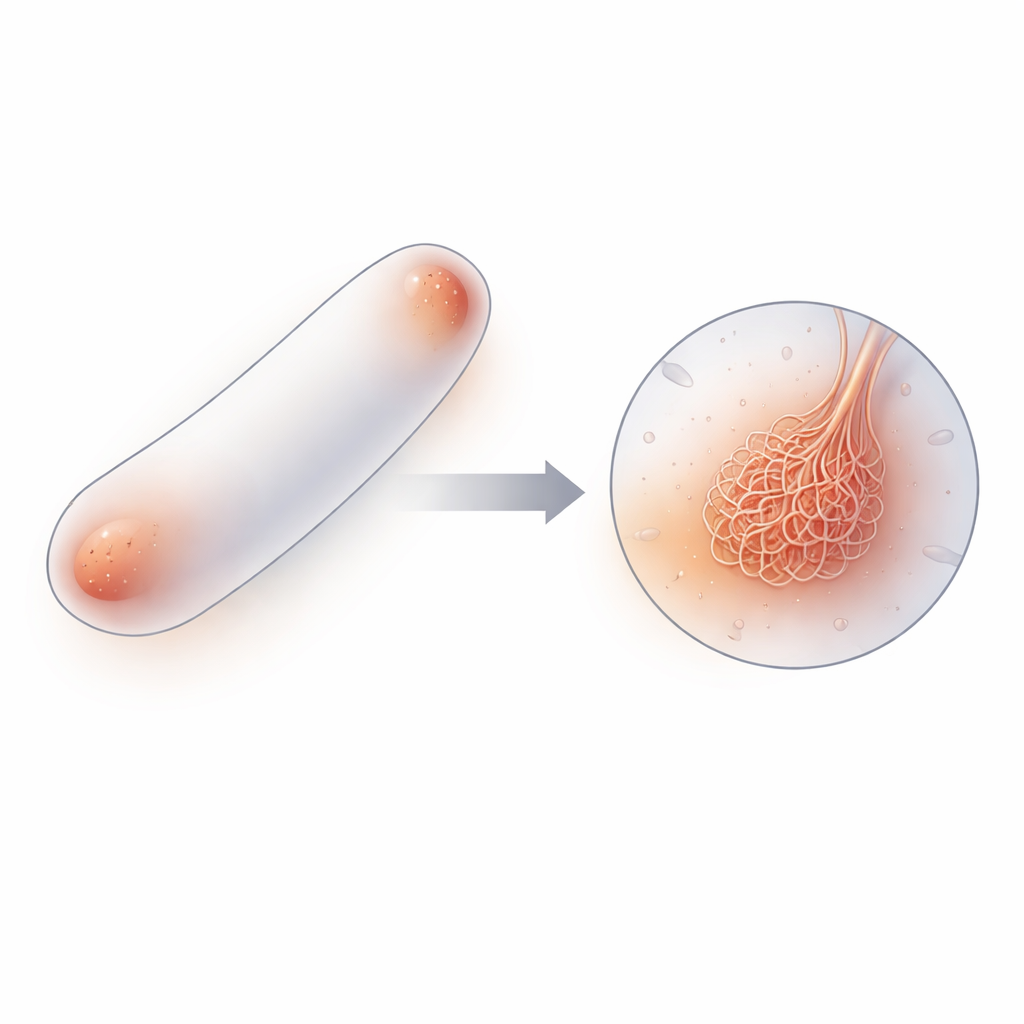
Van individuele moleculen naar een netwerk van filamenten
Met een combinatie van cryo–elektronentomografie (een 3D-afbeeldingsmethode bij zeer lage temperaturen), biochemische testen, enkelmolecuulfluorescentie en computersimulaties brachten de auteurs in kaart hoe PopZ-moleculen zich over verschillende schalen assembleren. Individuele PopZ-proteïnen vormen eerst driedeeltjes-eenheden (trimers), die vervolgens paren en zesdeeltjes-eenheden (hexameren) vormen. Deze hexameren stapelen zich eind-aan-eind tot korte, flexibele filamenten van enkele tientallen nanometers lang, en verwarde netwerken van deze filamenten vormen het PopZ-condensaat. Beelden van zowel gezuiverde PopZ-druppels als PopZ in intacte cellen toonden hetzelfde filamentachtige netwerk, wat laat zien dat deze architectuur geen artefact is van reageerbuisexperimenten maar een kernkenmerk van hoe PopZ in levende bacteriën functioneert.
Ingebouwde remmen en schakelaars voor druppelvorming
PopZ bestaat uit verschillende secties die elk een andere rol spelen in deze assemblagelijn. Een compacte helixachtige segment aan het staartuiteinde fungeert als het belangrijkste oligomerisatie- en filamentvormende module, krachtig genoeg om op zichzelf filamenten en druppels te bouwen. Daarentegen neigt een slapper, negatief geladen stuk in het midden ertoe moleculen uit elkaar te houden, waardoor condensatie wordt bemoeilijkt. Aan het tegenovergestelde uiteinde rekruteert een korte helix zowel cliënt-eiwitten als, in de verdunde toestand, zich terug te vouwen om het staartgedeelte te raken, wat vroegtijdige clustering verder ontmoedigt. Wanneer de omstandigheden veranderen — bijvoorbeeld bij de aanwezigheid van bepaalde zouten — worden deze afstotende interacties verzwakt. PopZ verandert dan van vorm: de cliënt-bindende helix zwaait weg van de staart, de remmende wolk van gedesordeerde segmenten opent zich, hexameren stapelen makkelijker tot filamenten en inter-filamentcontacten worden gunstiger. Deze fasedependente conformationele verandering betekent dat hetzelfde eiwitgebied dat in de verdunde toestand binding blokkeert, een actief dockingpunt wordt zodra een condensaat is gevormd.
Wat gebeurt er wanneer de filamenten worden verwijderd
Om te onderzoeken hoe filamenten het fysieke gedrag van de druppel beïnvloeden, maakten de onderzoekers PopZ-mutanten die nog wel hexameren konden vormen, maar deze niet meer konden stapelen tot filamenten. Deze varianten produceerden wel condensaten, maar met opvallend andere eigenschappen. In plaats van nette bolletjes die op het oppervlak rusten, werden de druppels afgevlakt en uitgespreid, wat wijst op een lagere oppervlaktespanning en sterkere bevochtiging van hun omgeving. Binnen deze filamentarme condensaten bewogen zowel PopZ zelf als zijn cliënt-eiwitten veel sneller, gemeten met fluorescentieherstel na photobleaching. Met andere woorden, het wegnemen van filamenten maakte de druppels zachter en lekkender. Toen zulke mutanten in Caulobacter-cellen werden geïntroduceerd, verstoorden ze het normale PopZ-gedrag aan de polen, interfereerden met chromosoomverankering en schaadden ze de groei ernstig, zelfs wanneer wildtype PopZ nog aanwezig was. Andere geconstrueerde varianten toonden het omgekeerde matchprobleem: ze konden filamenten vormen maar slaagden er niet in efficiënt te condenseren, en ook deze konden PopZ’s cellulaire rol niet volledig herstellen.
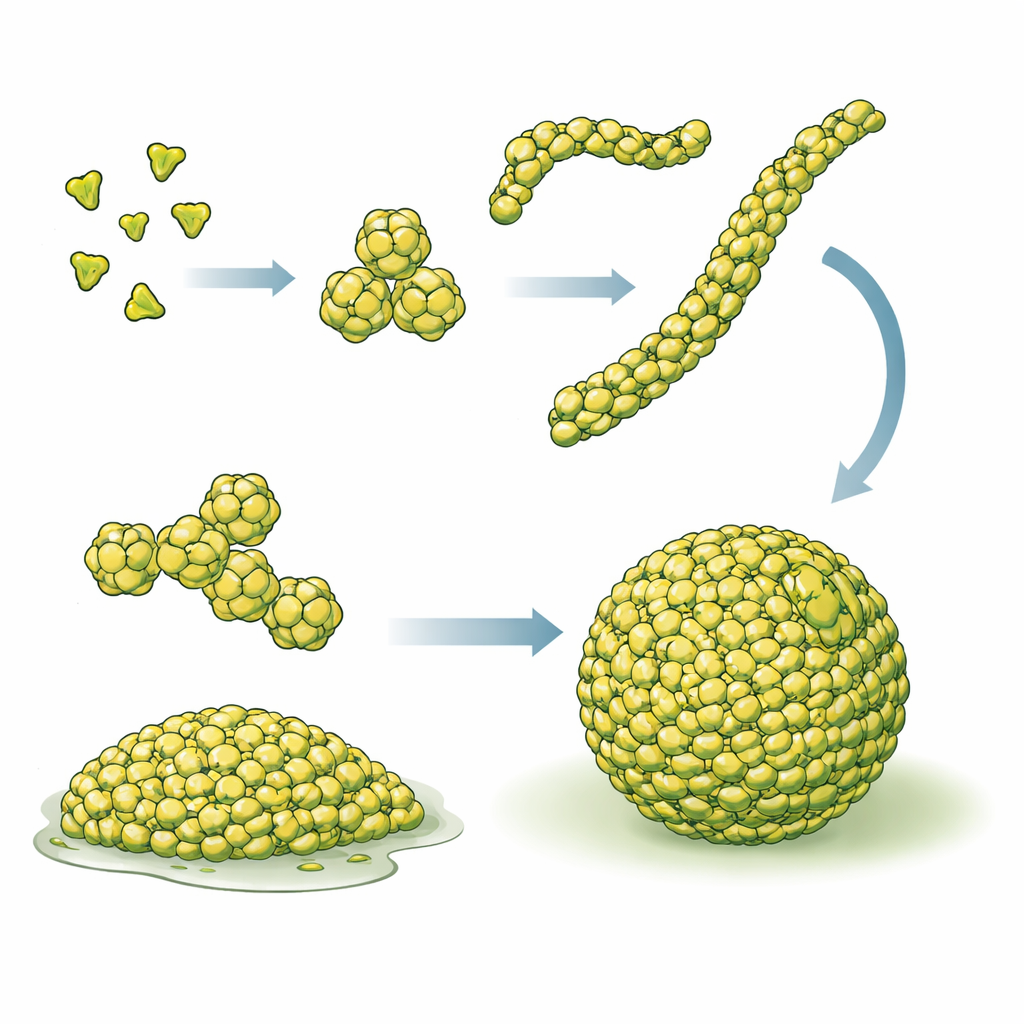
Een recept voor functionele cellulaire druppels
Het werk leidt tot een duidelijke boodschap voor niet-specialisten: het is niet voldoende dat een eiwit zoals PopZ gewoon samenklontert, en het is ook niet genoeg om filamenten geïsoleerd te vormen. Wat telt voor celfunctie is een zeer specifieke ultrastructuur — condensaten die zelf zijn opgebouwd uit korte, onderling verbonden filamenten. Dit filamentachtige geraamte vergroot het aantal contactpunten tussen moleculen, verhoogt de oppervlaktespanning van de druppel, vertraagt de beweging van belangrijke cliënten en biedt een ingebouwde moleculaire schakel die cliëntbinding pas inschakelt in de dichte fase. Door deze keten van oorzaak en gevolg te volgen van aminozuursequentie naar moleculaire assemblages en vervolgens naar gedrag op celniveau, biedt de studie een algemeen stappenplan voor hoe cellen de ‘gevoel’ van hun zachte interne druppels kunnen afstemmen om vitale processen te beheersen.
Bronvermelding: Scholl, D., Boyd, T., Latham, A.P. et al. The filamentous ultrastructure of the PopZ condensate is required for its cellular function. Nat Struct Mol Biol 33, 420–432 (2026). https://doi.org/10.1038/s41594-025-01742-y
Trefwoorden: biomoleculaire condensaten, proteïnefilamenten, celpolariteit, faseafscheiding, bacteriële celcyclus