Clear Sky Science · nl
Mechanisme en reconstitutie van circadiane transcriptie in cyanobacteriën
Waarom biologische klokken ertoe doen, zelfs bij bacteriën
Alle levende wezens, van mensen tot kleine microben, houden de tijd bij. Deze interne klokken helpen organismen om zonsopgang en zonsondergang te voorspellen en activiteiten zoals voeding, herstel en groei in te plannen. Dit artikel onderzoekt hoe een eenvoudige fotosynthetische bacterie, Synechococcus elongatus, een eiwitgebaseerde klok gebruikt om genen met opmerkelijke precisie gedurende een cyclus van 24 uur aan- en uit te zetten. Door dit tijdhoudingssysteem in een reageerbuis te herbouwen, tonen de onderzoekers een afgeslankte versie van een biologische klok die nieuwe instrumenten voor biotechnologie en synthetische biologie zou kunnen inspireren.
Een kleine klok die op chemie draait
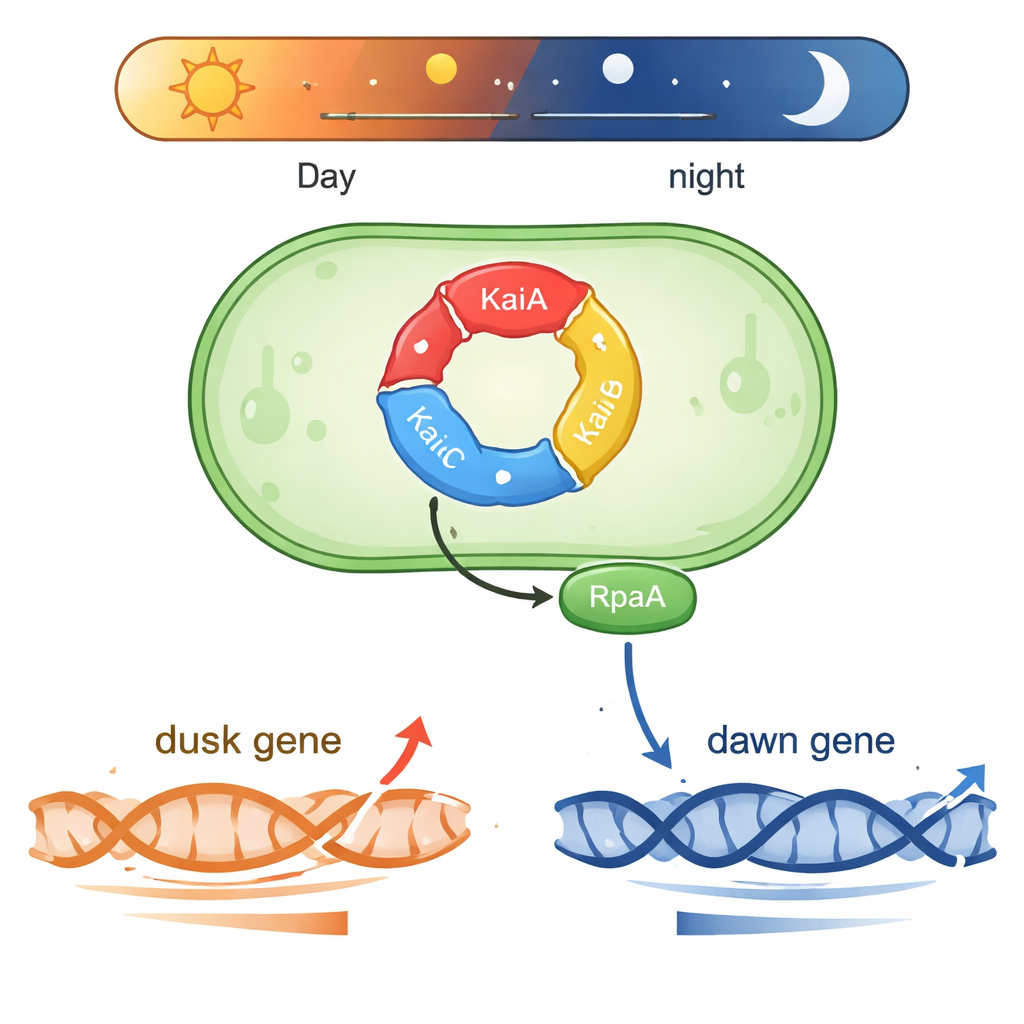
Synechococcus leeft in zonnig water en moet dagelijkse lichtveranderingen voorspellen. In de kern bevindt zich een drietalig eiwitcomplex bestaande uit KaiA, KaiB en KaiC. Deze eiwitten geven fosfaatgroepen aan elkaar door in een herhalende cyclus van ongeveer 24 uur, waardoor een biochemische "tandwieloverbrenging" ontstaat die de tijd bijhoudt, zelfs buiten de cel. Twee andere eiwitten, SasA en CikA, lezen de fosforylatiestatus van KaiC en gebruiken die om een ander eiwit, RpaA, te regelen. Wanneer RpaA gefosforyleerd is, bindt het aan DNA en fungeert het als een hoofdschakelaar voor honderden genen die in constante lichtomstandigheden rond subjectieve "dageraad" of "schemering" omhoog en omlaag gaan.
Eén eiwit, twee tegengestelde genprogramma’s
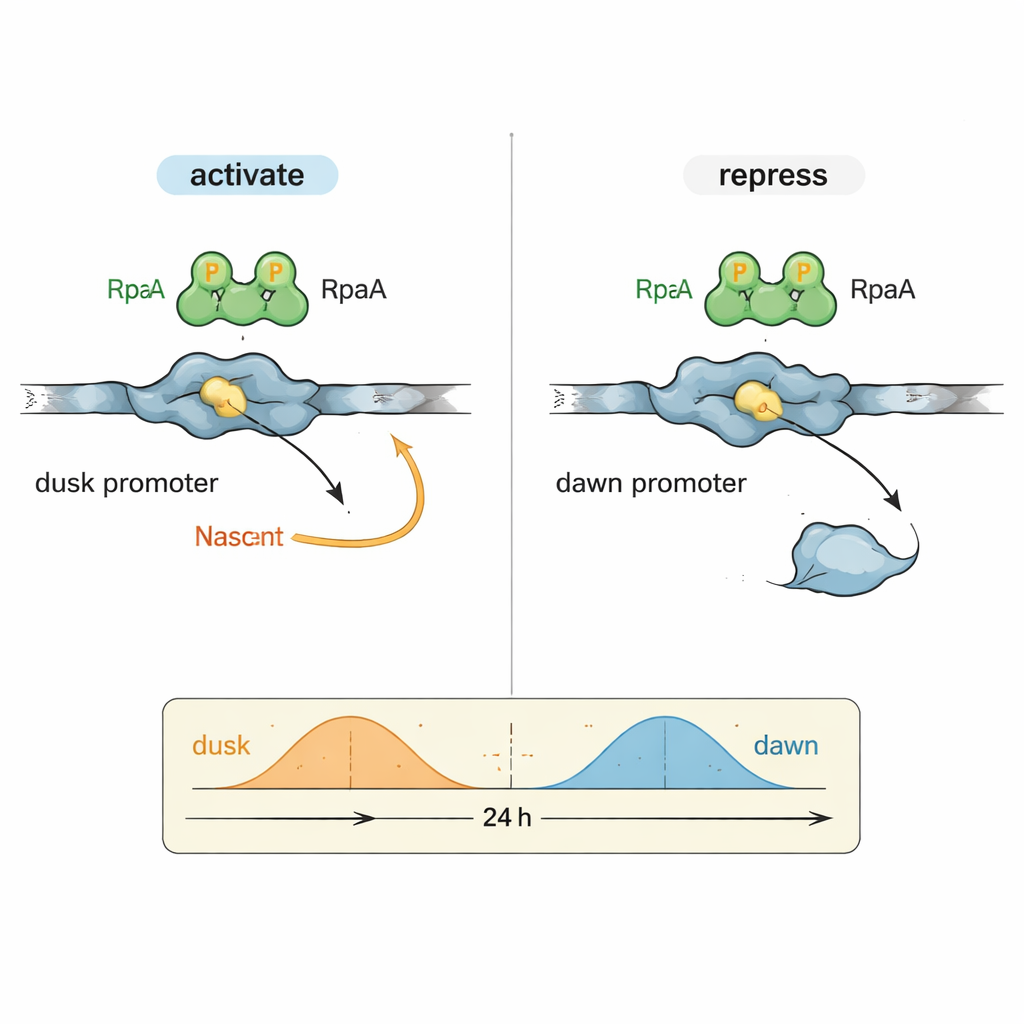
Een raadsel in de circadiane biologie is hoe één uitvoereiwit, RpaA, genen kan coördineren die op heel verschillende momenten van de dag een piek bereiken. De auteurs richtten zich op twee representatieve DNA-regio’s (promoters): kaiBC, dat het meest actief is bij schemering, en purF, dat piekt bij dageraad. In gecontroleerde reacties met gezuiverde cyanobacteriële RNA-polymerase en RpaA lieten ze zien dat gefosforyleerd RpaA de transcriptie vanaf de kaiBC-promoter versterkt terwijl het tegelijkertijd de transcriptie vanaf de purF-promoter vermindert. Gedetailleerde footprinting-experimenten brachten precies in kaart waar RpaA aan elk stuk DNA bindt, wat onthult dat zijn positie ten opzichte van de standaard promotorelementen bepaalt of het als gas of als rem fungeert.
De schakelaar van de klok in atomair detail zien
Om dit dubbele gedrag op moleculair niveau te begrijpen, gebruikte het team cryo-elektronenmicroscopie met hoge resolutie om de structuur vast te leggen van RpaA gebonden aan de kaiBC-promoter samen met RNA-polymerase. De beelden tonen RpaA dat het DNA als een asymmetrisch paar grijpt en contact maakt met twee sleutelonderdelen van het enzym: de staart van de alfa-subunit en een regio van de sigmafactor die normaal promotorsequenties herkent. Deze contacten buigen het DNA en helpen RNA-polymerase te positioneren op een iets herdefinieerde startplaats voor transcriptie. Zorgvuldig gekozen mutaties die één van deze contactpunten verzwakken verminderen of doen de activatie van kaiBC verdwijnen, zowel in vitro als in levende cellen, wat bevestigt dat fysieke rekrutering van RNA-polymerase ten grondslag ligt aan de genactivatie tijdens de schemeringsfase.
Een klokgestuurd gen vanaf nul opbouwen
Aangezien het native cyanobacteriële RNA-polymerase complex is en moeilijk actief te houden gedurende dagen, schakelden de onderzoekers vervolgens over op het veel eenvoudigere T7-bacteriofaagpolymerase, dat in laboratoria veel wordt gebruikt. RpaA kan dit niet-verwante enzym niet rekruteren, maar kan het nog steeds blokkeren door op het DNA te gaan zitten. Het team ontwierp een synthetische DNA-template waarin een T7-promoter een fluorescerende RNA-"Broccoli"-reporter aandrijft, met een RpaA-bindingsplaats stroomafwaarts geplaatst. Wanneer ze deze template combineerden met het KaiA–KaiB–KaiC-klokmechanisme, de CikA kinase/phosphatase, RpaA en T7-polymerase in één geoptimaliseerde buffer, observeerden ze op- en afnemende transcriptiesnelheden met een periode van ongeveer 24 uur. Het ritme kon worden gereset door de ATP-tot-ADP-verhouding te veranderen en handhaafde vrijwel dezelfde periode over een reeks temperaturen—klassieke kenmerken van een echte circadiane klok.
Van eenvoudige klokken naar ontworpen tijdsregeling
De studie toont aan dat slechts zes eiwitten voldoende zijn om een chemische pacemaker te koppelen aan ritmische genuitvoer: de drie Kai-klokeiwitten, CikA, RpaA en een RNA-polymerase. Door te veranderen waar RpaA op DNA zit, kan hetzelfde molecuul sommige genen bij schemering piekeren en andere bij dageraad, wat helpt de complexe golven van genactiviteit in cyanobacteriën te verklaren. Omdat het repressie-gebaseerde ontwerp zelfs werkt met een vreemd polymerase zoals T7, zou het mogelijk moeten zijn om deze minimale klokmodule in andere microben of celvrije systemen te transplanteren, zodat wetenschappers genen kunnen programmeren om met dagelijkse ritmes aan- en uitgezet te worden voor onderzoek, industriële productie of toekomstige therapeutische toepassingen.
Bronvermelding: Fang, M., Gu, Y., Leanca, M. et al. Mechanism and reconstitution of circadian transcription in cyanobacteria. Nat Struct Mol Biol 33, 275–281 (2026). https://doi.org/10.1038/s41594-025-01740-0
Trefwoorden: circadiaanse klok, cyanobacteriën, transcriptieregulatie, RpaA, synthetische biologie