Clear Sky Science · nl
Cereblon veroorzaakt afbraak van G3BP2 als neosubstraat door moleculaire oppervlaknadering
Cellulaire opruiming omvormen tot een slim richtsysteem
Moderne geneesmiddelen proberen ziekte steeds vaker niet alleen te bestrijden door probleem-eiwitten te blokkeren, maar door ze volledig te verwijderen. Dit artikel onderzoekt een slimme manier om een van de cellulaire "opruimmachines" om te bouwen zodat die, wanneer gecombineerd met een klein molecuul, een eiwit dat aan kanker en andere aandoeningen gelinkt is kan herkennen en vernietigen. Het werk onthult een onverwachte truc: de opruimmachine herschept een deel van zijn oppervlak zodat het een natuurlijke partner van het doelwit nabootst, waardoor het kan vastgrijpen en het eiwit naar het cellulaire afval stuurt.
Een cellulaire vuilverzamelaar met verborgen flexibiliteit
Onze cellen markeren voortdurend versleten of ongewenste eiwitten voor afbraak met een systeem rondom E3-ligases—grote eiwitcomplexen die beslissen wat weggegooid moet worden. Een dergelijk complex is afhankelijk van een component die cereblon heet en optreedt als sensor die specifieke kenmerken ("degrons") op andere eiwitten herkent. Bepaalde goedgekeurde geneesmiddelen benutten cereblon al als "moleculaire lijmen": ze binden aan cereblon en creëren een nieuw aanhechtingsvlak dat ziektegerelateerde eiwitten aantrekt, die vervolgens gemarkeerd en afgebroken worden. Tot nu toe gebruikten de meeste bekende doelwitten een bepaald structureel patroon, waardoor het scala aan eiwitten dat op deze manier kon worden verwijderd beperkt leek.
Een nieuw doel buiten de oude regels ontdekken
In de nieuwe studie screeneden de auteurs een verzameling cereblon-gerichte moleculaire lijmen in menselijke cellen en identificeerden ze een verbinding genaamd MRT-5702. Dit kleine molecuul veroorzaakte een snelle verdwijning van een eiwit genaamd G3BP2, dat helpt RNA te beheren en deel uitmaakt van stressgranulen—assemblages die gekoppeld zijn aan kanker, hartproblemen en neurodegeneratieve ziekten. Belangrijk is dat G3BP2 het gebruikelijke degronpatroon mist dat cereblon herkent. Vervolgexperimenten in cellen, waaronder gevoelige lichtgebaseerde metingen van eiwitnabijheid, bevestigden dat MRT-5702 cereblon en G3BP2 samenbrengt in een drieledig complex dat leidt tot G3BP2-afbraak, terwijl het nauw verwante broereiwit G3BP1 gespaard blijft tenzij zijn sleuteldomein wordt verwisseld.
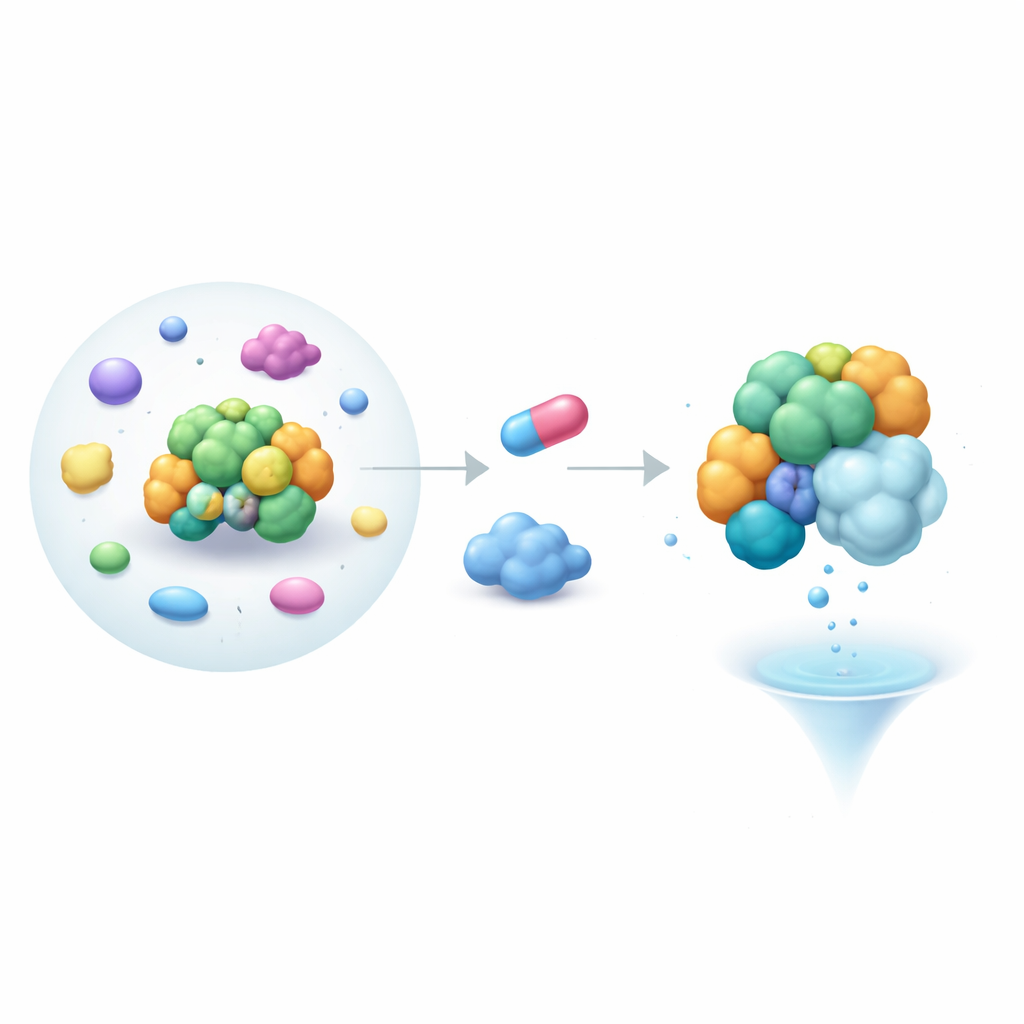
Nabootsing als bindingsstrategie
Dieper gravend vroegen de onderzoekers zich af hoe G3BP2 aan cereblon kon binden zonder het standaard herkenningsmotief. In plaats van te zoeken naar overeenkomsten tussen G3BP2 en bekende cereblon-doelen, keerden ze de vraag om: zou cereblon één van G3BP2’s gebruikelijke bindpartners kunnen nabootsen? G3BP-eiwitten interageren vaak met andere moleculen via een hotspot op een regio die het NTF2-achtige domein wordt genoemd, dat normaal korte sequentiemotieven herkent. Met structurele modellen van de natuurlijke partner USP10 van G3BP2 scande het team computationeel cereblon’s oppervlak en vond een patch op een minder begrepen regio, het LON-domein, die de vorm en chemie van USP10’s bindingsmotief nauw lijkt na te bootsen. Het veranderen van slechts een paar sleutelaminozuren op dit patch, of in de G3BP2-hotspot, verzwakte het drieledige complex, wat suggereert dat cereblon effectief USP10 imiteert om zich aan G3BP2 te hechten.
Het nieuwe interface vastleggen in atomaire details
Om deze ongebruikelijke interactie te visualiseren, gebruikte het team cryo-elektronenmicroscopie met hoge resolutie om de structuur op te lossen van een complex met cereblon, een andere kerncomponent van de ligase, MRT-5702 en het NTF2-achtige domein van G3BP2. De beelden toonden dat een flexibele lus in cereblon’s LON-domein buigt en van vorm verandert om bijna de helft van het contactoppervlak met G3BP2 te vormen. De actieve spiegelvorm van MRT-5702 zit in cereblon’s gebruikelijke geneesmiddel-bindingsplaats maar helpt, samen met de lus, een breed landingsvlak te creëren dat één helft van het G3BP2-dimeer opvangt. Opmerkelijk is dat deze opstelling nauwelijks het canonieke cereblon-oppervlak gebruikt dat eerdere lijm-doelen behandelde, wat aantoont dat cereblon zeer verschillende regio’s van zijn oppervlak kan aanspreken afhankelijk van de lijm en het betrokken eiwit. Tegelijk blijft de onaangetaste helft van het G3BP2-dimeer beschikbaar om andere partners te binden, wat een plausibele route biedt voor "collaterale" afbraak van eiwitten die eraan vastzitten.
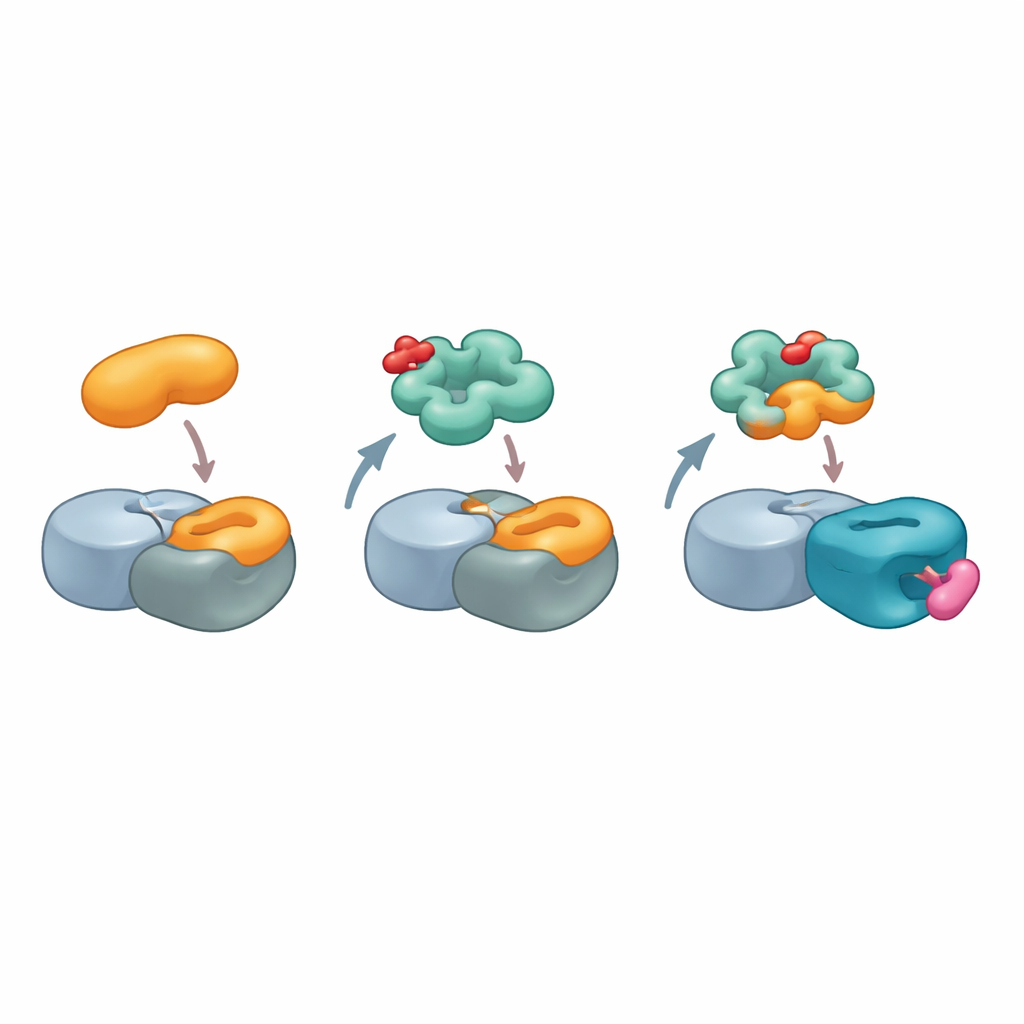
Lijmafdrukken voor toekomstige medicijnontwerp
Samengevat schetsen de bevindingen cereblon als een veel veelzijdigere matchmaker dan eerder werd aangenomen. In plaats van te eisen dat doelwitten één soort degron dragen, kan cereblon, wanneer uitgerust met de juiste moleculaire lijm, een samengesteld oppervlak vormen dat natuurlijke eiwit–eiwitcontacten elders in de cel nabootst. De auteurs stellen dat zulke gecombineerde eiwit-en-lijm-oppervlakken, die zij "glueprints" noemen, in kaart gebracht en ontworpen zouden kunnen worden om bestaande interactie-hotsports op vele ziektegeassocieerde eiwitten te imiteren. Voor een niet‑specialistische lezer is de kernboodschap dat geneesmiddelontwikkelaars mogelijk geen geheel nieuwe bindingspockets op probleem-eiwitten hoeven te vinden; in plaats daarvan kunnen ze de eigen recycleermachine van de cel leren die eiwitten te herkennen door slim de vormen van hun gebruikelijke partners te kopiëren, waardoor het bereik van veilig en selectief verwijderbare doelen sterk wordt vergroot.
Bronvermelding: Annunziato, S., Quan, C., Donckele, E.J. et al. Cereblon induces G3BP2 neosubstrate degradation using molecular surface mimicry. Nat Struct Mol Biol 33, 479–487 (2026). https://doi.org/10.1038/s41594-025-01738-8
Trefwoorden: moleculaire lijm-degraders, cereblon, gerichte eiwitafbraak, G3BP2, eiwit–eiwitinteracties