Clear Sky Science · nl
TGFβ‑signaalering bemiddelt microgliale veerkracht tegen ruimtelijk‑tijdelijk beperkte myelinedegeneratie
Waarom de bedrading van de hersenen verzorgers nodig heeft
Naarmate we ouder worden, slijt de “isolatie” rond onze zenuwvezels — myeline genoemd — vanzelf. Deze isolatie is cruciaal voor snelle, betrouwbare communicatie tussen hersenen en lichaam. De nieuwe studie onderzoekt waarom een specifieke zenuwroute in het ruggenmerg, de dorsale kolom, uitzonderlijk kwetsbaar is voor dit slijtageproces, en hoe een ingebouwde rem in het immuunsysteem, een signaalroute genaamd TGFβ, voorkomt dat schade uit de hand loopt. Het begrijpen van deze verborgen bescherming is belangrijk omdat het falen ervan bepaalde aandoeningen van het ruggenmerg kan helpen verklaren en invloed kan hebben op de behandeling van hersen‑ en kankerpatiënten op hogere leeftijd.
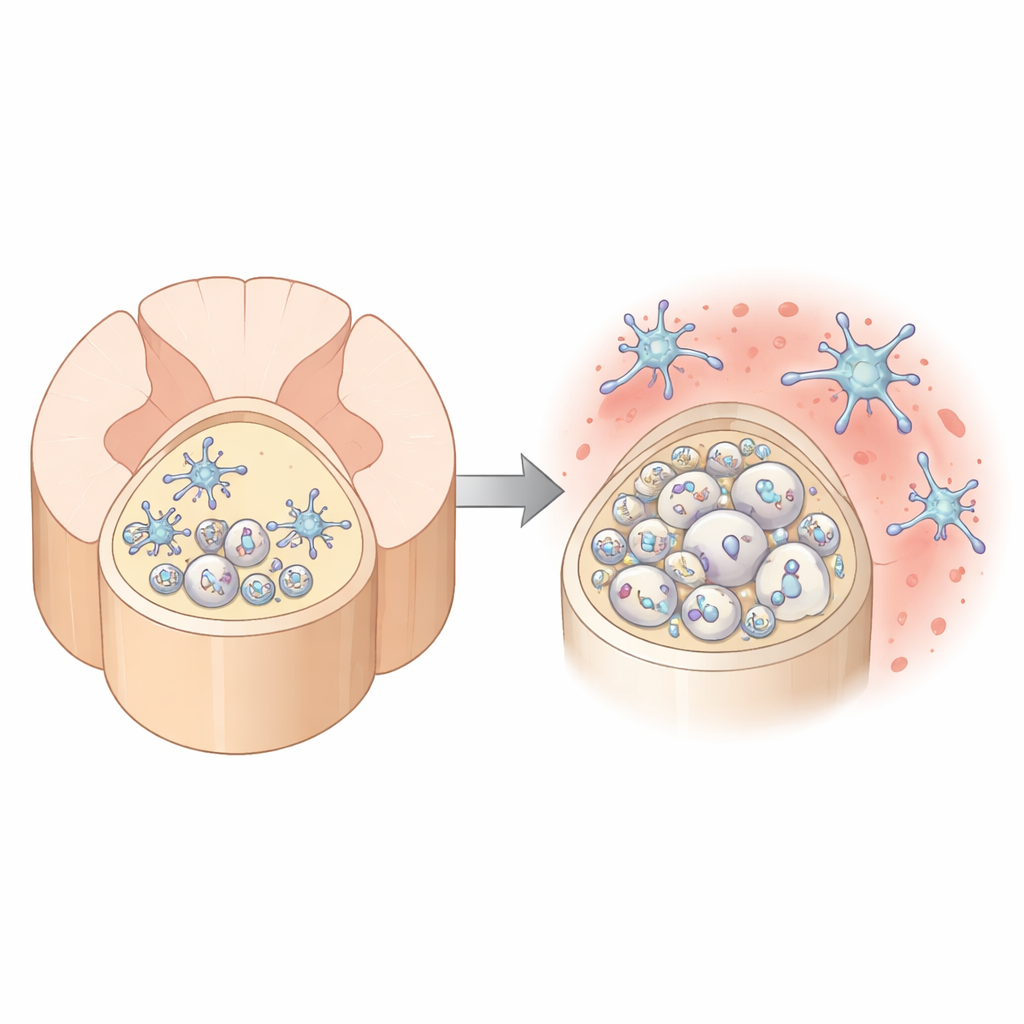
Waar veroudering de ruggenmerg‑“snelweg” het hardst treft
De auteurs vergeleken eerst twee belangrijke witte‑stofbanen in het muizenruggenmerg: de dorsale kolom achterin en de ventrale kolom vooraan. Met hoog‑resolutie elektronenmicroscopie vonden ze dat myeline in de dorsale kolom met de leeftijd steeds meer vervormt. De normaal strakke wikkelingen rond zenuwvezels laten los, bollen naar buiten of raken los, waardoor vergrote ruimtes ontstaan tussen zenuw en isolatie en het aantal gevallen van daadwerkelijke myelineafbraak toeneemt. De ventrale kolom blijft daarentegen relatief stabiel. De dorsale regio bevat bovendien veel meer, maar dunnere, axonen, wat het een bijzonder veeleisende omgeving maakt voor de cellen die myeline opbouwen en onderhouden.
Immune waakhonden onder toenemende druk
Rondom deze vezels bevinden zich microglia, de resident‑immuuncellen van hersenen en ruggenmerg. Ze patrouilleren continu in het weefsel, ruimen afval op en verfijnen verbindingen. Naarmate myeline in de dorsale kolom met de leeftijd afbreekt, beginnen deze microglia er anders uit te zien en anders te functioneren: ze reguleren genen omhoog die samenhangen met immuunactivatie, stapelen olierijke druppels op in hun binnenste en vertonen tekenen dat ze meer beschadigde myeline hebben opgenomen. Tegelijkertijd raakt de weefselomgeving in de dorsale kolom sterk verrijkt met TGFβ1, een signaalmolecuul dat bekendstaat om microglia in een geremde, homeostatische beschermende staat te houden. Microglia zelf zijn de belangrijkste bron van dit TGFβ1, wat suggereert dat ze proberen zichzelf onder controle te houden terwijl stresssignalen toenemen.
Wat er gebeurt als de veiligheidsrem faalt
Om te onderzoeken hoe belangrijk deze rem is, schakelden de onderzoekers de TGFβ‑signaalering specifiek in microglia van volwassen muizen genetisch uit, ofwel door de receptor te verwijderen die ze gebruiken om TGFβ te voelen, ofwel door te voorkomen dat ze TGFβ1 aanmaken. In beide gevallen was het resultaat opvallend overeenkomstig en sterk gelokaliseerd: microglia in de dorsale kolom werden overmatig talrijk, sterk geactiveerd en kregen een schuimige aanblik vol opgenomen myeline. Myeline in dit gebied werd ontdaan, axonen vertoonden degeneratietekenen en muizen ontwikkelden verergerende bewegings‑ en coördinatieproblemen, vooral bij het ouder worden. Andere ruggenmergregio’s waren veel minder getroffen, wat een regio‑specifieke afhankelijkheid van dit pad aantoont.
Een bijzondere microgliale subtype en gestreste myelinebouwers
Single‑nucleus RNA‑sequencing stelde het team in staat individuele celtypen te catalogiseren naarmate de ziekte zich ontwikkelde. Ze ontdekten een onderscheidende subset microglia — genoemd TGFβ‑gevoelige microglia — die dramatisch uitbreidde wanneer TGFβ‑signaalering werd verwijderd. Deze cellen drukten hoge niveaus uit van genen die geassocieerd worden met sterke ontstekingsreacties, intensieve myelineopname en lipidenverwerking, en ze waren geconcentreerd in de dorsale kolom. Tegelijkertijd verschoof de populatie volwassen myelinevormende cellen, oligodendrocyten. Gezonde subtypes namen af, terwijl een “ziekte‑geassocieerde” oligodendrocytengroep uitbreidde in de beschadigde dorsale kolom maar er niet in slaagde functionele myeline te herbouwen, waardoor axonen bloot bleven ondanks een schijnbare poging tot herstel.
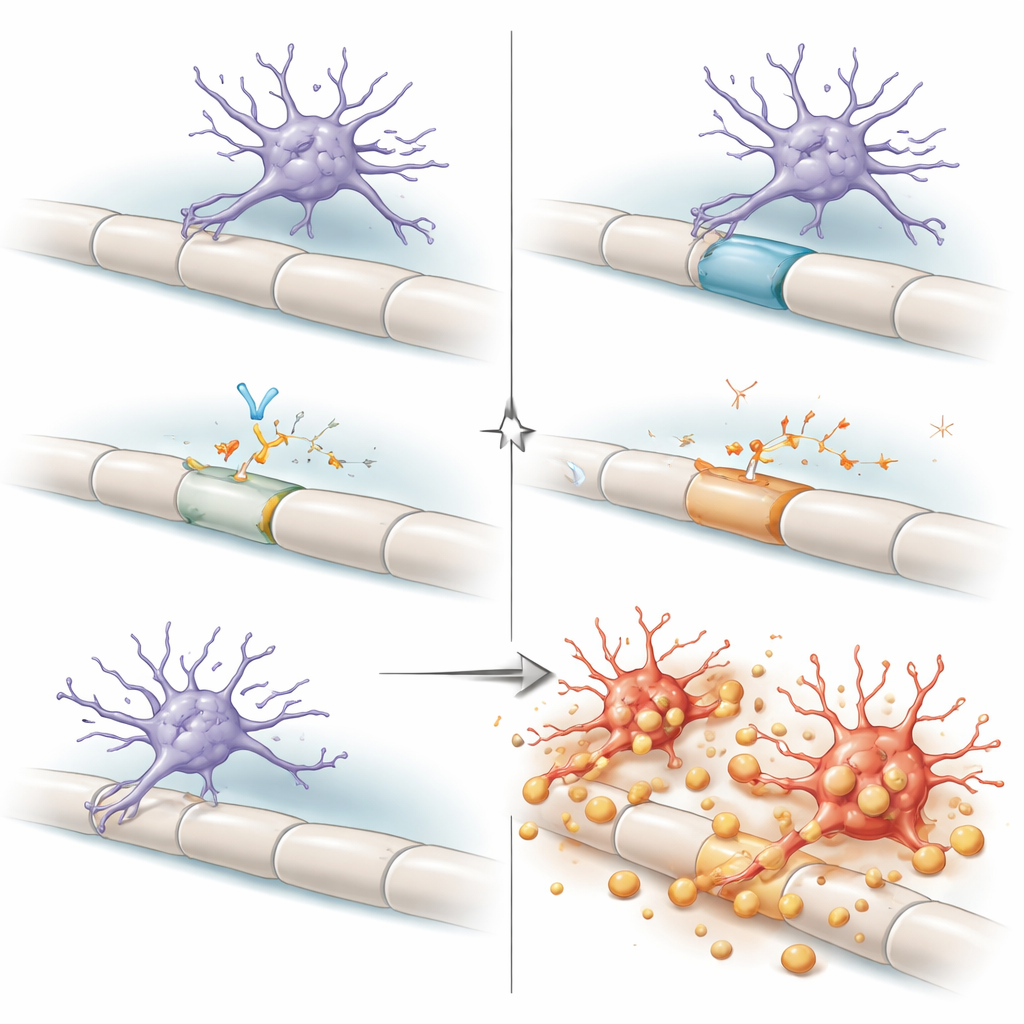
Implicaties voor veroudering en toekomstige therapieën
Gezien als geheel schetsen de bevindingen de dorsale kolom als een stressrijke buurt waar verouderende myeline en overbelaste ondersteunende cellen microglia naar een kantelpunt duwen. Onder normale omstandigheden houdt een autocriene lus — microglia die hun eigen TGFβ1 produceren en waarnemen — ze in een “geprimede maar veerkrachtige” staat, in staat om continu afval te verwerken zonder relatief intacte myeline aan te vallen. Als deze lus wordt doorbroken, schakelen microglia over naar een maladaptieve modus, waarbij ze myeline agressief strippen en neurologische achteruitgang aandrijven. Voor een algemeen publiek is de kernboodschap dat de immuuncellen van de hersenen niet eenvoudigweg goed of slecht zijn; hun gedrag hangt sterk af van lokale bedradingseisen en van moleculaire remmen zoals TGFβ. Omdat TGFβ‑blokkerende geneesmiddelen worden ontwikkeld voor kanker en sommige hersenaandoeningen, geeft dit werk een belangrijke waarschuwing: het verstoren van dit pad, met name bij oudere mensen, kan per ongeluk kwetsbare ruggenmergregio’s beschadigen door microglia los te laten op juist die isolatie die onze zenuwen nodig hebben om te functioneren.
Bronvermelding: Zhu, K., Liu, Y., Min, JH. et al. TGFβ signaling mediates microglial resilience to spatiotemporally restricted myelin degeneration. Nat Neurosci 29, 617–631 (2026). https://doi.org/10.1038/s41593-025-02161-4
Trefwoorden: microglia, myelineveroudering, dorsale kolom van het ruggenmerg, TGF beta‑signaalering, neuroinflammatie