Clear Sky Science · nl
Scaffolds met geoptimaliseerde quaternaire symmetrie voor de novo cryo-EM-structuurbepaling van kleine RNA's
De kleinste vormen van RNA zichtbaar maken
In elke cel vouwen korte RNA-strengen zich tot kleine driedimensionale vormen die genen aan- of uitzetten, cellulaire schade waarnemen of oplichten onder een microscoop. Veel van deze RNA's zijn zo klein dat huidige beeldvormingstechnieken moeite hebben hun precieze architectuur te onthullen. Dit artikel beschrijft een slimme manier om deze lastige moleculen zichtbaar te maken: ze vastmaken aan een groter, zelfassemblerend RNA-“frame” dat duidelijk zichtbaar is met cryo-elektronenmicroscopie, een krachtige methode voor het afbeelden van bevroren biomoleculen.
Een behulpzaam RNA-frame bouwen
De auteurs begonnen met een RNA-segment uit een virus dat van nature de neiging heeft zich te vormen tot een structuur van twee delen. Ze herontwierpen dit segment zodat het, in plaats van slechts een klein deel van de tijd paren te vormen, nu bijna altijd regelmatige twee- of vierdelige structuren vormt in oplossing. Deze repeterende ordeningen creëren wat in wezen een RNA-frame of scaffold is, met ingebouwde symmetrie. Symmetrie is waardevol voor cryo-elektronenmicroscopie omdat identieke herhaalde eenheden samen gemiddeld kunnen worden, waardoor het uiteindelijke beeld scherper wordt.
Bekende RNA's als testgasten bevestigen
Om te testen of hun scaffold andere RNA's in beeld kon brengen, graften de onderzoekers goed bestudeerde moleculen op één regio van het frame. Eén gast was een transfer-RNA uit bacteriën, een klassieke L-vormige molecule die aminozuren tijdens de eiwitsynthese aflevert. Een andere was Mango-III, een klein, ontworpen RNA dat een kleurstof bindt en oplicht, veel gebruikt als fluorescent label. In beide gevallen voudden en paarden de gecombineerde moleculen zoals ontworpen, en cryo-elektronenmicroscopie leverde gedetailleerde kaarten van de algemene vormen. Voor het transfer-RNA waren de beelden scherp genoeg om subtiele verschillen te zien tussen de ongewijzigde vorm die hier werd gebruikt en eerder bestudeerde, chemisch gemodificeerde versies. Voor Mango-III toonden de kaarten dat het aptameer veel stijver wordt wanneer de kleurstof gebonden is, wat verklaart hoe binding de fluorescentie aanzet. 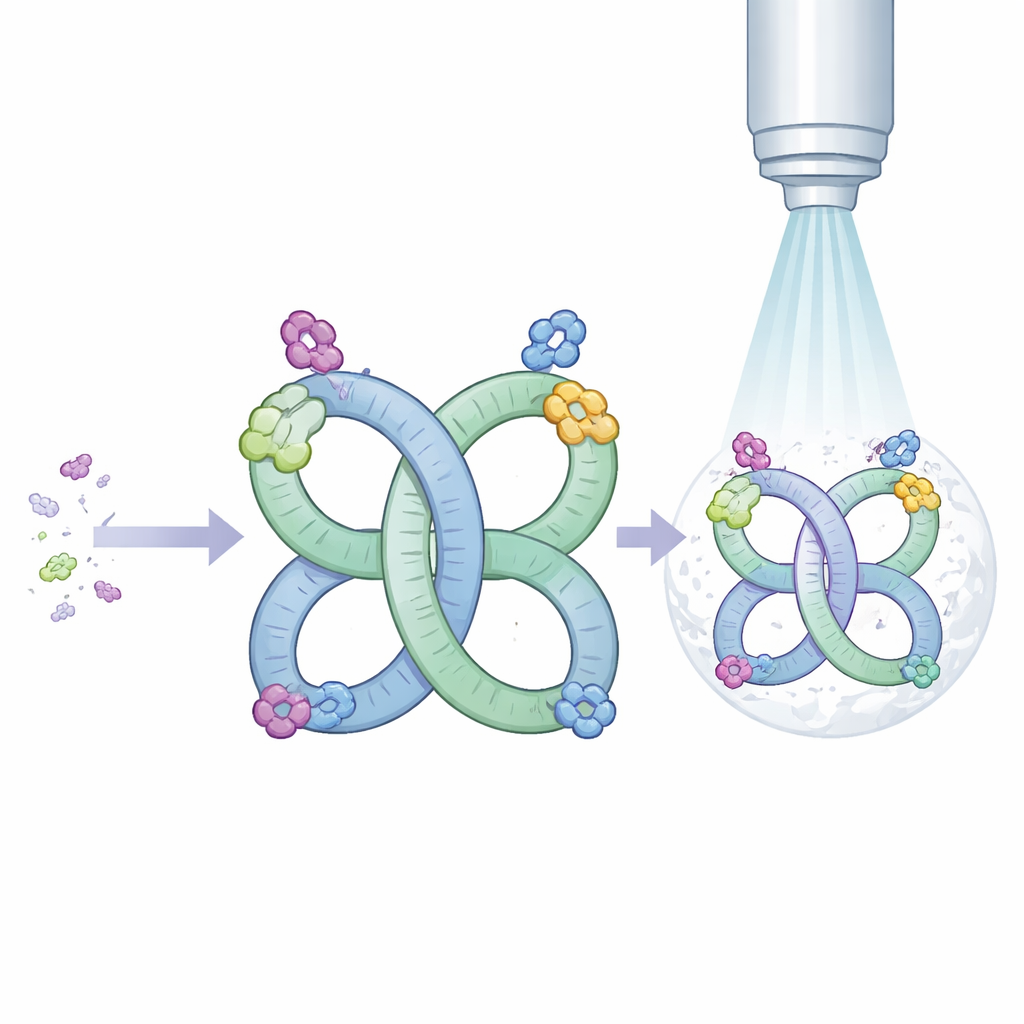
Onthullen hoe ontworpen RNA's kleine moleculen vasthouden
Het team ging vervolgens verder dan de testgevallen en nam RNA's onder de loep waarvan de volledige structuren nog niet gezien waren. Ze bevestigden twee kleine aptameren — korte RNA's die in het laboratorium zijn geselecteerd om specifieke kleine moleculen te binden — aan de scaffold. Het ene aptameer herkent het geneesmiddel kinine; het andere detecteert 8-oxoguanine, een beschadigde vorm van een genetische letter die oxidatieve stress in bacteriën signaleert. Dankzij de scaffold leverde cryo-elektronenmicroscopie uitzonderlijk hoogwaardige kaarten op, fijn genoeg om elke RNA-keten van begin tot eind te volgen en om te zien waar metaalionen en watermoleculen zitten. In het kinine-aptameer omvat de bindingsholte het geneesmiddel vooral door strakke stapeling en vormcomplementariteit, met verrassend weinig directe waterstofbruggen. In tegenstelling daarmee wikkelt het 8-oxoguanine-aptameer zijn ligand in een ingewikkeld web van waterstofbruggen die vrijwel elk chemisch onderscheidend deel van de beschadigde base contacteren, wat de scherpe discriminatie tussen 8-oxoguanine en normale guanine verklaart.
Flexibele symmetrie voor scherpere beelden
Opmerkelijk genoeg kan hetzelfde RNA-scaffold, afhankelijk van de omstandigheden en de aangehechte gast, ofwel in paren ofwel in vierdelige structuren assembleren. Wanneer een vierdelige ordening ontstaat, verbetert de herhaalde geometrie de beeldkwaliteit nog verder. In één geval nam het scaffold een vierdelige vorm aan hoewel de sequentie identiek was aan de tweedelige versie, wat benadrukt hoe kleine verschuivingen in basenparing de hele assemblage kunnen herschikken. De auteurs onderzochten ook praktische aspecten van cryo-elektronenmicroscopie-gegevensverzameling, zoals hoe het kantelen van het objecttafeltje voorkeursoriëntaties van de deeltjes op het grid kan overwinnen, en hoe het opleggen van symmetrie tijdens beeldverwerking de resulterende structuren bescheiden maar consistent verscherpt.
Een nieuw venster op kleine RNA-machines
Al met al toont dit werk aan dat een compact, symmetrisch RNA-frame anders onzichtbare kleine RNA's kan veranderen in uitstekende cryo-elektronenmicroscopie-doelen, waardoor structuren in gunstige gevallen tot voorbij atomaire details kunnen worden bepaald. Door een onbekend RNA aan de scaffold te hechten via een eenvoudige helicale verbinding, kunnen onderzoekers nu zijn driedimensionale vouwing bepalen, precies zien hoe het een klein-molecuulpartner grijpt, en geordende metaalionen en watermoleculen waarnemen die zijn gedrag afstemmen. Voor een breed publiek is de kernboodschap dat we nu een praktisch hulpmiddel hebben om sommige van de kleinste en meest veelzijdige RNA-machines in de natuur en biotechnologie van dichtbij te bekijken, wat de weg vrijmaakt voor rationeel ontwerp van nieuwe RNA-gebaseerde sensoren, geneesmiddelen en moleculaire apparaten. 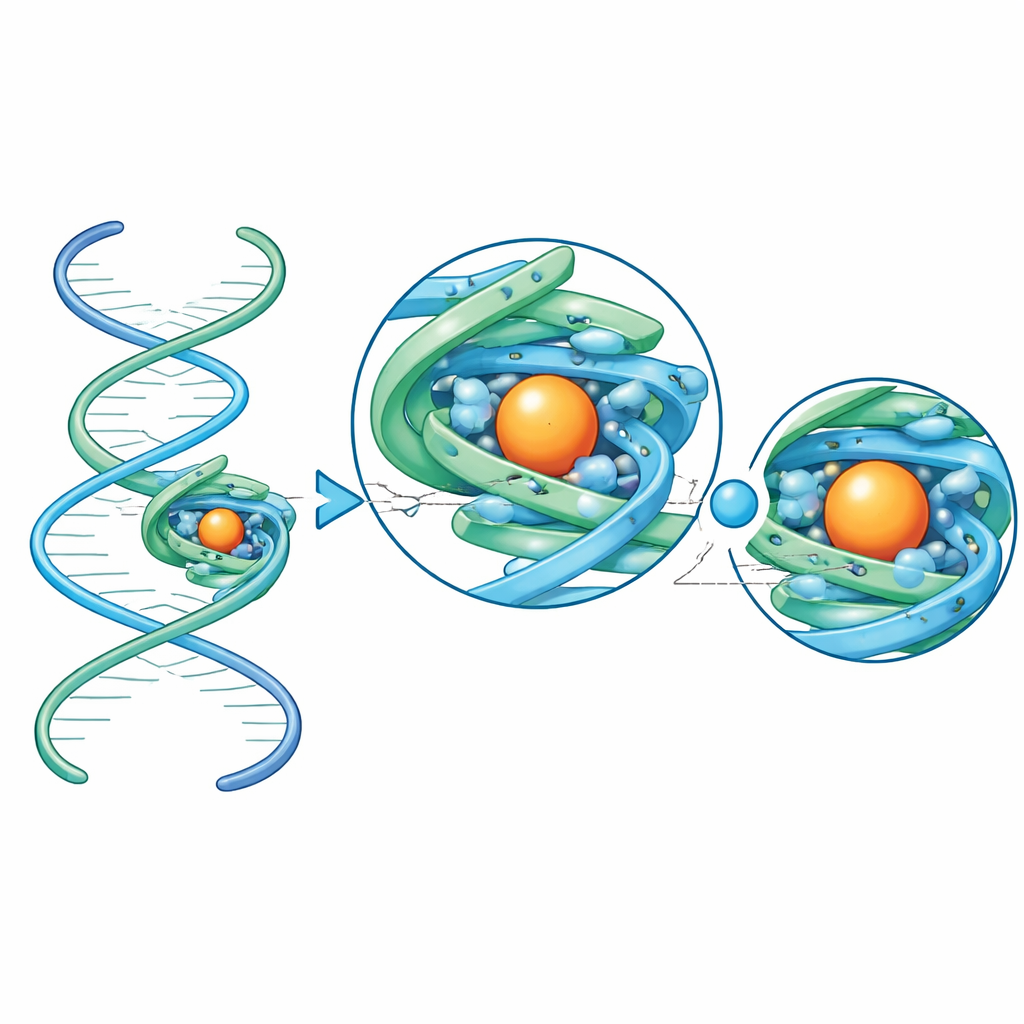
Bronvermelding: Jones, C.P., Ferré-D’Amaré, A.R. Scaffolds with optimized quaternary symmetry for de novo cryoEM structure determination of small RNAs. Nat Methods 23, 609–616 (2026). https://doi.org/10.1038/s41592-026-03016-x
Trefwoorden: RNA-structuur, kryo-elektronenmicroscopie, aptameer, riboswitch, moleculaire scaffolden