Clear Sky Science · nl
AF2BIND: het voorspellen van kleine-molecuul bindingsplaatsen met de pair-representatie van AlphaFold2
Het vinden van geneesmiddendoelen in een zee van eiwitten
Moderne medicijnen werken vaak door zich vast te hechten aan kleine nisjes en holtes op de oppervlakken van eiwitten in onze cellen. Zelfs met de enorme huidige catalogi van eiwitstructuren is het echter verrassend moeilijk om van tevoren te zeggen waar een klein molecuul — een potentiëel geneesmiddel — daadwerkelijk zal blijven zitten. Deze studie introduceert AF2BIND, een eenvoudige maar krachtige computationele tool die de interne gegevenslagen van AlphaFold2, de baanbrekende voorspeller van eiwitstructuren, benut om waarschijnlijke geneesmiddelbindingsplaatsen in duizenden menselijke eiwitten uit te lichten. Het doel is de zoektocht naar nieuwe medicijnen te verkleinen en verborgen functionele hotspots te onthullen die traditionele methoden over het hoofd zien.
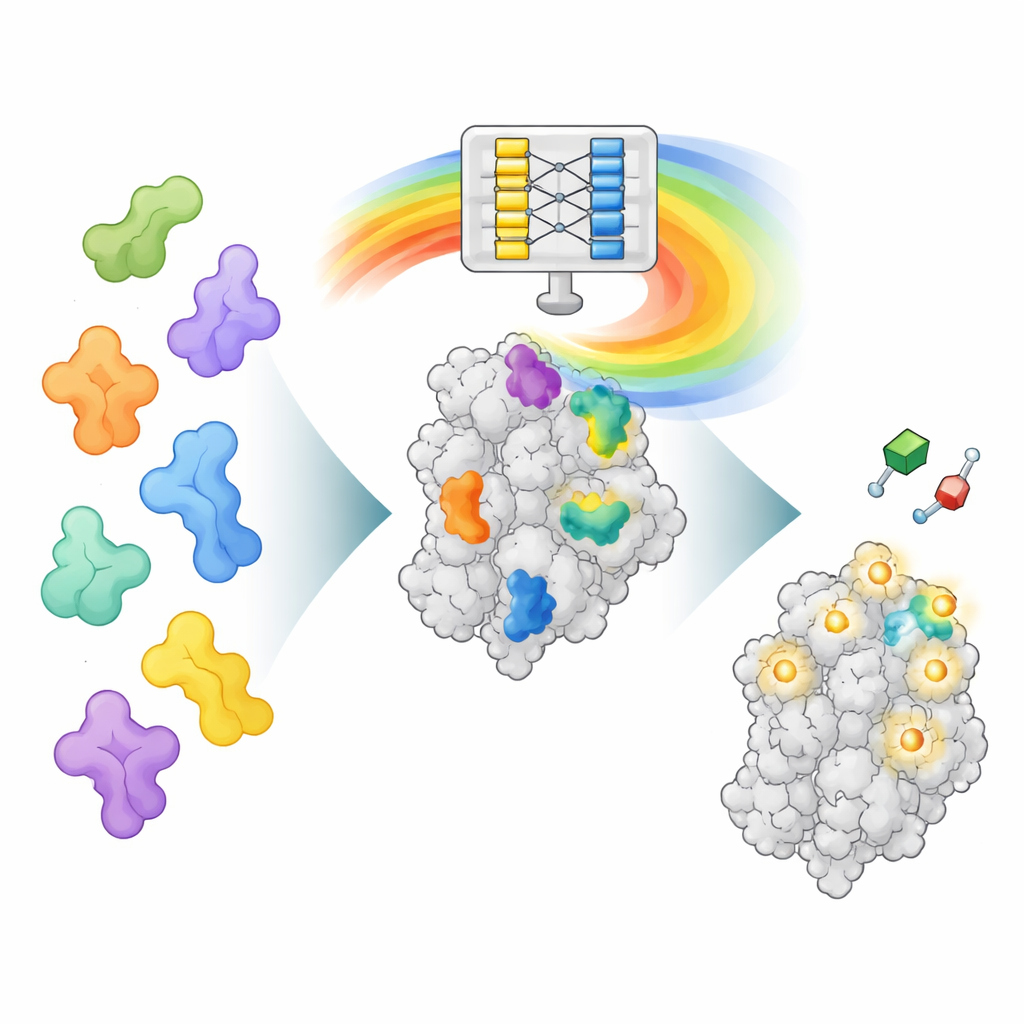
Een nieuwe manier om AlphaFold’s “denken” te lezen
AlphaFold2 is getraind om te voorspellen hoe een keten aminozuren vouwt tot een driedimensionaal eiwit, niet om te vinden waar geneesmiddelen binden. In het leren vouwen van eiwitten heeft het echter ook rijke patronen geleerd over hoe verschillende delen van eiwitten met elkaar interageren. AF2BIND benut één van deze interne datalagen, de zogenaamde pair-representatie, die vastlegt hoe elk paar aminozuurposities ruimtelijk met elkaar samenhangt. De auteurs voeren aan AlphaFold2 een eiwitsequentie samen met de ruggengraatstructuur toe en voegen daarnaast 20 extra aminozuren toe, één van elk type, als aparte “aas”ketens. AlphaFold2 berekent vervolgens hoe het eiwit met elk aasresidu interacteert. Deze interactiepatronen vormen de invoer voor een zeer eenvoudige logistische regressiemodel dat voor iedere positie in het eiwit de waarschijnlijkheid schat dat het tot een kleine-molecuul bindingsplaats behoort.
Verborgen signalen omzetten in praktische voorspellingen
Het trainen van AF2BIND vergde een zorgvuldig geselecteerde set van ongeveer 1.900 eiwit–ligandstructuren waarbij kleine moleculen met hoogwaardige experimentele bewijzen waren gebonden. De onderzoekers deden veel moeite om ‘‘valsspelen’’ door gelijkenis te voorkomen: zij splitsten hun data zodat testeiwitten geen gemeenschappelijke vouw, sequentie of zelfs bindingszakvorm deelden met de trainingsset. Op deze rigoureuze benchmark overtrof de AF2 pair-representatie verschillende alternatieve neurale-netwerk-embeddings, inclusief die alleen op sequentie of op structuur-geconditioneerde sequentieontwerp waren gebaseerd. Met alleen de pair-features herstelde AF2BIND ongeveer tweederde van de bekende bindende residuen in de hoogst gerangschikte voorspellingen en liet het sterke prestaties zien over standaard classificatiemaatstaven, terwijl het robuust bleef tegen beperkte veranderingen in eiwitvorm en zijketenoriëntaties.
Chemische aanwijzingen lezen vanuit aasresiduen
Aangezien AF2BIND een simpel lineair model is, zijn de beslissingen uitzonderlijk transparant voor een modern AI-systeem. Elk van de 20 aasaminozuren levert een meetbare bijdrage aan de uiteindelijke bindingsscore op een gegeven eiwitpositie. Door deze bijdragen te onderzoeken in ongeveer 2.000 eiwit–ligandcomplexen vonden de auteurs dat bepaalde aascombinaties sterker aanspringen voor vette, koolstofrijke liganden, terwijl andere juist oplichten voor meer polaire, watervriendelijke moleculen. Met andere woorden: het patroon van aasactivatie functioneert als een grove chemische vingerafdruk van welke soorten kleine moleculen een bepaalde pocket verkiest. Dit suggereert dat AF2BIND-achtige benaderingen in de toekomst niet alleen kunnen aangeven waar een medicijn zou kunnen binden, maar ook kunnen suggereren welke soort chemie het beste zou passen.
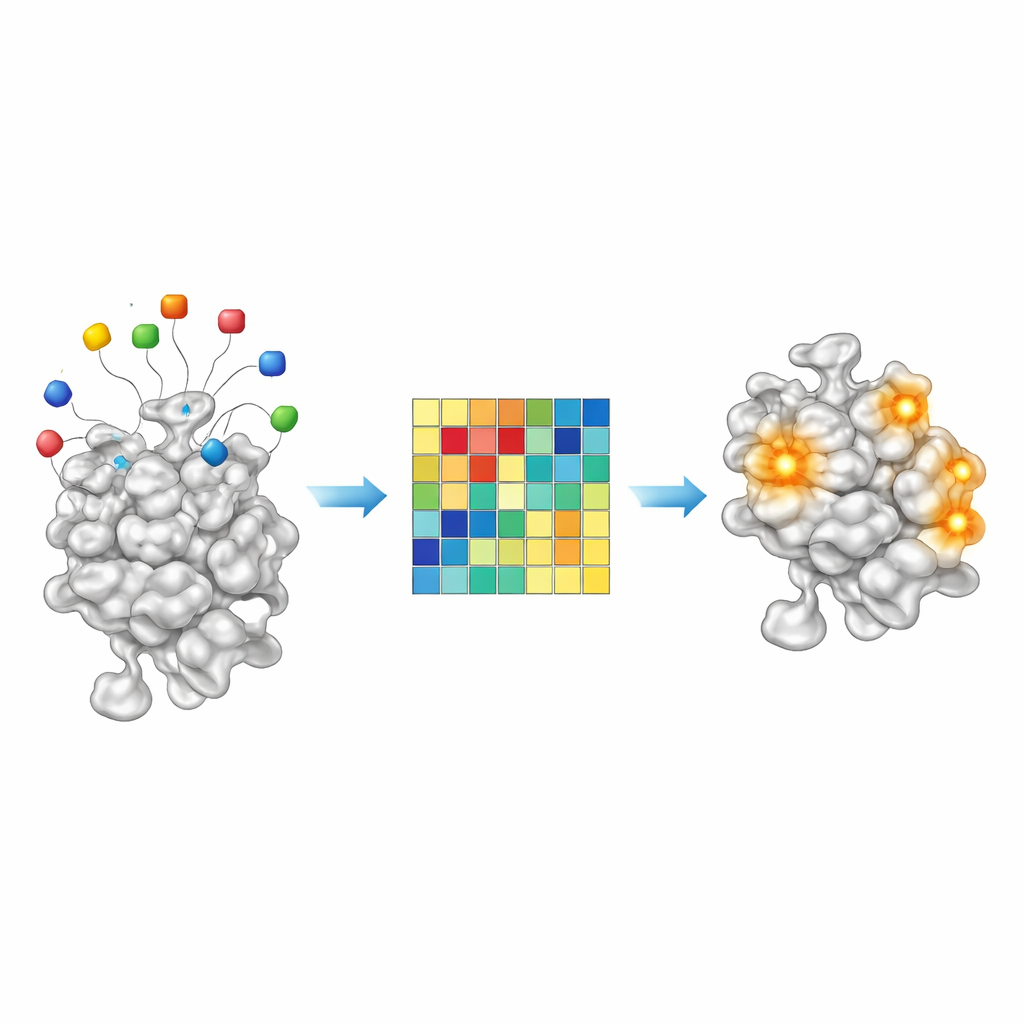
De menselijke proteoom scannen op nieuwe pockets
Gewapend met hun getrainde model zette het team AF2BIND vervolgens in op de AlphaFold-voorspelde structuren van het volledige menselijke proteoom. Na het wegknippen van lage-vertrouwensregio’s en het splitsen van zeer grote eiwitten in hanteerbare structurele stukken, groepeerden zij nabijgelegen hooggescoorde residuen tot kandidaat-bindingsplaatsen. AF2BIND voorspelde meer dan 20.000 zulke sites in meer dan 13.000 eiwitten. Opvallend was dat het merendeel hiervan niet samenviel met pockets afgeleid via homologie-gebaseerde methoden zoals AlphaFill, die liganden kopiëren uit verwante kristalstructuren, noch met een veelgebruikt pocket-finding gereedschap genaamd P2Rank. Veel AF2BIND-only sites zijn ondieper of diffuser dan klassieke verzonken pockets en vallen vaak samen met regio’s die peptiden, RNA, DNA of andere eiwitten binden — interfaces die desalniettemin door kleine moleculen te targeten kunnen zijn.
Gevolgen voor geneesmiddelenontwikkeling en ziekte
Om te beoordelen hoe veelbelovend deze nieuw gesuggereerde sites voor medicijnontwerp zouden kunnen zijn, gebruikten de auteurs een onafhankelijk hulpmiddel dat ‘‘drugbaarheid’’ scoort op basis van pocketgrootte, omsluiting en chemische omgeving. Gemiddeld scoorden de AF2BIND-sites boven een gebruikelijke drempel voor aantrekkelijke geneesmiddendoelen, inclusief die gevonden in eiwitten die verband houden met erfelijke ziekten. Wanneer ze werden gekruist met chemoproteomische experimenten die reactieve cysteïnes in cellen labelen, verklaarden AF2BIND en P2Rank samen bijna de helft van de waargenomen ligandbare regio’s, waarbij elke methode gevallen ving die de andere miste. Het werk toont aan dat de interne representaties die structuur-voorspellende netwerken leren, kunnen worden hergebruikt om op enorme schaal waarschijnlijke geneesmiddelbindingsplaatsen in kaart te brengen, zonder voorafgaande kennis van een specifiek ligand. Voor niet-specialisten is de kernboodschap dat dezelfde AI-doorbraken die eiwitvormen voorspellen, beginnen te onthullen waar en hoe medicijnen die vormen het beste kunnen grijpen, waardoor de zoektocht naar nieuwe behandelingen kan versnellen en eerder verborgen controlepunten in onze eiwitten zichtbaar worden.
Bronvermelding: Gazizov, A., Lian, A., Goverde, C. et al. AF2BIND: predicting small-molecule binding sites using the pair representation of AlphaFold2. Nat Methods 23, 626–635 (2026). https://doi.org/10.1038/s41592-026-03011-2
Trefwoorden: eiwitbindingsplaatsen, geneesmiddelenontwikkeling, AlphaFold2, computationele biologie, structurele bio-informatica