Clear Sky Science · nl
MaAsLin 3: verfijnen en uitbreiden van gegeneraliseerde multivariabele lineaire modellen voor meta-omische associatieontdekking
Waarom die kleine bewoners van de darm ertoe doen
Ons lichaam herbergt biljoenen microben die helpen voedsel te verteren, het immuunsysteem te trainen en mogelijk zelfs onze stemming te beïnvloeden. Nu DNA-sequencing het eenvoudig heeft gemaakt deze microbiele gemeenschappen in kaart te brengen, is een cruciale vraag naar voren gekomen: welke specifieke microben gaan samen met ziekten zoals inflammatoire darmziekte, of met alledaagse kenmerken zoals leeftijd en dieet? Dat beantwoorden blijkt verrassend lastig. De gegevens zijn lawaaierig, zitten vol nullen en worden vaak als percentages gerapporteerd in plaats van als werkelijke aantallen. Dit artikel introduceert MaAsLin 3, een nieuw statistisch hulpmiddel dat is ontworpen om helderdere signalen uit rommelige microbioomgegevens te halen, zodat onderzoekers betrouwbaarder microben kunnen koppelen aan menselijke gezondheid en het milieu.
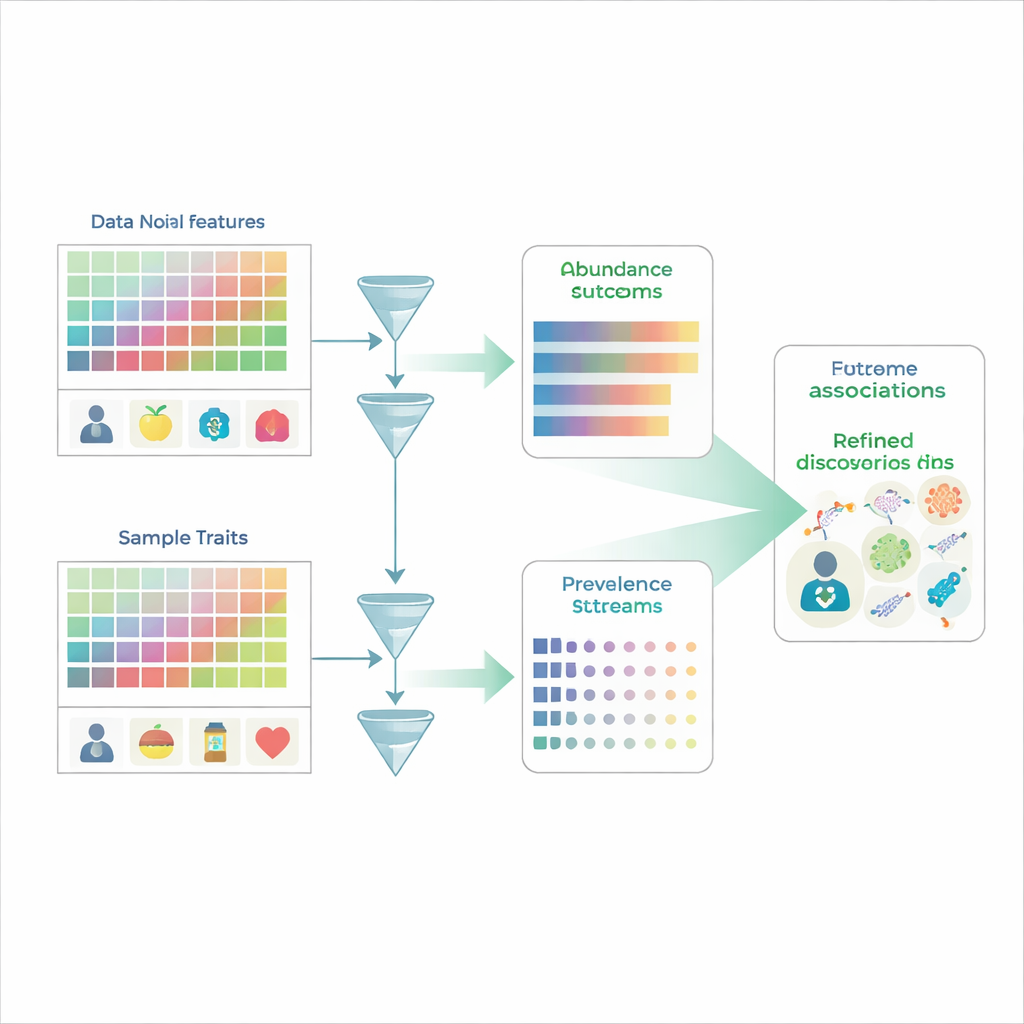
Patronen zoeken in een rumoerige menigte
Traditionele microbioomstudies werken een beetje als het tellen van gezichten in een menigte: onderzoekers meten de relatieve abundanties van honderden of duizenden microbiele soorten over veel mensen en vragen vervolgens welke soorten verschillen tussen bijvoorbeeld zieke en gezonde groepen. Maar microbioomgegevens zijn beperkt tot percentages die samen 100% moeten vormen, dus als één soort toeneemt, lijkt minstens één andere soort te dalen, zelfs als de werkelijke hoeveelheid daarvan niet veranderd is. Daarbovenop worden veel soorten in een bepaald monster simpelweg niet gedetecteerd, wat veel nullen oplevert die zowel ware afwezigheid als detectielimieten kunnen weerspiegelen. Gangbare analysemethoden verwarren doorgaans twee verschillende vragen—of een microbe überhaupt aanwezig is, en hoeveel ervan aanwezig is als hij er wel is—waardoor het makkelijk wordt de onderliggende biologie verkeerd te interpreteren.
Aanwezigheid scheiden van hoeveelheid
MaAsLin 3 pakt deze problemen aan door aanwezigheid en hoeveelheid uitdrukkelijk als aparte maar gerelateerde verschijnselen te behandelen. Voor elk microbiëel kenmerk—zoals een soort, gen of metabool pad—bouwt het twee modellen parallel. Het ene model kijkt naar prevalentie en vraagt hoe vaak het kenmerk wordt gedetecteerd in monsters met verschillende eigenschappen. Het andere model richt zich op abundanties en onderzoekt hoe het niveau van het kenmerk verandert binnen alleen die monsters waarin het wordt gedetecteerd. Door de gegevens op deze manier te splitsen, vermijdt MaAsLin 3 de gebruikelijke snelle oplossing om nullen op te vullen met willekeurig kleine getallen, wat resultaten kan vertekenen. Het combineert vervolgens de twee effecten tot een totaalbeeld van hoe elk kenmerk zich verhoudt tot elk kenmerk, terwijl onderzoekers toch kunnen zien of een associatie vooral over aanwezigheid, hoeveelheid of beide gaat.
Dichter bij echte hoeveelheden komen
Een aanvullende complicatie in de microbiële wetenschap is dat de meeste metingen relatief zijn: ze vertellen welk aandeel van de totale gemeenschap een soort inneemt, niet hoeveel cellen er daadwerkelijk zijn. Toch hangen biologische vragen vaak af van absolute abundanties—bijvoorbeeld of het aantal cellen van een pathogeen een drempel overschrijdt die ziekte kan veroorzaken. MaAsLin 3 biedt twee complementaire oplossingen. Wanneer experimenten extra informatie bevatten, zoals bekende hoeveelheden van een referentie-organisme of schattingen van de totale microbiële belasting, kan de methode relatieve percentages omzetten in schattingen van absolute aantallen en die direct modelleren. Wanneer zulke data niet beschikbaar zijn, vergelijkt MaAsLin 3 in plaats daarvan het gedrag van elk kenmerk met het typische patroon over alle kenmerken, wat onder realistische aannames benadert wat op een absolute schaal te zien zou zijn. Uitgebreide computersimulaties en tests op echte datasets met experimenteel gemeten absolute abundanties tonen aan dat deze strategie onderliggende trends nauwkeurig herstelt en beter presteert dan verschillende veelgebruikte hulpmiddelen.
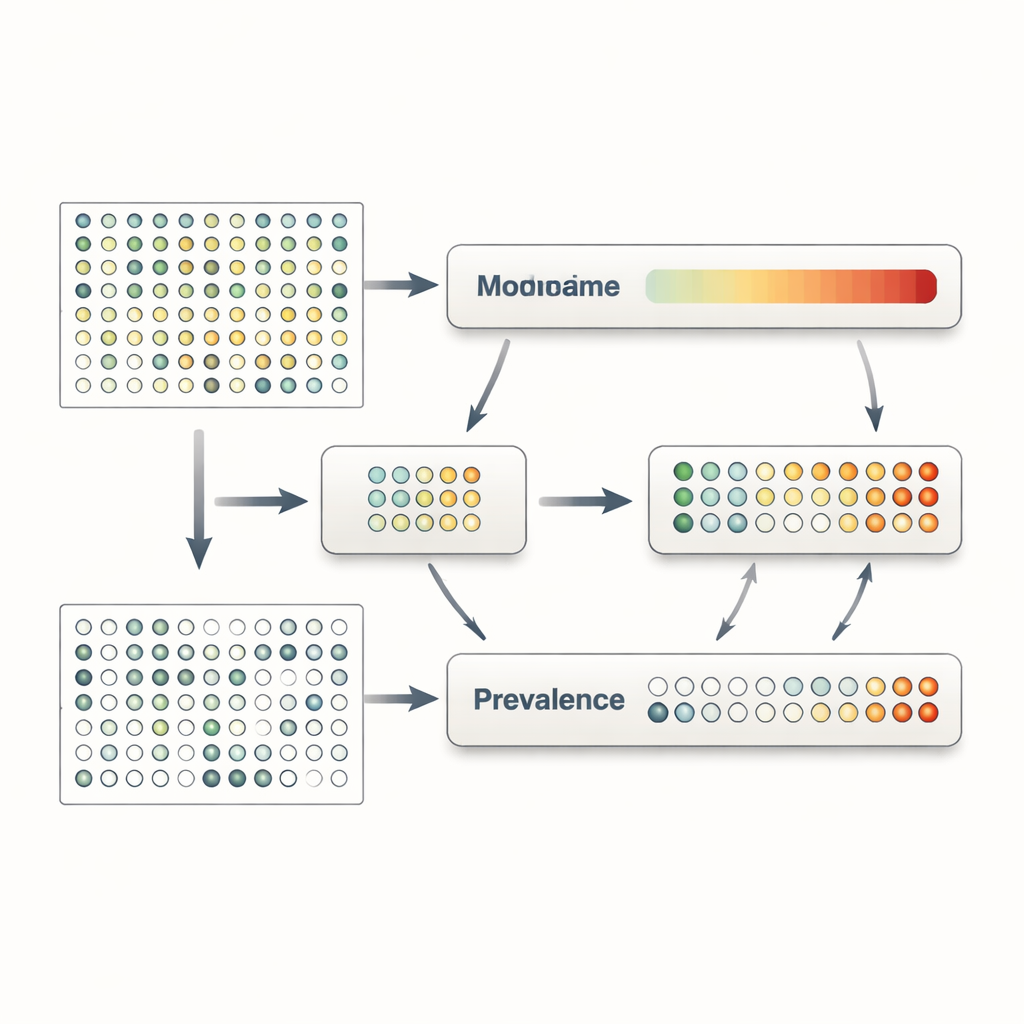
Verborgen signalen in darmaandoeningen onthullen
Om te laten zien wat deze verbeteringen in de praktijk betekenen, pasten de auteurs MaAsLin 3 toe op een grote, goed bestudeerde cohorte van mensen met en zonder inflammatoire darmziekten zoals de ziekte van Crohn en colitis ulcerosa. Eerder onderzoek had al veel microbiële veranderingen in deze aandoeningen geïdentificeerd, maar MaAsLin 3 voegde meerdere lagen nuance toe. Het bevestigde de meeste bekende verbanden en verduidelijkte dat ongeveer driekwart van de associaties te maken had met veranderingen in of microben überhaupt aanwezig waren, in plaats van met hoeveel ze aanwezig waren wanneer ze voorkwamen. Met andere woorden, darmontsteking ging vaak samen met het volledig verdwijnen van bepaalde nuttige microben of het niet detecteren ervan, in plaats van slechts een milde afname in hun niveaus. De methode liet ook microben zien waarvan de aanwezigheid op zichzelf—ongeacht de hoeveelheid—sterk samenhing met ziektegerelateerde verstoring van de darmgemeenschap.
Wat dit betekent voor toekomstige studies en zorg
Voor niet-specialisten is de kernboodschap dat de manier waarop we microbioomgegevens analyseren sterk kan bepalen welke microben we belangrijk achten voor de gezondheid. Door beter met nullen om te gaan, aanwezigheid van hoeveelheid te scheiden en reële celgetallen te benaderen, biedt MaAsLin 3 een scherper instrumentarium voor het ontdekken van betrouwbare microbiële markers van ziekte, dieet en milieu. De resultaten bij inflammatoire darmziekte suggereren dat veel klinisch relevante verschuivingen te maken hebben met microben die verdwijnen of nieuw verschijnen, en niet alleen met soorten die geleidelijk in abundanties omhoog of omlaag bewegen. Dit onderscheid is belangrijk voor het ontwerpen van therapieën: als ziekte gekoppeld is aan het volledig verlies van nuttige soorten, zijn strategieën die deze microben herintroduceren of beschermen mogelijk effectiever dan benaderingen die alleen proberen de algemene gemeenschapsbalans te verschuiven. MaAsLin 3 rust onderzoekers dus uit met een preciezer en flexibeler gereedschap om complexe microbioommetingen om te zetten in bruikbare biologische inzichten.
Bronvermelding: Nickols, W.A., Kuntz, T., Shen, J. et al. MaAsLin 3: refining and extending generalized multivariable linear models for meta-omic association discovery. Nat Methods 23, 554–564 (2026). https://doi.org/10.1038/s41592-025-02923-9
Trefwoorden: microbioom, inflammatoire darmziekte, statistische modellering, absolute abundantie, microbiële prevalentie