Clear Sky Science · nl
Massale toediening van azitromycine en antibioticaresistentie in darm en nasofarynx: een clustergemedieerd gerandomiseerd onderzoek
Waarom één pil aan veel kinderen geven ertoe doet
In delen van West-Afrika is één antibioticum, azitromycine, in massale campagnes gebruikt om het aantal jonge kinderen dat aan infecties sterft te verminderen. De strategie werkt — maar ze wekt een ernstige zorg: kweken we stilletjes sterkere, medicijnresistente ziekteverwekkers in de lichamen van kinderen? Deze studie, uitgevoerd in honderden dorpen in Niger, kijkt nauwkeurig in de darmen en neuzen van kinderen om te zien hoe herhaalde behandeling van hele gemeenschappen hun verborgen microbieel landschap en antibioticaresistentie verandert.
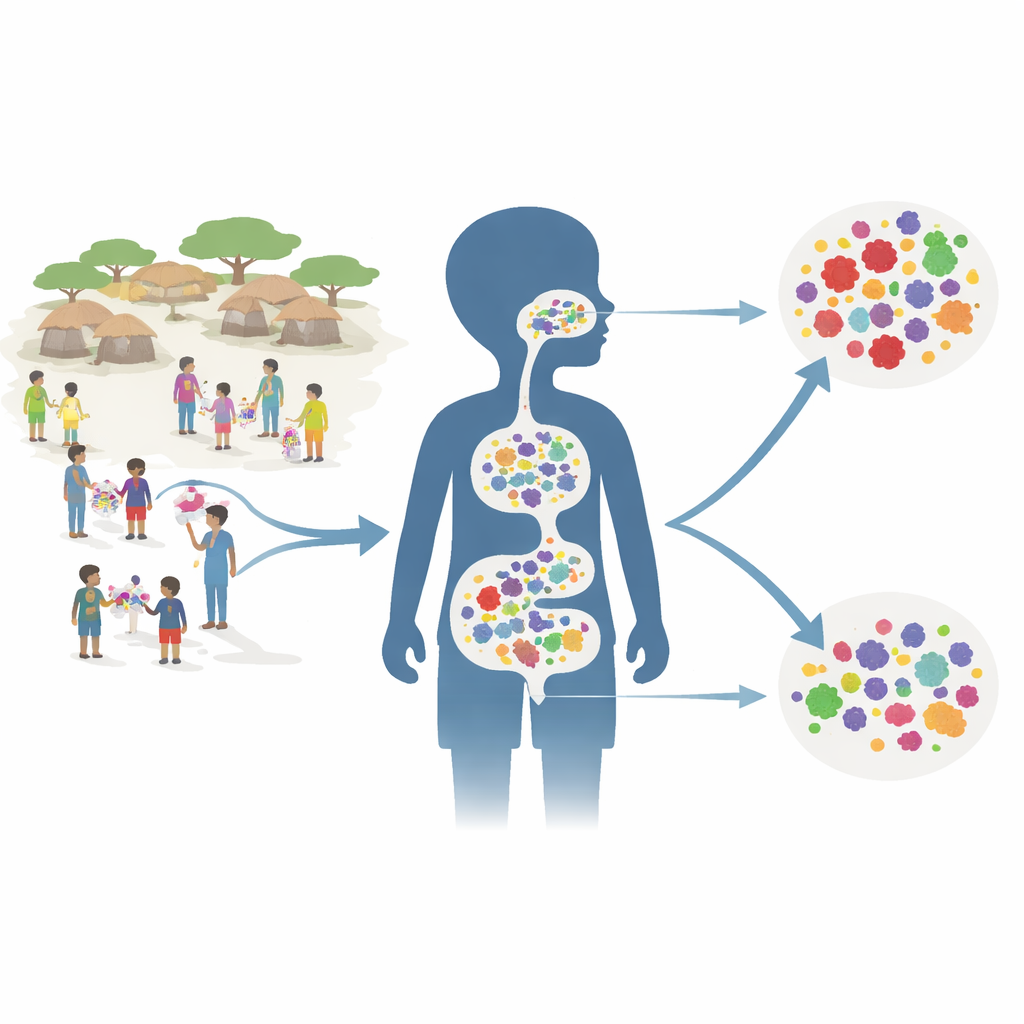
Een gemeenschapsbreed medicijnplan testen
Onderzoekers plaatsten hun werk binnen een groot onderzoek genaamd AVENIR, dat al had aangetoond dat het elke zes maanden toedienen van azitromycine aan alle kinderen van 1 tot 59 maanden de sterfte in deze leeftijdsgroep kon verlagen. Voor de resistentiestudie richtten ze zich op 150 toevallig gekozen dorpen. Elk dorp hoorde bij één van drie groepen: alle jonge kinderen kregen azitromycine; alleen zuigelingen tot 11 maanden kregen azitromycine terwijl oudere peuters en kleuters placebo kregen; of alle kinderen kregen placebo. Twee jaar na aanvang — zes maanden na de vierde behandelingsronde — verzamelde het team rectale en diepe neusswabs van ongeveer 30 kinderen per dorp.
Kijken in darm en neus
In plaats van ziekteverwekkers in het laboratorium te kweken, poolden de wetenschappers de monsters per dorp en gebruikten moderne DNA-sequencing. Daarmee konden ze in kaart brengen welke bacteriën aanwezig waren en genetische markers tellen die wijzen op resistentie tegen verschillende antibioticaklassen. Ze besteedden bijzondere aandacht aan macroliden — de geneesmiddelfamilie waartoe azitromycine behoort — en scanden ook op resistentie tegen veel andere veelgebruikte antibiotica, zoals penicilline-achtige middelen. De darm en de nasofarynx (het bovenste deel van de keel achter de neus) werden onderzocht omdat beide belangrijke reservoirs zijn waar resistentiegenen zich kunnen ophopen en mogelijk verspreiden.
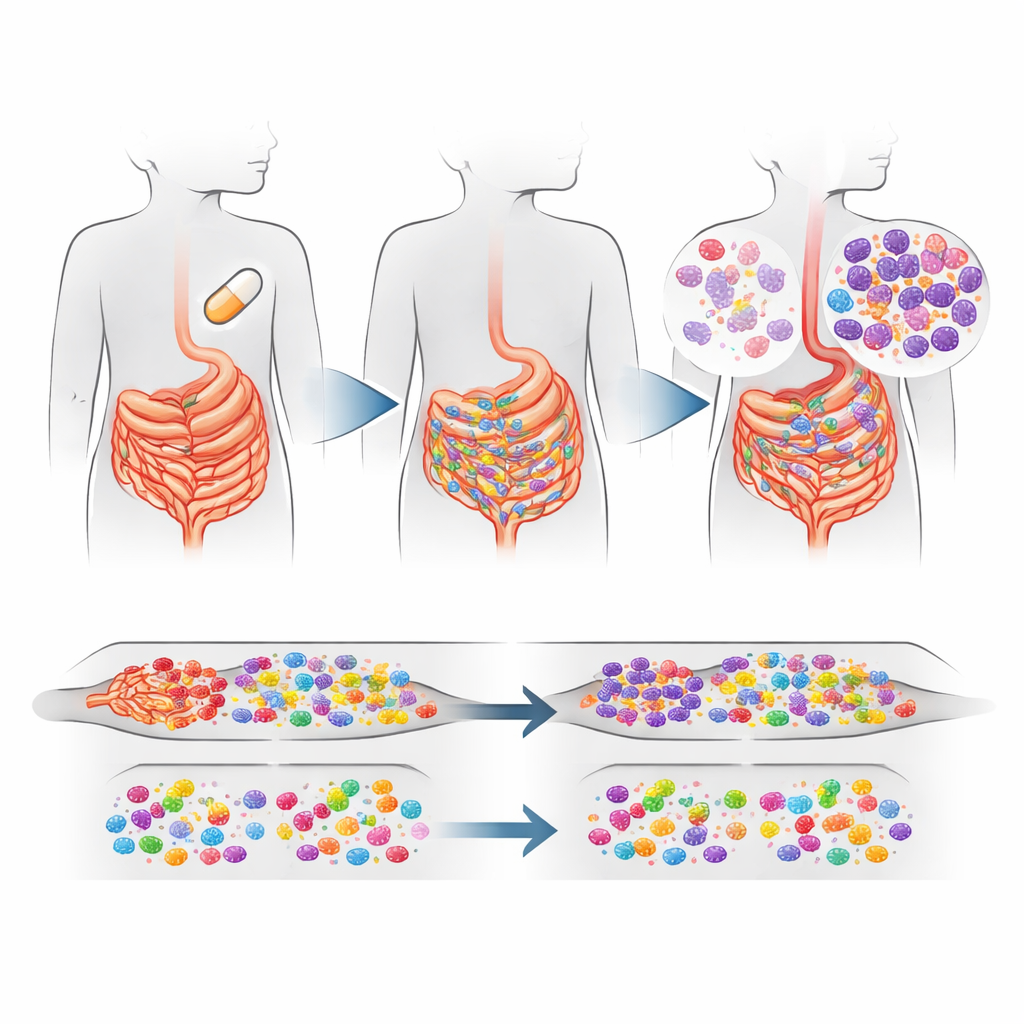
Wat er in de darmen van kinderen veranderde
Het duidelijkste signaal kwam uit de darm. Dorpen waar alle kinderen azitromycine kregen, hadden een bescheiden maar statistisch betrouwbare toename — ongeveer 16% hoger in totaal — van macrolide-resistentiegenen in darmbacteriën vergeleken met placebodorpen. De stijging werd grotendeels gedreven door één resistentiegen, genoemd ermF, dat bacteriën helpt beschermen tegen macrolidegeneesmiddelen. Dit gen wordt vaak gedragen door veelvoorkomende darmbacteriën zoals Bacteroides en Prevotella, die gewoonlijk onschadelijk in de darmen leven maar soms ziekte kunnen veroorzaken. Interessant genoeg namen resistentiegenen tegen andere belangrijke antibioticafamilies niet toe, en de algemene samenstelling en diversiteit van darmbacteriën leken in grote lijnen vergelijkbaar tussen behandelingsgroepen, hoewel sommige specifieke soorten meer of minder voorkwamen.
Wat hetzelfde bleef in de neus
De neuspassages vertelden daarentegen een rustiger verhaal. De studie vond geen duidelijke, statistisch sterke verschillen in macrolide-resistentiegenen tussen behandelingsgroepen in de nasofarynx, noch bewijs dat resistentie tegen andere antibiotica daar werd geselecteerd. De gebruikelijke neusresidenten — geslachten zoals Moraxella, Haemophilus en Streptococcus — bleven dominant. Enkele mondgerelateerde bacteriën die met tandvleesziekte geassocieerd zijn, kwamen vaker voor in met azitromycine behandelde gemeenschappen, en sommige daarvan kunnen ook resistentiegenen dragen, maar de totale resistentielast in de neus verschuift niet op dezelfde manier als in de darm.
De balans tussen hedendaagse winst en risico’s voor morgen
Samengevoegd tonen de bevindingen aan dat het geven van azitromycine aan alle jonge kinderen in een gemeenschap levens kan redden, maar dat het ook de darmbacteriën subtiel in de richting van grotere resistentie tegen deze geneesmiddelfamilie duwt, hoofdzakelijk door de expansie van specifieke resistentiegenen zoals ermF. In het tweejarige venster zag de studie geen overslaan naar resistentie tegen andere antibiotica, noch sterke veranderingen in het nasale reservoir, maar de auteurs waarschuwen dat resistente darmbacteriën en hun genen zich in de loop van de tijd en tussen mensen kunnen verspreiden. Zij pleiten ervoor dat ieder breed antibioticaprogramma voor kinderoverleving zorgvuldige, langetermijnmonitoring van resistentie moet inbouwen, zodat gezondheidsinstanties het directe voordeel van minder kindersterfte kunnen blijven afwegen tegen de langzamere, minder zichtbare kost van het versterken van medicijnresistente microben.
Bronvermelding: Doan, T., Yan, D., Arzika, A.M. et al. Mass azithromycin distribution and antibiotic resistance in the gut and nasopharynx: a cluster-randomized trial. Nat Med 32, 859–868 (2026). https://doi.org/10.1038/s41591-026-04217-9
Trefwoorden: azitromycine, kindersterfte, antibioticaresistentie, darmmicrobioom, massale geneesmiddeltoediening