Clear Sky Science · nl
Single-cellatlas van de zich ontwikkelende cortex bij het syndroom van Down
Waarom dit onderzoek ertoe doet
Het syndroom van Down is de meest voorkomende genetische oorzaak van verstandelijke beperkingen, maar we weten nog steeds weinig over hoe het de zich ontwikkelende menselijke hersenen vóór de geboorte verandert. Deze studie zoomt in tot op het niveau van individuele cellen in de foetale cortex — het hersengebied dat cruciaal is voor denken en geheugen — om in kaart te brengen wat er misgaat, wanneer het begint en welke moleculaire schakelaars mogelijk kunnen worden aangestuurd om te helpen.
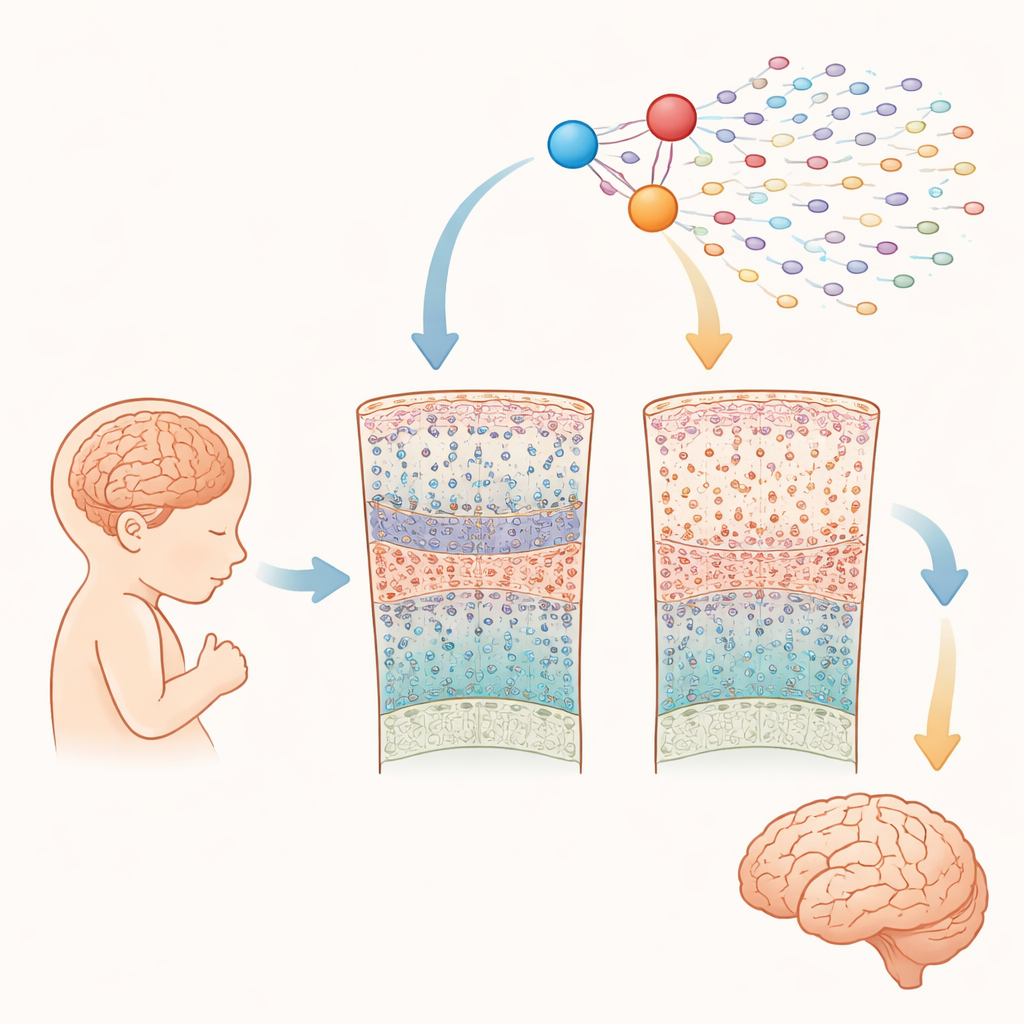
Nauwkeurige blik op de groeiende hersenen
De onderzoekers analyseerden bijna een kwart miljoen cellen afkomstig uit de cerebrale cortex van 15 foetussen met het syndroom van Down en 15 zonder, tussen 10 en 20 weken na conceptie. Met geavanceerde "single-cell" methoden maten ze zowel welke genen waren aangezet als hoe toegankelijk het DNA in elke cel was. Hierdoor konden ze alle belangrijke celtypen identificeren die in dit midden-zwangerschapsstadium aanwezig zijn — zoals stamachtige progenitorcellen, verschillende soorten exciterende en remmende neuronen en vroege gliacellen — en hun abundanties en genactiviteit tussen Downsyndroom- en typische hersenen vergelijken.
Vroege veranderingen in sleutelcellen voor denken
De meeste brede celklassen waren in vergelijkbare aantallen aanwezig in beide groepen tijdens dit vroege venster. Toch vond het team een opvallend en selectief tekort aan één specifiek type exciterend neuron dat normaal gesproken laag 4 van de cortex bezet en belangrijk is voor het verwerken van binnenkomende informatie. Deze neuronen worden gekenmerkt door eiwitten genaamd RORB en FOXP1. Bij foetussen met het syndroom van Down waren RORB–FOXP1-neuronen al verminderd rond mid-gestatie, met name tussen 16 en 20 weken, terwijl andere neuronale typen relatief gespaard leken. Dit suggereert dat problemen bij de generatie of rijping van deze subpopulatie al in utero beginnen en mogelijk direct bijdragen aan latere cognitieve moeilijkheden.
Verstoorde genetische programma’s en hoofdschakelaars
Verder dan celgetallen onthulde de studie dat honderden genen subtiel verkeerd gereguleerd waren, vooral in exciterende neuronen en hun progenitoren. Veel van deze genen zijn betrokken bij het bouwen van de voorhersenen, het vormen van dendritische takken, het leggen van verbindingen en het ondersteunen van hogere hersenfuncties. In plaats van dat alleen de extra kopieën van ruwweg 200 genen op chromosoom 21 verantwoordelijk zijn, wijzen de gegevens op een verstoord netwerk van genregulatie. Met een aanpak die genactiviteit combineert met DNA-toegankelijkheid brachten de auteurs regulerende circuits in kaart en lichtten drie transcriptiefactoren — BACH1, PKNOX1 en GABPA — die op chromosoom 21 gecodeerd zijn, uit als dosisgevoelige "hubs." Deze moleculen lijken andere kritische regelaars van corticale ontwikkeling te beïnvloeden, waaronder factoren die al in verband zijn gebracht met verstandelijke beperkingen, en helpen verklaren hoe een bescheiden 1,5-voudige toename in gen-dosering door hele ontwikkelingsprogramma’s kan golven.
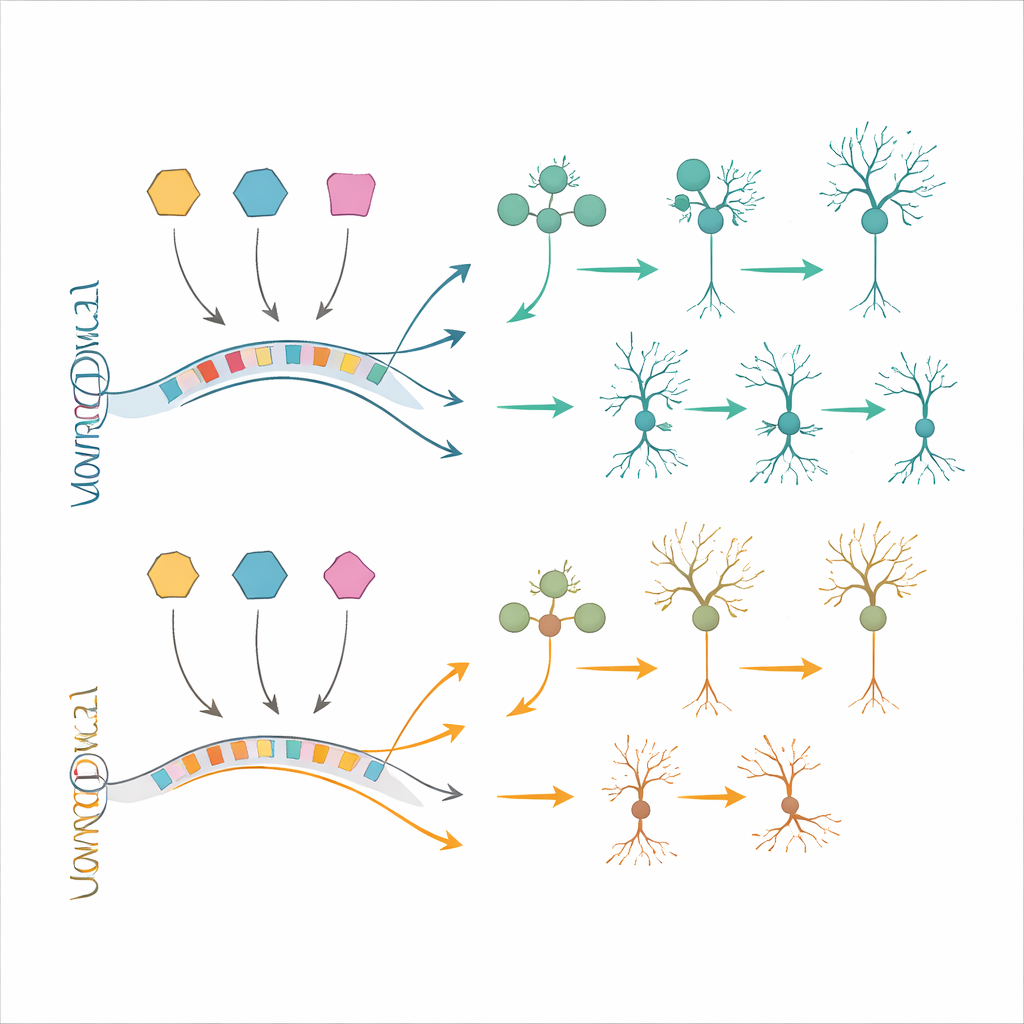
Testen van herstelstrategieën in cellen en levende hersenen
Om te onderzoeken of deze moleculaire veranderingen gecorrigeerd konden worden, gebruikte het team stamcelmodellen. Ze genereerden neurale progenitorcellen en neuronen uit geïnduceerde pluripotente stamcellen met trisomie 21 en uit bijpassende controlecellen. Veel van de genexpressieveranderingen die in foetaal weefsel werden gezien, verschenen opnieuw in deze in het lab gekweekte cellen, wat de relevantie van de modellen bevestigt. De onderzoekers gebruikten vervolgens antisense-oligonucleotiden — korte strengs ontworpen DNA-achtige molecule — om BACH1, PKNOX1 of GABPA terug te brengen naar normale niveaus. Deze gedeeltelijke normalisatie van de overgeëxprimeerde transcriptiefactoren leidde tot gedeeltelijk herstel van meerdere downstream-genen, waaronder genen die bekend zijn betrokken bij verstandelijke beperkingen en neuronale differentiatie. In een aanvullende benadering transplantieerden ze menselijke trisomie 21 neurale cellen in muizenhersenen en lieten die in vivo rijpen. Deze ingrepen reproduceerden extra Downsyndroom-achtige kenmerken, zoals een veranderde neuron–glia-balans en genveranderingen die niet volledig in kweek worden vastgelegd, en bieden daarmee een krachtig testveld voor toekomstige therapieën.
Wat dit betekent voor de toekomst
Samengevoegd levert dit werk een gedetailleerde atlas van hoe het syndroom van Down het genetische landschap van de zich ontwikkelende cortex vormt op single-cell resolutie. Voor de algemene lezer is de kernboodschap dat het extra chromosoom niet simpelweg een paar uitschietende genen toevoegt; het verschuift veel onderling verbonden moleculaire schakelaars, wat leidt tot vroege en selectieve tekorten aan bepaalde denkgerelateerde neuronen. Door een klein aantal transcriptiefactoren op chromosoom 21 als centrale spelers aan te wijzen — en te laten zien dat hun effecten gedeeltelijk omkeerbaar zijn in menselijke cellen — opent de studie de deur naar meer gerichte strategieën gericht op het verbeteren van hersenontwikkeling en -functie bij het syndroom van Down.
Bronvermelding: Lattke, M., Tan, W.L., Sukumaran, S.K. et al. Single-cell atlas of the developing Down syndrome brain cortex. Nat Med 32, 1061–1072 (2026). https://doi.org/10.1038/s41591-026-04211-1
Trefwoorden: Syndroom van Down, foetale hersenontwikkeling, single-cell genomica, corticale neuronen, transcriptiefactoren