Clear Sky Science · nl
CD19 CAR-T-cellen voor therapieresistente auto-immuunziekten: de fase 1/2 CASTLE basket-studie
Waarom een eenmalige behandeling ertoe doet
Veel mensen met ernstige auto-immuunziekten leven op een draaistel van voortdurende medicatie: de ene opvlamming na de andere en toenemende bijwerkingen. Deze studie onderzoekt een radicaal ander idee: één enkele infusie van geherprogrammeerde immuuncellen gebruiken om het immuunsysteem te "herstarten", zodat het stopt met het aanvallen van het lichaam. Voor patiënten met ernstige lupus, verharding van de huid en organen, of spierontsteking die geen opties meer hebben, zou zo’n reset langdurige verlichting kunnen betekenen zonder dagelijkse medicatie.
Drie lastige ziekten, één gemeenschappelijk probleem
Systemische lupus erythematosus, systemische sclerose en idiopathische inflammatoire myopathieën zien er aan de oppervlakte verschillend uit — ze treffen gewrichten, huid, longen, nieren of spieren — maar ze delen een kernfout: bepaalde immuuncellen, de B-cellen, schieten tekort en drijven chronische ontsteking aan. Standaardbehandelingen, van steroïden tot krachtige immunosuppressiva en antistofinfusies, kunnen symptomen kalmeren maar pakken zelden de onderliggende oorzaak aan. Veel patiënten doorlopen meerdere therapieën die slechts deels werken of onacceptabele bijwerkingen geven, wat leidt tot aanhoudende orgaanschade en een verminderde levenskwaliteit.
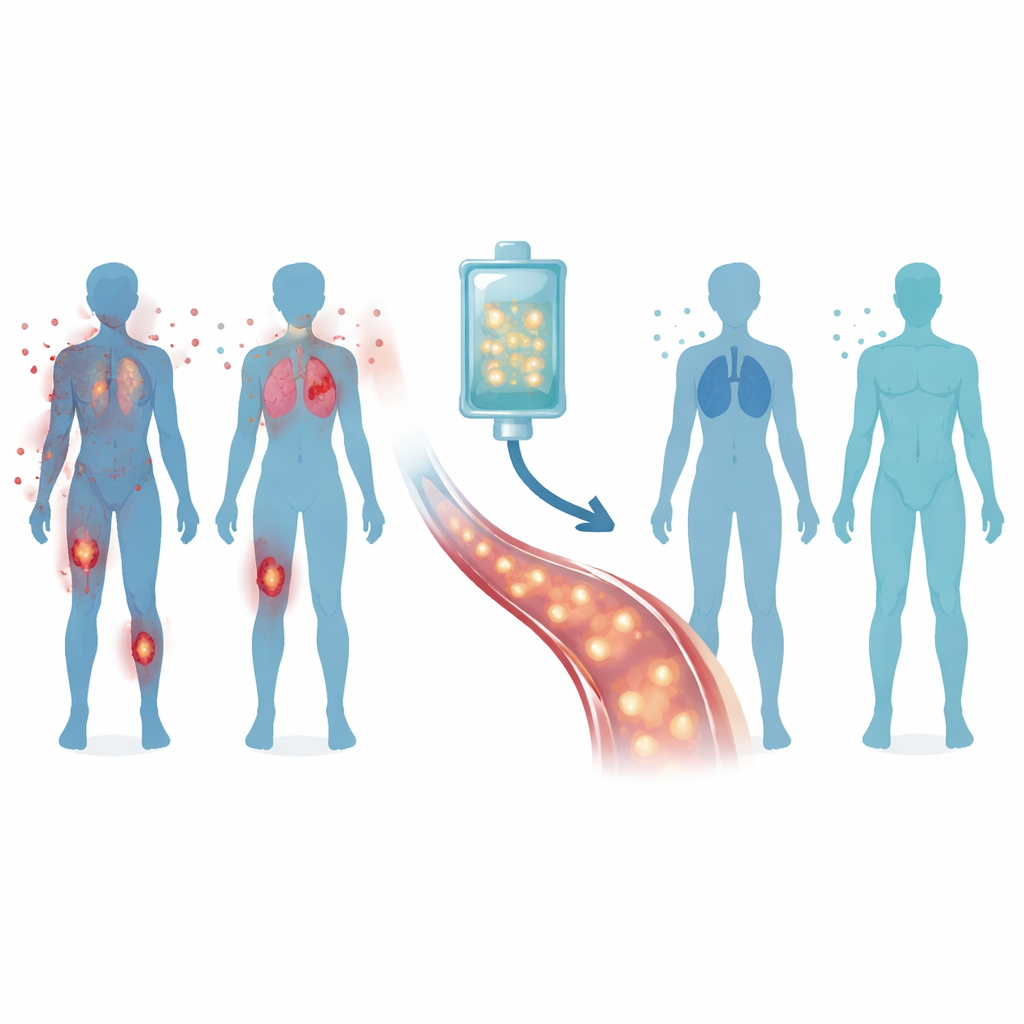
De verdedigers van het lichaam herprogrammeren
De CASTLE-studie testte een gepersonaliseerde celtherapie genaamd Zorpo-cel bij 24 volwassenen met ernstige, therapieresistente vormen van deze drie ziekten. Artsen verzamelden eerst de T-cellen van elke patiënt, de "soldaten" van het immuunsysteem, en voorzagen ze in het laboratorium van een nieuwe sensor — een chimerische antigeenreceptor — die een marker genaamd CD19 herkent die op de meeste B-cellen voorkomt. Na een korte kuur chemotherapie om ruimte te maken in het immuunsysteem, kregen patiënten één infusie van deze gemodificeerde cellen, bekend als CD19 CAR-T-cellen. De hoop was dat ze de slecht functionerende B-cellen zouden opsporen en verwijderen, zodat een gezondere populatie cellen terug kon groeien.
Veiligheid eerst, daarna tekenen van verlichting
Aangezien deze behandeling bij kankerpatiënten intens kan zijn, was het voornaamste doel van deze vroegfaseproef de veiligheid. De onderzoekers hielden nauwlettend toezicht op een gevaarlijke ontstekingsreactie, het cytokine release-syndroom, en op hersengerelateerde bijwerkingen. In CASTLE kreeg bijna driekwart van de patiënten alleen milde, kortdurende koorts en ontstekingsverschijnselen; er werden geen ernstige cytokinestormen, geen hersentoxiciteit en geen blijvende bloedcelproblemen waargenomen. De meest voorkomende problemen waren tijdelijke dalingen van witte bloedcellen en milde infecties, die met standaardzorg werden behandeld. Eén patiënt ontwikkelde nierletsel gerelateerd aan reactivatie van een virus en een opvlamming van de onderliggende ziekte, wat strengere regels opleverde om de ziekteactiviteit vóór infusie beter te beheersen.
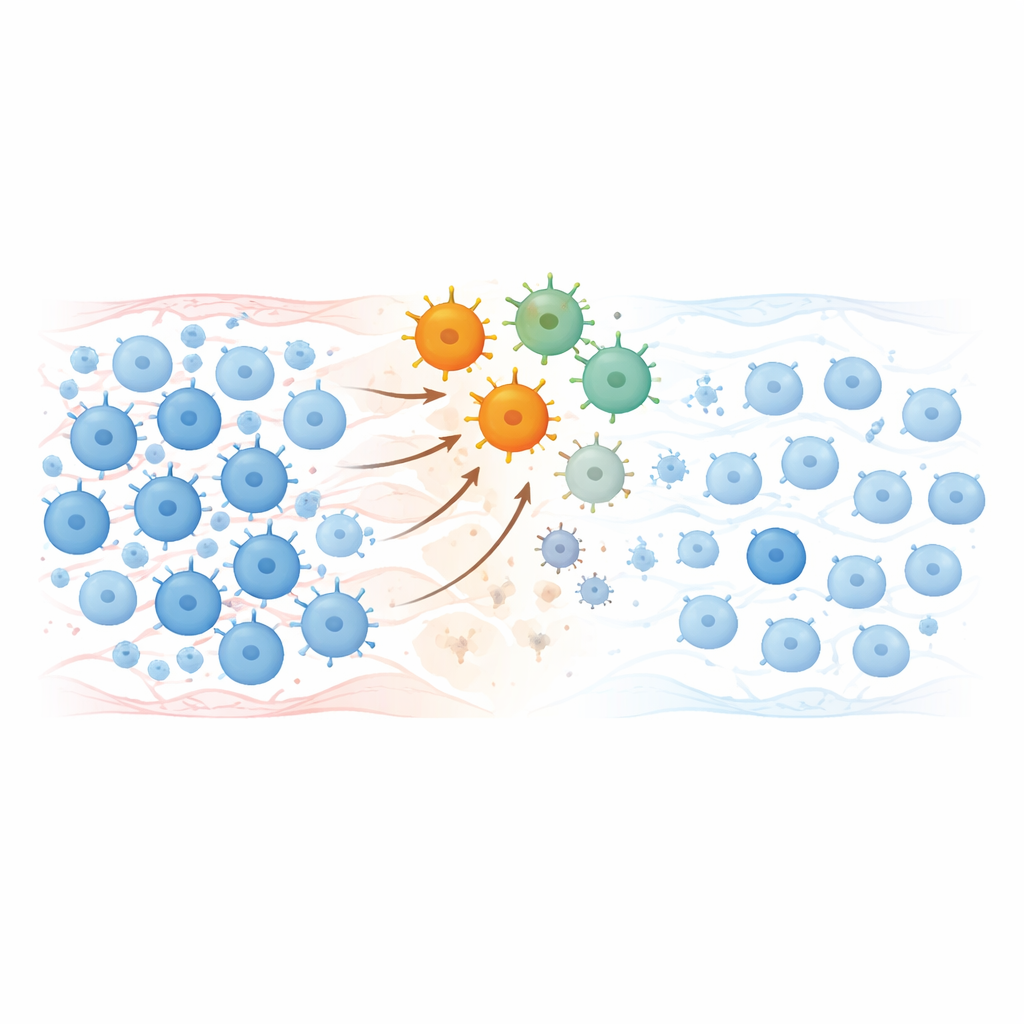
Het immuunsysteem resetten
Hoewel veiligheid de hoogste prioriteit had, waren de klinische verbeteringen opvallend. Na zes maanden voldeed 22 van de 24 patiënten aan vooraf bepaalde succescriteria, aangepast aan hun ziekte: de meeste lupuspatiënten bereikten een strikte remitteleer, alle systemische sclerosepatiënten hadden geen verslechtering van de longziekte en toonden verbeterde longfunctie en zachtere huid, en de meeste patiënten met spierontsteking kregen meer kracht en lagere spierenzymwaarden. Belangrijk is dat alle deelnemers konden stoppen met steroïden en andere immunosuppressiva en gedurende de zes maanden durende studie en daarna hiervan afbleven, zonder terugvallen tijdens een mediaan opvolginterval van ongeveer een jaar.
Wat er in het bloed gebeurt
Laboratoriumtests toonden aan dat de geïnfusioneerde CAR-T-cellen enkele dagen uitbreidden, circulerende B-cellen uitroeiden en vervolgens geleidelijk verdwenen over enkele maanden. Toen B-cellen later terugkeerden, zag hun populatie er anders uit: nagenoeg naïeve, "verse" cellen domineerden, terwijl geheugencellen en antistofproducerende voorlopercellen die vaak auto-immuun geheugen herbergen sterk waren verminderd. Veel schadelijke autoantistoffen daalden tot zeer lage of niet-detecteerbare niveaus, terwijl beschermende antilichamen van eerdere vaccinaties tegen infecties zoals mazelen of tetanus grotendeels behouden bleven, wat wijst op een gerichte reset in plaats van een volledige uitwissing van immuungeheugen.
Een glimp van een nieuw behandeltijdperk
Voor mensen met ernstige auto-immuunziekten leek het idee van een eenmalige behandeling die duurzame, medicijnvrije remissie brengt lange tijd onbereikbaar. Deze proef suggereert dat gemodificeerde T-cellen veilig afwijkende B-cellen in drie verschillende aandoeningen kunnen uitschakelen en het immuunsysteem wellicht in staat stellen opnieuw op te bouwen in een rustiger, minder zelfdestructieve staat. CASTLE is een vroege, relatief kleine studie, en grotere beslissende onderzoeken zijn nodig om te bevestigen hoe lang het voordeel aanhoudt en welke patiënten het meest profiteren. Toch wijst het op een toekomst waarin het resetten van het immuunsysteem — in plaats van het eindeloos onderdrukken ervan — een realistisch doel zou kunnen worden.
Bronvermelding: Müller, F., Hagen, M., Wirsching, A. et al. CD19 CAR-T cells for treatment-refractory autoimmune diseases: the phase 1/2 CASTLE basket trial. Nat Med 32, 1142–1151 (2026). https://doi.org/10.1038/s41591-025-04185-6
Trefwoorden: CAR-T-celtherapie, auto-immuunziekte, systemische lupus erythematosus, systemische sclerose, B-cellen