Clear Sky Science · nl
Humorale IgG1-responsen tegen tumooreiwitten onderbouwen klinische uitkomsten bij remming van immuuncheckpoints
Waarom dit belangrijk is voor kankerpatiënten
Immunotherapie heeft de kankerzorg veranderd door het eigen afweersysteem te helpen tumoren aan te vallen, maar alleen sommige patiënten profiteren ervan. De meeste aandacht ging uit naar één groep immuunstrijders — T-cellen — maar deze studie toont aan dat een andere groep, de antilichaamproducerende B-cellen, het verschil kan maken tussen succes en falen. Door aan te tonen hoe een specifiek type antilichaamrespons, IgG1 genoemd, samenhangt met betere uitkomsten, wijst het onderzoek op nieuwe manieren om te voorspellen wie baat heeft bij immunotherapie en hoe deze behandelingen voor meer mensen effectief gemaakt kunnen worden.
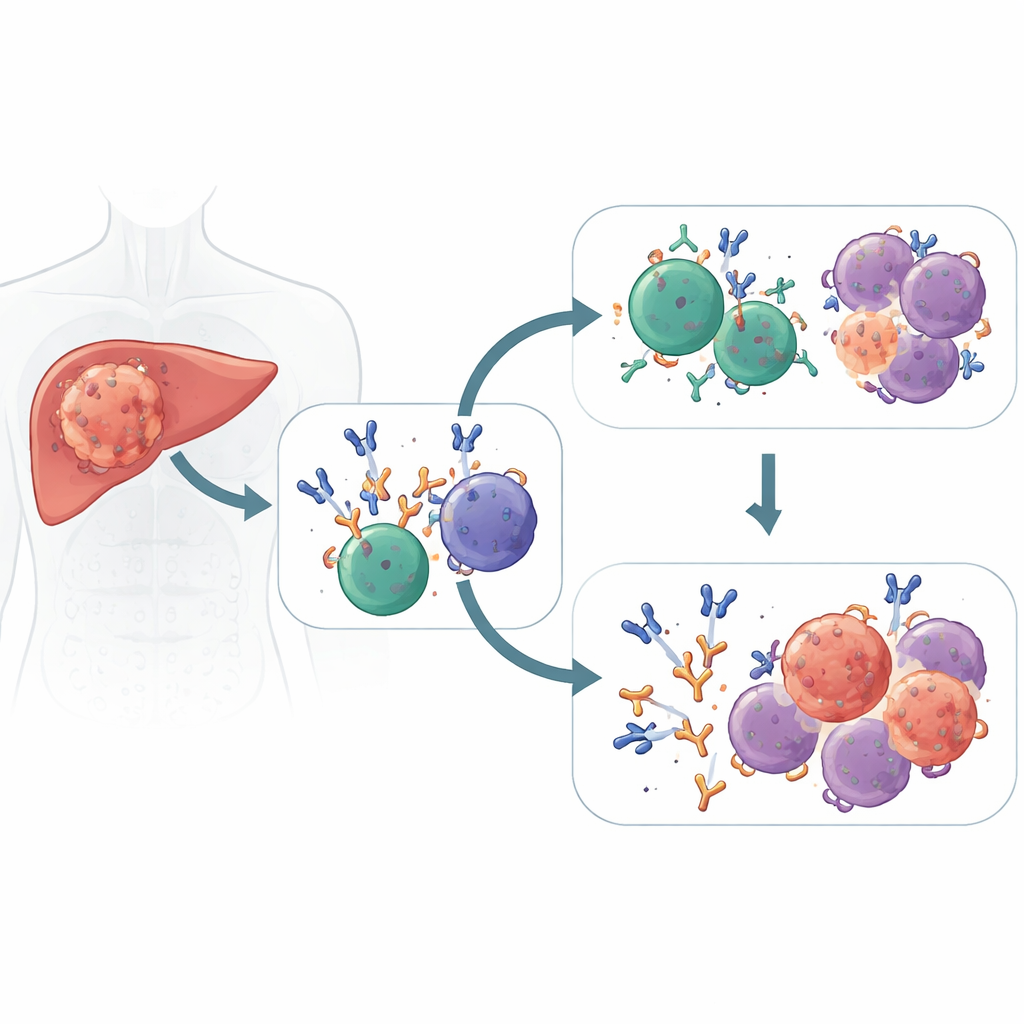
Twee verdedigingslinies die samenwerken
Moderne medicijnen, bekend als immuuncheckpointblokkers, halen de "rem" van T-cellen zodat zij kankercellen kunnen herkennen en doden. De onderzoekers bestudeerden mensen met leverkanker die deze middelen vóór de operatie kregen en ontdekten dat goede responders niet alleen op T-cellen vertrouwden. Hun tumoren zaten ook vol plasmacellen — rijpe B-cellen die functioneren als kleine antilichaamfabriekjes — die een dominante golf van IgG1-antilichamen produceerden gericht tegen kankertargets. Ter vergelijking: patiënten bij wie de tumor niet krimpte hadden meer inactieve of dysfuntionele B-cellen en minder van deze gespecialiseerde plasmacellen in hun tumoren.
Het antilichaamspoor volgen door het lichaam
Om te begrijpen waar deze nuttige plasmacellen vandaan komen combineerde het team single-cell sequencing met gedetailleerde tracking van de unieke antilichaam-"barcodes" die elke B-cel draagt. Ze vonden dat succesvolle patiënten families van nauw verwante IgG1-producerende cellen hadden die zowel in de tumor als in nabijgelegen lymfeklieren — de commandocentra van het immuunsysteem — uitdijnden. Dezelfde klonale signaturen waren vóór de behandeling aanwezig en namen daarna toe, wat aangeeft dat checkpointremming vooraf bestaande, tumorbewuste B-celklonen versterkt in plaats van volledig nieuwe te creëren. Dit suggereert een gecoördineerde circulatie van getrainde antilichaamproducenten tussen lymfeklieren en tumorlocaties.
Hoe antilichamen de tumoromgeving hervormen
Microscopische beeldvorming en ruimtelijke gen-mapping toonden dat plasmacellen bij responders niet aan de randen van de tumor bleven zitten — ze drongen diep in de kanker door samen met killer-T-cellen en behulpzame macrofagen. Deze regio’s waren rijk aan signalen die B-celactivatie en antilichaamproductie bevorderen, en vormden immuunnabijheden die geoptimaliseerd waren voor aanval. Non-responders daarentegen stapelden geheugenachtige B-cellen en regulerende immuuncellen op in vezelige stromale pockets die effectieve reacties dempten. In meerdere onafhankelijke patiëntengroepen en bij verschillende immunotherapiekombinaties markeerde een verschuiving naar IgG1-producerende plasmacellen consequent betere tumorcontrole en tragere ziekteprogressie.
Antilichamen die kankerspecifieke vlaggen herkennen
Aangezien plasmacellen antilichamen in de bloedbaan afscheiden, vroegen de onderzoekers zich af of deze moleculen in bloedmonsters gedetecteerd konden worden. Bij veel responders vonden ze hoge niveaus van IgG1-antilichamen gericht tegen zogenaamde cancer/testis-antigenen — eiwitten zoals NY-ESO-1 die normaal afwezig zijn in gezond weefsel maar opnieuw verschijnen in tumoren. Patiënten met deze antilichamen toonden vaker ook sterke T-celactiviteit tegen dezelfde targets, wat impliceert dat antilichamen helpen tumorfragmenten te presenteren aan de cellulaire tak van de immuniteit. Grote overlevingsdatasets van melanoom en longkanker bevestigden dat tumoren met sterke IgG1-signaturen geneigd zijn beter te reageren op checkpointmedicijnen, terwijl kankers die voornamelijk met standaardchemotherapie werden behandeld geen dergelijke relatie toonden.
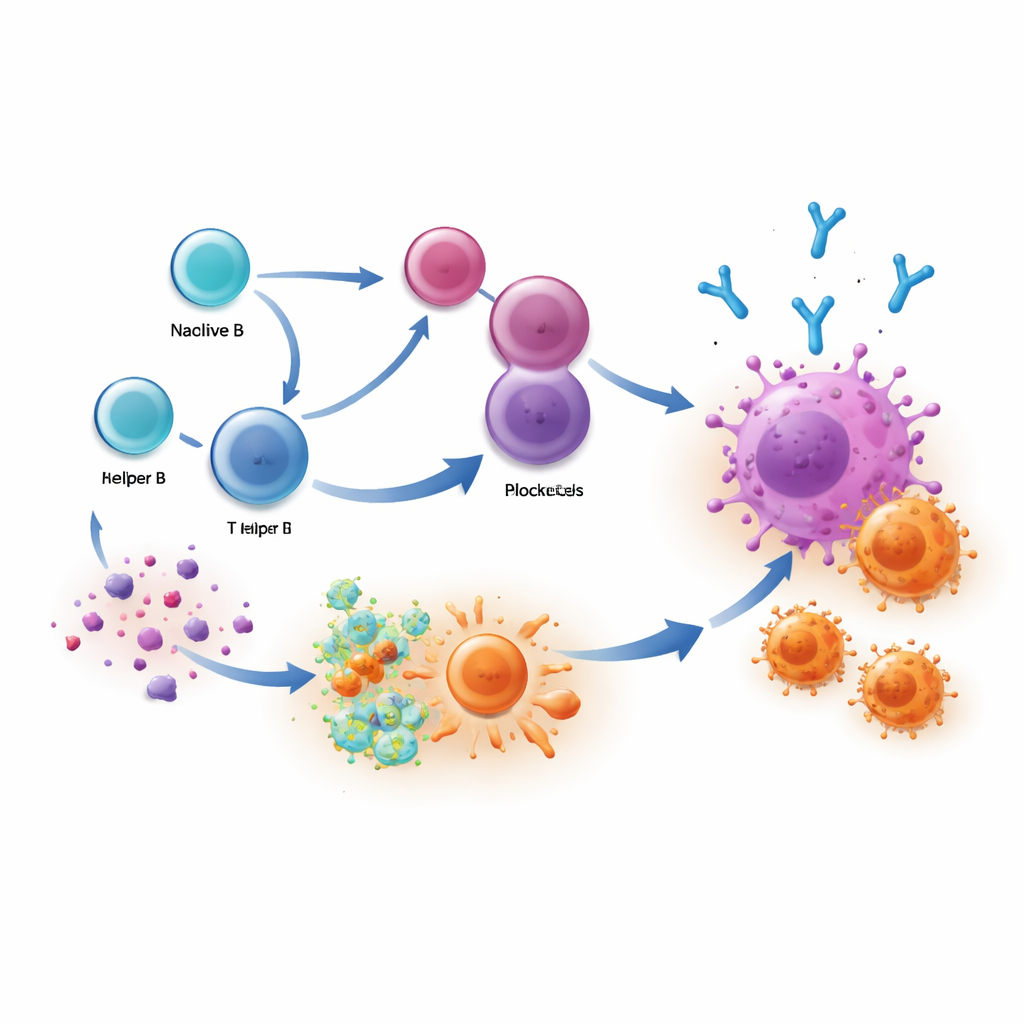
Wat dit betekent voor toekomstige behandelingen
Simpel gezegd doen patiënten het het beste wanneer hun immuunsysteem een tweesporige aanval uitvoert: IgG1-antilichamen van plasmacellen markeren kankercellen, en T-cellen rukken op om te doden. Deze studie toont aan dat checkpointtherapieën deze antilichaamresponsen kunnen versterken, vooral wanneer nuttige B-celklonen vóór de behandeling aanwezig zijn. Het meten van IgG1-rijke plasmacellen of hun antilichamen in bloed- en tumormonsters kan artsen helpen waarschijnlijke responders te identificeren en te monitoren hoe goed de behandeling werkt. Op lange termijn kunnen vaccins of geneesmiddelen die B-cellen sturen richting het maken van meer van deze precieze, tumorgeneigde IgG1-antilichamen de voordelen van immunotherapie vergroten en duurzame responsen voor meer mensen met kanker mogelijk maken.
Bronvermelding: Gonzalez-Kozlova, E., Sweeney, R., Figueiredo, I. et al. Humoral IgG1 responses to tumor antigens underpin clinical outcomes in immune checkpoint blockade. Nat Med 32, 978–991 (2026). https://doi.org/10.1038/s41591-025-04177-6
Trefwoorden: kankerimmunotherapie, B-cellen, IgG1-antilichamen, immuuncheckpointremming, hepatocellulair carcinoom